在一固定容积的密闭容器中,充入2 mol CO2和1 mol H2发生如下化学反应:CO2(g)+H2(g)⇌CO(g)+H2O(g),其化学平衡常数与温度(T)的关系如表:
回答下列问题:
(1)该反应的化学平衡常数表达式为K=__________ 。
(2)若反应在830℃下达到平衡,则CO2气体的转化率为_________ 。
(3)若绝热时(容器内外没有热量交换),平衡发生移动的结果是使容器内CO的浓度增大,则容器内气体温度_________ (填“升高”、“降低”或“不能确定”)。
(4)在830℃达平衡后在其容器中分别又充入1 mol CO2 和1 molCO后,该反应的v正__ v逆(填“大于”“小于”“等于”)。
| T/℃ | 700 | 800 | 830 | 1 000 | 1 200 |
| K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
回答下列问题:
(1)该反应的化学平衡常数表达式为K=
(2)若反应在830℃下达到平衡,则CO2气体的转化率为
(3)若绝热时(容器内外没有热量交换),平衡发生移动的结果是使容器内CO的浓度增大,则容器内气体温度
(4)在830℃达平衡后在其容器中分别又充入1 mol CO2 和1 molCO后,该反应的v正
更新时间:2020-11-22 06:48:00
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】(1)在一定温度下,有下列反应发生:Fe2O3(s)+3CO(g) ⇌2Fe(s)+3CO2(g),该反应的平衡常数表达式K=________ 。
(2)在配制FeCl3溶液时,加入少许浓盐酸,其目的是:_____________ ;不断加热FeCl3溶液,蒸干其水分并灼烧固体,最后得到的物质是________ 。
(3)已知:Fe2O3(s)+ C(s)=
C(s)= CO2(g)+2Fe(s) ΔH=+234.1 kJ/mol
CO2(g)+2Fe(s) ΔH=+234.1 kJ/mol
C(s)+O2(g)===CO2(g) ΔH=-393.5 kJ/mol
则2Fe(s)+ O2(g)===Fe2O3(s)的ΔH是
O2(g)===Fe2O3(s)的ΔH是____________________ 。
(4)Fe(OH)2在空气中短时间内可被氧化为Fe(OH)3,发生的反应为:4Fe(OH)2+O2+2H2O=4Fe(OH)3,下列说法中错误的是________ (填字母)。
A.该反应是能自发进行的反应
B.该反应是熵增加的反应
C.该反应是化合反应
D.该反应是氧化还原反应
(2)在配制FeCl3溶液时,加入少许浓盐酸,其目的是:
(3)已知:Fe2O3(s)+
 C(s)=
C(s)= CO2(g)+2Fe(s) ΔH=+234.1 kJ/mol
CO2(g)+2Fe(s) ΔH=+234.1 kJ/molC(s)+O2(g)===CO2(g) ΔH=-393.5 kJ/mol
则2Fe(s)+
 O2(g)===Fe2O3(s)的ΔH是
O2(g)===Fe2O3(s)的ΔH是(4)Fe(OH)2在空气中短时间内可被氧化为Fe(OH)3,发生的反应为:4Fe(OH)2+O2+2H2O=4Fe(OH)3,下列说法中错误的是
A.该反应是能自发进行的反应
B.该反应是熵增加的反应
C.该反应是化合反应
D.该反应是氧化还原反应
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】1913年,德国化学家哈伯实现了合成氨的工业化生产,被称作解救世界粮食危机的化学天才,现将1molN2和3molH2投入1L的密闭容器,在一定条件下,利用反应模拟哈伯合成氨的工业化生产:N2(g)+3H2(g) 2NH3(g)
2NH3(g)  H<0. 回答下列问题:
H<0. 回答下列问题:
(1)合成氨反应平衡常数的表达式为_______ 。温度升高,K值_______ (填“增大”“减小”或“不变"):使用催化剂,K值_______ (填“增大“减小”或“不变”)。
(2)反应的 S
S_______ 0(填“>”“<"或“=”)
(3)有利于提高平衡混合物中氨含量的条件有_______ (填序号)。
A.低温 B.高温 C.低压 D.高压 E.催化剂
(4)当反应达到平衡后,向体系中充入N2的,平衡_______ 移动(填“正向”“逆向”或“不”);给体系升温,
_______ (填“增大”“减小”或不变”),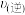
_______ (填“增大”“减小”或“不变”),平衡_______ 移动(填“正向”“逆向”或“不”)。
 2NH3(g)
2NH3(g)  H<0. 回答下列问题:
H<0. 回答下列问题:(1)合成氨反应平衡常数的表达式为
(2)反应的
 S
S(3)有利于提高平衡混合物中氨含量的条件有
A.低温 B.高温 C.低压 D.高压 E.催化剂
(4)当反应达到平衡后,向体系中充入N2的,平衡

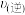
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】在相同温度下,向1L的恒容密闭容器中,按照如下方式投料,
已知:2HI(g)⇌H2(g)+I2(g) ΔH=+26.5 kJ·mol-1。
(1)已知甲容器中,H2物质的量随时间的变化如右图所示:
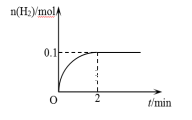
①0~2min内的平均反应速率v(H2)=____ 。
②该温度下反应的平衡常数K1=____ 。若温度升高,则K1____ (填“变大”或“变小”)。
③下列各项能说明反应在该温度下已达到平衡状态的是____ 。
A.各组分浓度不变 B.混合气体密度不变
C.v(H2)=0 D.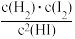 恒定
恒定
(2)对比甲、乙、丙,回答下列问题:
①K1、K2、K3的大小关系是____ 。
②下列物理量中,乙为甲的2倍的是____ 。
A.平衡常数 B.HI的平衡浓度
C.达到平衡的时间 D.平衡时H2的体积分数
(3)已知相同温度下,反应2HBr(g)⇌H2(g)+Br2(g)的平衡常数为KHBr,反应2HI(g)⇌H2(g)+I2(g)的平衡常数为KHI,且KHI>KHBr,下列推断正确的是____ 。
A.相同条件下,平衡时的转化率:HI>HBr B.分解的速率:HI>HBr
C.氧化性:Br2>I2D.HX的稳定性:HI>HBr
| 容器 | HI(g) | H2(g) | I2(g) | 平衡常数 |
| 甲 | 1 | 0 | 0 | K1 |
| 乙 | 2 | 0 | 0 | K2 |
| 丙 | 0 | 0.5 | 0.5 | K3 |
已知:2HI(g)⇌H2(g)+I2(g) ΔH=+26.5 kJ·mol-1。
(1)已知甲容器中,H2物质的量随时间的变化如右图所示:

①0~2min内的平均反应速率v(H2)=
②该温度下反应的平衡常数K1=
③下列各项能说明反应在该温度下已达到平衡状态的是
A.各组分浓度不变 B.混合气体密度不变
C.v(H2)=0 D.
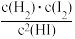 恒定
恒定(2)对比甲、乙、丙,回答下列问题:
①K1、K2、K3的大小关系是
②下列物理量中,乙为甲的2倍的是
A.平衡常数 B.HI的平衡浓度
C.达到平衡的时间 D.平衡时H2的体积分数
(3)已知相同温度下,反应2HBr(g)⇌H2(g)+Br2(g)的平衡常数为KHBr,反应2HI(g)⇌H2(g)+I2(g)的平衡常数为KHI,且KHI>KHBr,下列推断正确的是
A.相同条件下,平衡时的转化率:HI>HBr B.分解的速率:HI>HBr
C.氧化性:Br2>I2D.HX的稳定性:HI>HBr
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】在容积为1.00 L的容器中,通入一定量的N2O4,发生反应N2O4(g) 2NO2(g),随温度升高,混合气体的颜色变深。
2NO2(g),随温度升高,混合气体的颜色变深。

(1)反应为_______ (填“吸热”或“放热”);100 ℃时,体系中各物质浓度随时间变化如图所示。在0~60 s,反应速率v(N2O4)为__________ mol·L-1·s-1;反应的平衡常数K1为_____________ 。
(2)100 ℃时达平衡后,改变反应温度为T,c(N2O4) 以0.001 0 mol·L-1·s-1的平均速率降低,经10 s又达到平衡。
①T________ 100 ℃(填“大于”或“小于”),
②温度T时反应的平衡常数K2_________ 。
 2NO2(g),随温度升高,混合气体的颜色变深。
2NO2(g),随温度升高,混合气体的颜色变深。
(1)反应为
(2)100 ℃时达平衡后,改变反应温度为T,c(N2O4) 以0.001 0 mol·L-1·s-1的平均速率降低,经10 s又达到平衡。
①T
②温度T时反应的平衡常数K2
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】随着科学技术发展和环保要求的不断提高,CO2的捕集利用技术成为研究的重点。
(1)目前国际空间站处理CO2的一个重要方法是将CO2还原,所涉及反应的化学方程式为:CO2(g)+4H2(g)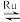 CH4(g)+2H2O(g)。已知H2的体积分数随温度的升高而增加。若温度从300℃升到400℃,重新达到平衡,判断下列表格中各物理量的变化(选填“增大”“减小”或“不变”)。
CH4(g)+2H2O(g)。已知H2的体积分数随温度的升高而增加。若温度从300℃升到400℃,重新达到平衡,判断下列表格中各物理量的变化(选填“增大”“减小”或“不变”)。
(2)相同温度时,上述反应在不同起始浓度下分别达到平衡,各物质的平衡浓度如下表:
a、b、x、y与m、n、p、q之间的关系式为___________ 。
(3)恒温条件下,该反应一定达到化学平衡状态的依据是___________ (填字母)。
a、c(CO2)=c(CH4) b、容器中的压强不变
c、K不变 d、c(H2)保持不变
e、v正(H2)=4v正(CO2) f、混合气体平均摩尔质量不变
(4)若某温度下,平衡时各物质的浓度符合下列关系:c(CO2)·c4(H2)=c(CH4)·c2(H2O),在此温度下,若某容器中含有1.2molCO2、2molH2、0.6molCH4、2molH2O,则此时反应所处的状态为_______ (填“向正反应方向进行”、“向逆反应方向进行”、“平衡状态”或“无法判断”)。
(1)目前国际空间站处理CO2的一个重要方法是将CO2还原,所涉及反应的化学方程式为:CO2(g)+4H2(g)
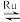 CH4(g)+2H2O(g)。已知H2的体积分数随温度的升高而增加。若温度从300℃升到400℃,重新达到平衡,判断下列表格中各物理量的变化(选填“增大”“减小”或“不变”)。
CH4(g)+2H2O(g)。已知H2的体积分数随温度的升高而增加。若温度从300℃升到400℃,重新达到平衡,判断下列表格中各物理量的变化(选填“增大”“减小”或“不变”)。| v(正) | v(逆) | 平衡常数(K) | CO2转化率(α) |
| 平衡时浓度 | CO2/(mol·L-1) | H2/(mol·L-1) | CH4/(mol·L-1) | H2O/(mol·L-1) |
| 平衡Ⅰ | a | b | x | y |
| 平衡Ⅱ | m | n | p | q |
(3)恒温条件下,该反应一定达到化学平衡状态的依据是
a、c(CO2)=c(CH4) b、容器中的压强不变
c、K不变 d、c(H2)保持不变
e、v正(H2)=4v正(CO2) f、混合气体平均摩尔质量不变
(4)若某温度下,平衡时各物质的浓度符合下列关系:c(CO2)·c4(H2)=c(CH4)·c2(H2O),在此温度下,若某容器中含有1.2molCO2、2molH2、0.6molCH4、2molH2O,则此时反应所处的状态为
您最近一年使用:0次
【推荐3】反应 可用于汽车尾气净化。在恒温恒容密闭容器中加入一定量反应物,获得如下数据:
可用于汽车尾气净化。在恒温恒容密闭容器中加入一定量反应物,获得如下数据:
(1)
___________ ,
___________ 。
(2)CO的平衡转化率为___________ 。
(3)该温度下该反应的K的数值为___________ 。
(4)该温度下,按未知浓度配比进行反应,某时刻测得如下数据:
此时反应向___________ 方向(填“正反应”或者“逆反应”)进行,结合计算说明理由:___________ 。
 可用于汽车尾气净化。在恒温恒容密闭容器中加入一定量反应物,获得如下数据:
可用于汽车尾气净化。在恒温恒容密闭容器中加入一定量反应物,获得如下数据: |  | 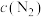 |  | |
起始时各物质的物质的量浓度/( ) ) | 0.4 | 0.4 | 0 | 0 |
平衡时各物质的物质的量浓度/( ) ) | 0.2 | x | y | z |


(2)CO的平衡转化率为
(3)该温度下该反应的K的数值为
(4)该温度下,按未知浓度配比进行反应,某时刻测得如下数据:
 |  | 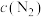 |  | |
某时刻各物质的物质的量浓度/( ) ) | 0.5 | 0.5 | 0.1 | 0.5 |
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】CS2是一种重要的化工原料。工业上可以利用硫(S8)与CH4为原料制备CS2,S8受热分解成气态S2,发生反应2S2(g)+CH4(g) CS2(g)+2H2S(g),某温度下,若S8完全分解成气态S2.在恒温密闭容器中,S2与CH4物质的量比为2∶1时开始反应。
CS2(g)+2H2S(g),某温度下,若S8完全分解成气态S2.在恒温密闭容器中,S2与CH4物质的量比为2∶1时开始反应。
(1)当CS2的体积分数为10%时,CH4的转化率为___________
(2)当以下数值不变时,能说明该反应达到平衡的是___________ (填序号)
a.气体密度 b.气体总压 c.CH4与S2体积比 d.CS2的体积分数
 CS2(g)+2H2S(g),某温度下,若S8完全分解成气态S2.在恒温密闭容器中,S2与CH4物质的量比为2∶1时开始反应。
CS2(g)+2H2S(g),某温度下,若S8完全分解成气态S2.在恒温密闭容器中,S2与CH4物质的量比为2∶1时开始反应。(1)当CS2的体积分数为10%时,CH4的转化率为
(2)当以下数值不变时,能说明该反应达到平衡的是
a.气体密度 b.气体总压 c.CH4与S2体积比 d.CS2的体积分数
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】一定温度下将3molA及3molB混合于2L的密闭容器中,发生如下反应3A(g)+B(g)  xC(g)+2D(g),经过5分钟后反应达到平衡,测得A的转化率为60%,C的平均反应速率是0.18mol/(L▪min)。求:
xC(g)+2D(g),经过5分钟后反应达到平衡,测得A的转化率为60%,C的平均反应速率是0.18mol/(L▪min)。求:
(1)平衡时B的浓度=___ mol/L。
(2)D的平均反应速率v(D)=___ mol/(L·min)。
(3)x=___ 。
 xC(g)+2D(g),经过5分钟后反应达到平衡,测得A的转化率为60%,C的平均反应速率是0.18mol/(L▪min)。求:
xC(g)+2D(g),经过5分钟后反应达到平衡,测得A的转化率为60%,C的平均反应速率是0.18mol/(L▪min)。求:(1)平衡时B的浓度=
(2)D的平均反应速率v(D)=
(3)x=
您最近一年使用:0次



