向含有0.2 mol FeI2的溶液中加入a mol Br2。下列叙述不正确的是
| A.当a=0.1时,发生的反应为2I-+Br2=I2+2Br- |
| B.当a=0.25时,发生的反应为2Fe2++4I-+3Br2=2Fe3++2I2+6Br- |
| C.当溶液中I-有一半被氧化时,c(I-):c(Br-)=1:1 |
| D.当a=0.28时, 4Fe2++10I-+7Br2=4Fe3++5I2+14Br- |
17-18高三上·河北石家庄·阶段练习 查看更多[2]
更新时间:2017-12-06 15:32:22
|
相似题推荐
单选题
|
较难
(0.4)
【推荐1】下列离子方程式书写正确的是
| A.石灰乳与Na2CO3溶液混合:Ca2++CO32-=CaCO3↓ |
| B.酸性条件下KIO3溶液与KI溶液发生反应生成I2:IO3-+5I-+3H2O=3I2+6OH- |
C.NH4HSO3溶液与足量的NaOH溶液混合加热:NH4++HSO3-+2OH- NH3↑+SO32-+2H2O NH3↑+SO32-+2H2O |
| D.AgNO3溶液中加入过量的氨水:Ag++NH3•H2O=AgOH↓+NH4+ |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐2】下列离子方程式不正确的是
| A.硫酸铁溶液中滴入硫氰化钾溶液:Fe3++3SCN-=Fe(SCN)3 |
| B.少量SO2气体通入足量的NaClO溶液中:SO2+H2O+ClO-=Cl-+ SO42-+2H+ |
| C.硫酸氢钠溶液中滴加氢氧化钡溶液至中性:Ba2++2OH-+ 2H++ SO42-=BaSO4↓+2H2O |
| D.含0. 03 mol NaHCO3的溶液和0.02 mol Ca(OH)2的溶液混合:3HCO3-+2Ca2++3OH-=CO32-+ 2CaCO3↓+3H2O |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐1】某小组同学设计如下实验能证实反应2Fe3++2I-=2Fe2++I2为可逆反应。已知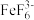 是一种无色的稳定的络离子。
是一种无色的稳定的络离子。
下列说法不正确的是
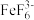 是一种无色的稳定的络离子。
是一种无色的稳定的络离子。| 实验装置 | 实验序号 | 实验操作和现象 |
 注:a、b均为石墨电极 | ① | ⅰ.闭合K,指针向右偏转 ⅱ.待指针归零,向U形管左管中加入1mol/LKI溶液,∙∙∙∙∙∙ |
| ② | ⅰ.闭合K,指针向右偏转 ⅱ.待指针归零,向U形管左管中滴加0.01mol/LAgNO3溶液,指针向左偏转。 |
| A.电流表指针归零,说明上述可逆反应达到了化学平衡状态 |
| B.①中加入KI溶液后,上述平衡向正反应方向移动,电流表指针向右偏转 |
| C.②中加入AgNO3溶液后,导致氧化性:Fe3+ >I2,上述平衡向逆反应方向移动 |
| D.②中电流表指针再次归零时,向U型管右管滴加饱和NH4F溶液,电流表指针向左偏转 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐2】向含有FeBr2溶液中通入一定量的Cl2(还原性:Fe2+>Br-),表示该反应的离子方程式肯定错误的是( )
| A.2Fe2++Cl2=2Fe3++2Cl- |
| B.10Fe2++2Br-+6Cl2=10Fe3++Br2+12Cl- |
| C.2Br-+Cl2=Br2+2Cl- |
| D.2Fe2++4Br-+3Cl2=2Br2+2Fe3++6Cl- |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐1】对于Cu+2H2SO4(浓)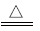 CuSO4+SO2↑+2H2O反应,下列说法正确的是( )
CuSO4+SO2↑+2H2O反应,下列说法正确的是( )
 CuSO4+SO2↑+2H2O反应,下列说法正确的是( )
CuSO4+SO2↑+2H2O反应,下列说法正确的是( )| A.Cu作还原剂,发生还原反应 |
| B.被还原的H2SO4与参加反应的H2SO4的物质的量比为1∶2 |
| C.当生成2.24 L(标准状况下)SO2时,转移的电子为2mol |
| D.当Cu足量时,H2SO4可完全反应 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐2】已知三个反应:①16H++10M-+2XO =2X2++5M2+8H2O;②2A2++B2=2A3++2B-;③2B-+M2=B2+2M-。下列结论不正确的是
=2X2++5M2+8H2O;②2A2++B2=2A3++2B-;③2B-+M2=B2+2M-。下列结论不正确的是
 =2X2++5M2+8H2O;②2A2++B2=2A3++2B-;③2B-+M2=B2+2M-。下列结论不正确的是
=2X2++5M2+8H2O;②2A2++B2=2A3++2B-;③2B-+M2=B2+2M-。下列结论不正确的是| A.还原性:B->X2+ |
B.氧化性: XO >B2>A3+ >B2>A3+ |
| C.X2+只有还原性 |
| D.溶液中可以发生M2+2A2+=2A3++2M- |
您最近一年使用:0次

 溶液中加入过量醋酸溶液:
溶液中加入过量醋酸溶液: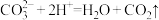
 溶液中通入过量
溶液中通入过量 :
: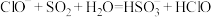
 溶液中加入
溶液中加入 溶液:
溶液: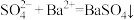

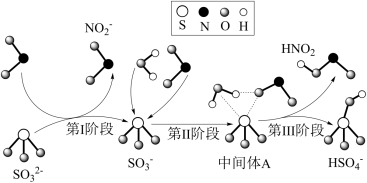
 ,还原性:SO
,还原性:SO


