(1)aH2 O2+bO3=== cO2+dH2O中,a:b: c:d为________ 。
(2)3S+6KOH===2K2S+K2SO3+3H2O中,被氧化和被还原的硫元素物质的量之比为________ 。
(3)5NH4NO3===4N2↑+2HNO3+9H2O中,反应中发生氧化反应和发生还原反应的氮原子物质的量之比为________ 。
(4)12.4 g Na2R含Na+ 0.4 mol,则Na2R的摩尔质量为________ ,R的相对原子质量为________ 。
(5)体积均为aL的硫酸钾、硫酸锌、硫酸铁溶液,均能和bL1mol/LBaCl2溶液恰好完全反应。则硫酸钾、硫酸锌、硫酸铁的物质的量浓度之比约为________ 。
(2)3S+6KOH===2K2S+K2SO3+3H2O中,被氧化和被还原的硫元素物质的量之比为
(3)5NH4NO3===4N2↑+2HNO3+9H2O中,反应中发生氧化反应和发生还原反应的氮原子物质的量之比为
(4)12.4 g Na2R含Na+ 0.4 mol,则Na2R的摩尔质量为
(5)体积均为aL的硫酸钾、硫酸锌、硫酸铁溶液,均能和bL1mol/LBaCl2溶液恰好完全反应。则硫酸钾、硫酸锌、硫酸铁的物质的量浓度之比约为
17-18高一上·湖北武汉·期中 查看更多[2]
更新时间:2017-12-12 18:51:51
|
相似题推荐
填空题
|
较难
(0.4)
解题方法
【推荐1】向100mLBaCl2、AlCl3和FeCl3的混合溶液A中,逐滴加入Na2SO4和NaOH的混合溶液B,产生的沉淀的物质的量(n)和加入溶液B的体积(V)关系如图。
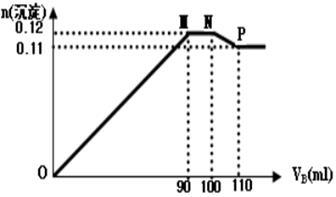
(1)当加入B溶液110mL时,溶液中的沉淀为(化学式)____________________
(2)从90 mL至100 mL之间加入10 mL B溶液时发生的离子反应方程式①_________________ ;②________________ ;并由此可以分析出溶液B中Na2SO4与NaOH物质的量浓度之比为________________ 。
(3)通过计算分析可知:
B溶液中NaOH物质的量浓度为_____________ mol/L;
A溶液中FeCl3物质的量浓度为______________ mol/L。

(1)当加入B溶液110mL时,溶液中的沉淀为(化学式)
(2)从90 mL至100 mL之间加入10 mL B溶液时发生的离子反应方程式①
(3)通过计算分析可知:
B溶液中NaOH物质的量浓度为
A溶液中FeCl3物质的量浓度为
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
【推荐2】已知硫酸、氨水的密度与所加水量的关系如图所示:
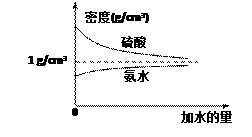
现有硫酸与氨水各一份,请根据表中信息,回答下列问题:
⑴ ρ1、ρ2、ρ3、ρ4由大到小的顺序为:________ 。
⑵ 表中2 mol·L-1氨水的质量分数为:________ 。
⑶ 将4 mol·L-1的氨水与2 mol·L-1的氨水等质量混合,所得氨水的物质的量浓度是_____ (填序号)。
A.>3 mol·L-1 B.=3 mol·L-1 C.<3 mol·L-1 D.无法判断
⑷ 将20%的硫酸与10%的硫酸等体积混合,所得硫酸溶液的质量分数是______ (填序号)。
A.>15% B.=15% C.<15% D.无法判断
⑸ 100g浓度为4 mol·L-1的硫酸溶液与_________ mL水混合,能使硫酸的物质的量浓度减小到2 mol·L-1。

现有硫酸与氨水各一份,请根据表中信息,回答下列问题:
| 溶液 | 溶质的物质的量浓度 | 溶液的密度/g·cm-3 |
| 硫酸 | 4 mol·L-1 | ρ1 |
| 2 mol·L-1 | ρ2 | |
| 氨水 | 4 mol·L-1 | ρ3 |
| 2 mol·L-1 | ρ4 |
⑴ ρ1、ρ2、ρ3、ρ4由大到小的顺序为:
⑵ 表中2 mol·L-1氨水的质量分数为:
⑶ 将4 mol·L-1的氨水与2 mol·L-1的氨水等质量混合,所得氨水的物质的量浓度是
A.>3 mol·L-1 B.=3 mol·L-1 C.<3 mol·L-1 D.无法判断
⑷ 将20%的硫酸与10%的硫酸等体积混合,所得硫酸溶液的质量分数是
A.>15% B.=15% C.<15% D.无法判断
⑸ 100g浓度为4 mol·L-1的硫酸溶液与
您最近一年使用:0次
填空题
|
较难
(0.4)
【推荐3】右图为实验室某浓盐酸试剂瓶标签上的有关数据,根据有关数据回答下列问题:
(1)该浓盐酸中HCl的物质的量浓度为_________ mol/L。
(2)取用任意体积的该盐酸溶液时,下列物理量不随所取体积多少 而变化的是______________ 。
A、溶液中HCl的质量 B、溶液的p H
C、溶液中H+的数目 D、溶液的密度
(3)欲配制上述浓盐酸,需要在1L水中通入标态下___________ L
HCl气体(保留1位小数)
(4)现有1L1mol/L的稀盐酸,欲使其浓度增大1倍,采取的措施合理的是______________ 。
A、通入标况下HCl气体22.4L B、将溶液加热浓缩至0.5L
C、加入5mol/L的盐酸0.6L,再稀释至2L。 D、加入1L 3mol/L的盐酸混合均匀。
| 盐酸 分子式:HCl 相对分子质量:36.5 密度:1.19g/m3 质量分数:36.5% |
(1)该浓盐酸中HCl的物质的量浓度为
(2)取用任意体积的该盐酸溶液时,下列物理量不随所取体积多少 而变化的是
A、溶液中HCl的质量 B、溶液的p H
C、溶液中H+的数目 D、溶液的密度
(3)欲配制上述浓盐酸,需要在1L水中通入标态下
HCl气体(保留1位小数)
(4)现有1L1mol/L的稀盐酸,欲使其浓度增大1倍,采取的措施合理的是
A、通入标况下HCl气体22.4L B、将溶液加热浓缩至0.5L
C、加入5mol/L的盐酸0.6L,再稀释至2L。 D、加入1L 3mol/L的盐酸混合均匀。
您最近一年使用:0次
【推荐1】写出下列反应的离子方程式(已知还原性: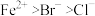 ):
):
(1)向 溶液中通入少量
溶液中通入少量 (
( 与
与 的微粒数的比值
的微粒数的比值 ):
):_________ ;
(2)向 溶液中通入足量
溶液中通入足量 :
:______ ;
(3)向 溶液中通入
溶液中通入 ,
, 与
与 的化学计量数之比为
的化学计量数之比为 :
:______ 。
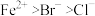 ):
):(1)向
 溶液中通入少量
溶液中通入少量 (
( 与
与 的微粒数的比值
的微粒数的比值 ):
):(2)向
 溶液中通入足量
溶液中通入足量 :
:(3)向
 溶液中通入
溶液中通入 ,
, 与
与 的化学计量数之比为
的化学计量数之比为 :
:
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
【推荐2】(1)用KClO3在H2SO4存在下与SO2反应制得ClO2。请写出反应的离子方程式:______ 。
(2)把ag固体NaHCO3加热分解一段时间后,固体质量变为b g。
①尚未分解的NaHCO3质量为________ g。
②当b为________ g时,表明NaHCO3完全分解。
(3)NaNO2因外观和食盐相似,又有咸味,容易使人误食中毒。已知NaNO2能发生如下反应:2NaNO2+4HI===2NO↑+I2+2NaI+2H2O。
①上述反应中氧化剂是__________________ 。
②根据上述反应,鉴别NaNO2和NaCl。可选用的物质有:①水、②碘化钾淀粉试纸、
③淀粉、④白酒、⑤食醋,你认为必须选用的物质有___________ (填序号)。
③某厂废液中,含有2%~5%的NaNO2,直接排放会造成污染,下列试剂能使NaNO2转化为不引起二次污染的N2的是________ (填编号)。
A.NaCl B.NH4Cl C.HNO3 D.浓H2SO4
④请配平以下化学方程式:________ □Al+□NaNO3+□NaOH===□NaAlO2+□N2↑+2H2O。若反应过程中转移5 mole-,则生成标准状况下N2的体积为________ L。
(2)把ag固体NaHCO3加热分解一段时间后,固体质量变为b g。
①尚未分解的NaHCO3质量为
②当b为
(3)NaNO2因外观和食盐相似,又有咸味,容易使人误食中毒。已知NaNO2能发生如下反应:2NaNO2+4HI===2NO↑+I2+2NaI+2H2O。
①上述反应中氧化剂是
②根据上述反应,鉴别NaNO2和NaCl。可选用的物质有:①水、②碘化钾淀粉试纸、
③淀粉、④白酒、⑤食醋,你认为必须选用的物质有
③某厂废液中,含有2%~5%的NaNO2,直接排放会造成污染,下列试剂能使NaNO2转化为不引起二次污染的N2的是
A.NaCl B.NH4Cl C.HNO3 D.浓H2SO4
④请配平以下化学方程式:
您最近一年使用:0次
【推荐3】二氧化氯( )是一种黄绿色到橙黄色的气体。工业上制备二氧化氯的方法之一是用甲醇在酸性介质中与氯酸钠反应。二氧化氯能与许多化学物质发生爆炸性反应,遇水则生成次氯酸、氯气和氧气。回答下列问题:
)是一种黄绿色到橙黄色的气体。工业上制备二氧化氯的方法之一是用甲醇在酸性介质中与氯酸钠反应。二氧化氯能与许多化学物质发生爆炸性反应,遇水则生成次氯酸、氯气和氧气。回答下列问题:
(1)将二氧化氯通入品红溶液中,溶液褪色的原因是_______ 。
(2)配平下列反应的化学方程式:_______ 。
_______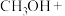 _______
_______ _______= CO2↑_______
_______= CO2↑_______ _______
_______ _______
_______
(3)上述反应中,被氧化的元素是_______ 。还原产物与氧化产物的物质的量之比是_______ 。
(4)根据上述反应可推知_______ (填字母)。
a.氧化性: b.氧化性:
b.氧化性: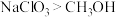
c.还原性: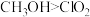 d.还原性:
d.还原性:
(5)若转移的电子数目为 (
( 为阿伏加德罗常数的值)则反应产生气体的体积约为
为阿伏加德罗常数的值)则反应产生气体的体积约为_______ L(标准状况)。
 )是一种黄绿色到橙黄色的气体。工业上制备二氧化氯的方法之一是用甲醇在酸性介质中与氯酸钠反应。二氧化氯能与许多化学物质发生爆炸性反应,遇水则生成次氯酸、氯气和氧气。回答下列问题:
)是一种黄绿色到橙黄色的气体。工业上制备二氧化氯的方法之一是用甲醇在酸性介质中与氯酸钠反应。二氧化氯能与许多化学物质发生爆炸性反应,遇水则生成次氯酸、氯气和氧气。回答下列问题:(1)将二氧化氯通入品红溶液中,溶液褪色的原因是
(2)配平下列反应的化学方程式:
_______
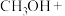 _______
_______ _______= CO2↑_______
_______= CO2↑_______ _______
_______ _______
_______(3)上述反应中,被氧化的元素是
(4)根据上述反应可推知
a.氧化性:
 b.氧化性:
b.氧化性: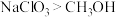
c.还原性:
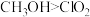 d.还原性:
d.还原性:
(5)若转移的电子数目为
 (
( 为阿伏加德罗常数的值)则反应产生气体的体积约为
为阿伏加德罗常数的值)则反应产生气体的体积约为
您最近一年使用:0次
填空题
|
较难
(0.4)
【推荐1】某工业废水中含有CN-和Cr2O72—等离子,需经污水处理达标后才能排放,污水处理厂拟用下列流程进行处理:
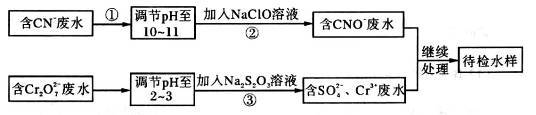
回答下列问题:
(1)步骤②中,CN-被ClO-氧化为CNO-的离子方程式为________________ 。
(2)步骤③的反应为S2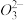 + Cr2
+ Cr2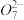 +H+
+H+ S
S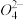 +Cr3++H2O(未配平),则每消耗0.4mol Cr2
+Cr3++H2O(未配平),则每消耗0.4mol Cr2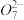 转移
转移__________ mol e-。
(3)含Cr3+废水可以加入熟石灰进一步处理,目的是____________________ 。
(4)在25℃下,将amol·L—1的NaCN溶液与0.01mol·L-1的盐酸等体积混合,反应后测得溶液pH=7,用含a的代数式表示HCN的电离常数Ka=_________________ 。若25ºC 时Ka=1×10-9则同体积均为0.1mol·L-1的NaCN、HCN的混合溶液中下列说法不正确的是_______
a.此溶液一定有C(Na+)+C(H+)=C(OH‾)+C(CN‾)
b.混合溶液中水的电离程度一定大于该温度下纯水的电离程度。
c.此溶液一定有C(Na+)=C(HCN)+ C(CN‾)
d.此溶液加入少量氢氧化钠或盐酸溶液的PH值变化不大
(5)取工业废水水样于试管中,加入NaOH溶液观察到有蓝色沉淀生成,继续加至不再产生蓝色沉淀为止,再向溶液中加入足量Na2S溶液,蓝色沉淀转化成黑色沉淀。该过程中反应的离子方程是____________ 。

回答下列问题:
(1)步骤②中,CN-被ClO-氧化为CNO-的离子方程式为
(2)步骤③的反应为S2
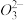 + Cr2
+ Cr2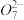 +H+
+H+ S
S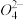 +Cr3++H2O(未配平),则每消耗0.4mol Cr2
+Cr3++H2O(未配平),则每消耗0.4mol Cr2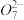 转移
转移(3)含Cr3+废水可以加入熟石灰进一步处理,目的是
(4)在25℃下,将amol·L—1的NaCN溶液与0.01mol·L-1的盐酸等体积混合,反应后测得溶液pH=7,用含a的代数式表示HCN的电离常数Ka=
a.此溶液一定有C(Na+)+C(H+)=C(OH‾)+C(CN‾)
b.混合溶液中水的电离程度一定大于该温度下纯水的电离程度。
c.此溶液一定有C(Na+)=C(HCN)+ C(CN‾)
d.此溶液加入少量氢氧化钠或盐酸溶液的PH值变化不大
(5)取工业废水水样于试管中,加入NaOH溶液观察到有蓝色沉淀生成,继续加至不再产生蓝色沉淀为止,再向溶液中加入足量Na2S溶液,蓝色沉淀转化成黑色沉淀。该过程中反应的离子方程是
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
【推荐2】铜是与人类关系非常密切的有色金属。已知:常温下,在溶液中 稳定,
稳定,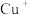 易在酸性条件下发生反应:
易在酸性条件下发生反应: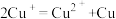 。大多数+1价铜的化合物是难溶物,
。大多数+1价铜的化合物是难溶物,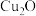 、CuI、CuCl、CuH等。
、CuI、CuCl、CuH等。
(1)在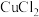 溶液中逐滴加入过量KI溶液可能发生以下反应:
溶液中逐滴加入过量KI溶液可能发生以下反应:
a.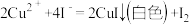
b.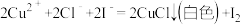 。
。
为顺利观察到白色沉淀可以加入的最佳试剂是________ 。
A. B.苯 C.NaOH溶液 D.乙醇
B.苯 C.NaOH溶液 D.乙醇
(2)一定条件下,在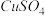 中加入
中加入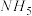 反应生成氢化亚铜(CuH)。
反应生成氢化亚铜(CuH)。
①已知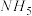 是离子化合物且所有原子都达到稀有气体的稳定结构,写出
是离子化合物且所有原子都达到稀有气体的稳定结构,写出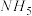 的电子式:
的电子式:__________ 。
②写出CuH在过量稀盐酸中有气体生成的离子方程式:____________ 。
(3)纳米级 具有特殊的光学、电学及光电化学性质,在太阳能电池、传感器、超导体等方面有着潜在的应用,研究制备纳米氧化亚铜的方法已成为当前的热点研究之一。
具有特殊的光学、电学及光电化学性质,在太阳能电池、传感器、超导体等方面有着潜在的应用,研究制备纳米氧化亚铜的方法已成为当前的热点研究之一。
方法一:在新制 浊液中滴入
浊液中滴入 水溶液,蓝色沉淀逐渐转化为砖红色,同时产生无色无味的气体。
水溶液,蓝色沉淀逐渐转化为砖红色,同时产生无色无味的气体。
①写出上述制备过程中的总反应方程式:_____________ 。
方法二:以铜作阳极,石墨作阴极电解。已知:铜作阳极时,铜先被氧化生成 ,后
,后 继续氧化生成
继续氧化生成 ;在碱性溶液中CuCl浊液易转化为
;在碱性溶液中CuCl浊液易转化为 。
。
②以NaOH溶液作为电解质溶液时需添加NaCl,其目的是______________ ,写出阳极反应式:______________ 。
③写出在碱性溶液中CuCl浊液转化为 的离子方程式:
的离子方程式:____________ 。
④这样制得的 中往往含有CuCl,请设计实验证明CuCl的存在:
中往往含有CuCl,请设计实验证明CuCl的存在:_________ 。
 稳定,
稳定,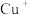 易在酸性条件下发生反应:
易在酸性条件下发生反应: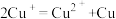 。大多数+1价铜的化合物是难溶物,
。大多数+1价铜的化合物是难溶物,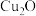 、CuI、CuCl、CuH等。
、CuI、CuCl、CuH等。(1)在
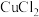 溶液中逐滴加入过量KI溶液可能发生以下反应:
溶液中逐滴加入过量KI溶液可能发生以下反应:a.
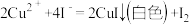
b.
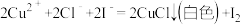 。
。为顺利观察到白色沉淀可以加入的最佳试剂是
A.
 B.苯 C.NaOH溶液 D.乙醇
B.苯 C.NaOH溶液 D.乙醇(2)一定条件下,在
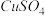 中加入
中加入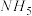 反应生成氢化亚铜(CuH)。
反应生成氢化亚铜(CuH)。①已知
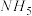 是离子化合物且所有原子都达到稀有气体的稳定结构,写出
是离子化合物且所有原子都达到稀有气体的稳定结构,写出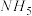 的电子式:
的电子式:②写出CuH在过量稀盐酸中有气体生成的离子方程式:
(3)纳米级
 具有特殊的光学、电学及光电化学性质,在太阳能电池、传感器、超导体等方面有着潜在的应用,研究制备纳米氧化亚铜的方法已成为当前的热点研究之一。
具有特殊的光学、电学及光电化学性质,在太阳能电池、传感器、超导体等方面有着潜在的应用,研究制备纳米氧化亚铜的方法已成为当前的热点研究之一。方法一:在新制
 浊液中滴入
浊液中滴入 水溶液,蓝色沉淀逐渐转化为砖红色,同时产生无色无味的气体。
水溶液,蓝色沉淀逐渐转化为砖红色,同时产生无色无味的气体。①写出上述制备过程中的总反应方程式:
方法二:以铜作阳极,石墨作阴极电解。已知:铜作阳极时,铜先被氧化生成
 ,后
,后 继续氧化生成
继续氧化生成 ;在碱性溶液中CuCl浊液易转化为
;在碱性溶液中CuCl浊液易转化为 。
。②以NaOH溶液作为电解质溶液时需添加NaCl,其目的是
③写出在碱性溶液中CuCl浊液转化为
 的离子方程式:
的离子方程式:④这样制得的
 中往往含有CuCl,请设计实验证明CuCl的存在:
中往往含有CuCl,请设计实验证明CuCl的存在:
您最近一年使用:0次
填空题
|
较难
(0.4)
【推荐3】磷单质及其化合物有广泛应用。
(1)三聚磷酸可视为三个磷酸分子之间脱去两个水分子的产物,三聚磷酸钠(俗称“磷酸五钠”)是常用的水处理剂,其化学式为________________ 。
(2)次磷酸钠(NaH2PO2)可用于化学镀镍。
①NaH2PO2中P元素的化合价为_________ 。
②化学镀镍的溶液中含有Ni2+和H2PO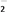 ,在酸性条件下发生下述反应,请配平:
,在酸性条件下发生下述反应,请配平:
____ Ni2++____ H2PO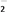 +
+____ ____ Ni++____ H2PO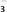 +
+____
(3)磷酸钙与焦炭、石英砂混合,在电炉中加热到1 500 ℃生成白磷,反应为
2Ca3(PO4)2+6SiO2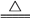 6CaSiO3+P4O10
6CaSiO3+P4O10
10C+P4O10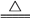 P4+10CO
P4+10CO
若反应生成31 g P4,则反应过程中转移的电子数为___________ (用NA表示阿伏伽德罗常数的值)。
(1)三聚磷酸可视为三个磷酸分子之间脱去两个水分子的产物,三聚磷酸钠(俗称“磷酸五钠”)是常用的水处理剂,其化学式为
(2)次磷酸钠(NaH2PO2)可用于化学镀镍。
①NaH2PO2中P元素的化合价为
②化学镀镍的溶液中含有Ni2+和H2PO
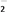 ,在酸性条件下发生下述反应,请配平:
,在酸性条件下发生下述反应,请配平: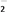 +
+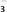 +
+(3)磷酸钙与焦炭、石英砂混合,在电炉中加热到1 500 ℃生成白磷,反应为
2Ca3(PO4)2+6SiO2
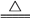 6CaSiO3+P4O10
6CaSiO3+P4O1010C+P4O10
 P4+10CO
P4+10CO若反应生成31 g P4,则反应过程中转移的电子数为
您最近一年使用:0次
填空题
|
较难
(0.4)
解题方法
【推荐1】已知Ca(OH)2与Cl2反应的氧化物与温度有关,在一定量的石灰乳中通入一定量的氯气,二者恰好完全反应(发生的反应均为放热反应),生成物中含有Cl-、ClO-、 三种含氧元素的离子,其中ClO-、
三种含氧元素的离子,其中ClO-、 两种离子的物质的量(n)与反应时间(t)的曲线
两种离子的物质的量(n)与反应时间(t)的曲线
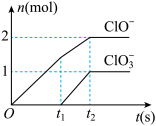
(1)t1前,氧化产物是_____________ (填化学式)。
(2)t2时,石灰乳与Cl2发生反应的总的离子方程式为:_______________ 。
(3)该反应中所消耗氯气的物质的量是______ mol。
(4)NaClO2较稳定,但加热或敲击亚氯酸钠固体时立即爆炸,其爆炸后的产物可能是__________(填字母)。
(5)配平下列离子方程式:Fe(OH)3+ClO-+OH-= +Cl-+H2O
+Cl-+H2O___________ 。
 三种含氧元素的离子,其中ClO-、
三种含氧元素的离子,其中ClO-、 两种离子的物质的量(n)与反应时间(t)的曲线
两种离子的物质的量(n)与反应时间(t)的曲线
(1)t1前,氧化产物是
(2)t2时,石灰乳与Cl2发生反应的总的离子方程式为:
(3)该反应中所消耗氯气的物质的量是
(4)NaClO2较稳定,但加热或敲击亚氯酸钠固体时立即爆炸,其爆炸后的产物可能是__________(填字母)。
| A.NaCl、Cl2 | B.NaCl、NaClO | C.NaClO3、NaClO4 | D.NaCl、NaClO3 |
 +Cl-+H2O
+Cl-+H2O
您最近一年使用:0次
填空题
|
较难
(0.4)
【推荐2】Ⅰ.煤炭中以FeS2形式存在的硫,在有水和空气及在脱硫微生物存在下发生生物氧化还原反应,有关反应的离子方程式依次为:
①2FeS2+7O2+2H2O 4H++2Fe2++4SO
4H++2Fe2++4SO ;
;
②Fe2++O2+H+ Fe3++________;
Fe3++________;
③FeS2+2Fe3+ 3Fe2++2S;
3Fe2++2S;
④2S+3O2+2H2O 4H++2SO
4H++2SO 。
。
已知:FeS2中的硫元素为-1价。
回答下列问题:
(1)根据质量守恒定律和电荷守恒定律,将上述②离子方程式配平并补充完整_______ 。
(2)反应③的还原剂是__________________ 。
(3)观察上述反应,硫元素最终转化为____________ 从煤炭中分离出来。
Ⅱ.在淀粉KI溶液中,滴入少量NaClO溶液,溶液立即变蓝,有关反应的离子方程式是____________________________ 。在上述蓝色溶液中,继续滴加足量的NaClO溶液,蓝色逐渐消失,有关反应的离子方程式是_______________________ 。(提示:碘元素被氧化成IO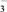 )从以上实验可知,ClO-、I2、IO
)从以上实验可知,ClO-、I2、IO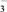 的氧化性由强到弱的顺序是
的氧化性由强到弱的顺序是________________ 。
Ⅲ.工业上用黄铜矿( CuFeS2)冶炼铜,副产品中有SO2,冶炼铜的反应为8CuFeS2+21O2 8Cu+4FeO+2Fe2O3+16SO2。若CuFeS2中 Fe 的化合价为+2 ,反应中被还原的元素是
8Cu+4FeO+2Fe2O3+16SO2。若CuFeS2中 Fe 的化合价为+2 ,反应中被还原的元素是________ (填元素符号)。当生成0.8 mol 铜时,此反应转移的电子数目是________ 。
①2FeS2+7O2+2H2O
 4H++2Fe2++4SO
4H++2Fe2++4SO ;
;②Fe2++O2+H+
 Fe3++________;
Fe3++________;③FeS2+2Fe3+
 3Fe2++2S;
3Fe2++2S;④2S+3O2+2H2O
 4H++2SO
4H++2SO 。
。已知:FeS2中的硫元素为-1价。
回答下列问题:
(1)根据质量守恒定律和电荷守恒定律,将上述②离子方程式配平并补充完整
(2)反应③的还原剂是
(3)观察上述反应,硫元素最终转化为
Ⅱ.在淀粉KI溶液中,滴入少量NaClO溶液,溶液立即变蓝,有关反应的离子方程式是
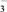 )从以上实验可知,ClO-、I2、IO
)从以上实验可知,ClO-、I2、IO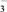 的氧化性由强到弱的顺序是
的氧化性由强到弱的顺序是Ⅲ.工业上用黄铜矿( CuFeS2)冶炼铜,副产品中有SO2,冶炼铜的反应为8CuFeS2+21O2
 8Cu+4FeO+2Fe2O3+16SO2。若CuFeS2中 Fe 的化合价为+2 ,反应中被还原的元素是
8Cu+4FeO+2Fe2O3+16SO2。若CuFeS2中 Fe 的化合价为+2 ,反应中被还原的元素是
您最近一年使用:0次
填空题
|
较难
(0.4)
解题方法
【推荐3】回答下列问题:
(1)同温同压下,当两者体积相等,CO2和N2质量比为_______ ,密度之比为_______ ,分子数之比为_______ 。
(2)某同学写出以下三个化学方程式(未配平):
①NO+HNO3→N2O3+H2O
②N2O4+H2O→HNO3+ HNO2
③NH3+NO→HNO2+H2O 其中你认为一定不可能实现的是_______ (填序号)。
(3)已知下列反应:①Cl2+2NaBr=2NaCl+Br2;②2KI+Br2=2KBr+I2;③Na2S+I2=2NaI+S↓。判断Cl2与Na2S能否反应?_______ (填写离子反应方程式)
(4)智利硝石矿层中含有碘酸钠,可用亚硫酸酸与其反应来制备单质碘。其化学方程式为2NaIO3+5NaHSO3=3NaHSO4+2Na2SO4+I2+H2O
①反应中_______ 元素被氧化,_______ 是氧化剂;
②用单线桥标法出电子转移方向和数目_______ 。
(1)同温同压下,当两者体积相等,CO2和N2质量比为
(2)某同学写出以下三个化学方程式(未配平):
①NO+HNO3→N2O3+H2O
②N2O4+H2O→HNO3+ HNO2
③NH3+NO→HNO2+H2O 其中你认为一定不可能实现的是
(3)已知下列反应:①Cl2+2NaBr=2NaCl+Br2;②2KI+Br2=2KBr+I2;③Na2S+I2=2NaI+S↓。判断Cl2与Na2S能否反应?
(4)智利硝石矿层中含有碘酸钠,可用亚硫酸酸与其反应来制备单质碘。其化学方程式为2NaIO3+5NaHSO3=3NaHSO4+2Na2SO4+I2+H2O
①反应中
②用单线桥标法出电子转移方向和数目
您最近一年使用:0次



