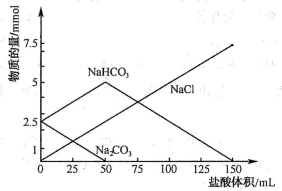
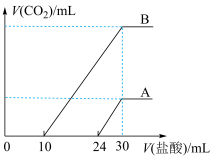
向两份30mL同一浓度的NaOH溶液中通入CO2气体,因CO2通入量的不同,溶液的组成也不同,得到溶液M、N。若向M、N溶液中逐滴加入浓度为0.25mol·L-1盐酸,产生的气体体积v(CO2)与加入盐酸的体积v(HCl)的关系分别为如图所示两种情况A和B。
请回答下列问题:
(1)M溶液中溶质为(写化学式)___________ ,其物质的量之比是__________ 。
(2)N溶液溶质为(写化学式)____________ ,标准状况下CO2气体的体积为________ ,原NaOH溶液的物质的量浓度为_________ 。

请回答下列问题:
(1)M溶液中溶质为(写化学式)
(2)N溶液溶质为(写化学式)
更新时间:2017-12-27 22:31:11
|
相似题推荐
填空题
|
较难
(0.4)
名校
解题方法
【推荐1】取等物质的量浓度的NaOH溶液两份,每份50ml.向其中分别通入一定量的CO2气体,随后各取溶液10ml,并分别加水稀释到100ml.分别向稀溶液后的溶液中逐滴加入0.1mol/L的盐酸,产生CO2气体的体积(标准状况)与所加入的盐酸的体积之间的关系如图(a)(b)所示(已知:向碳酸钠溶液中滴加盐酸时,刚开始滴的过程中,碳酸钠是过量的,Na2CO3+HCl=NaHCO3+NaCl ,随着过程的进行继续加盐酸,当盐酸过量时,生成的NaHCO3会与盐酸反应生成NaCl+H2O+CO2)。回答下列问题:
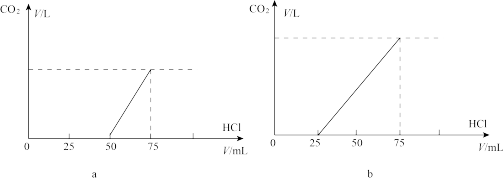
(1)在a情况下,溶质为(写化学式)________ ,其物质的量之比是________ ,标准状况下CO2气体的体积为________ 。
(2)在b情况下,溶质为(写化学式)________ ,标准状况下CO2气体的体积为________ ,原NaOH溶液的物质的量浓度为________ 。

(1)在a情况下,溶质为(写化学式)
(2)在b情况下,溶质为(写化学式)
您最近半年使用:0次
填空题
|
较难
(0.4)
名校
【推荐2】I.(1)粗盐中含有Ca2+、Mg2+、SO42-等杂质离子,粗盐精制过程中要使用Na2CO3溶液,请写出加入Na2CO3溶液后相关化学反应的离子方程式:_________________________ 。
(2)将足量CO2气体通入水玻璃(Na2SiO3溶液)中,然后加热蒸干,再在高温下充分灼烧,最后得到的固体物质是_________________________ 。
II.(1)120 mL含有0.20 mol碳酸钠的溶液和200 mL盐酸,不管将前者滴加入后者,还是将后者滴加入前者,都有气体产生,但最终生成的气体体积不同,则盐酸的浓度合理的范围是_________________________________________
(2)取体积相同的KI、Na2SO3、FeBr2溶液,分别通入足量氯气,当恰好完全反应时,三种溶液消耗氯气的物质的量相同,则KI、Na2SO3、FeBr2溶液的物质的量浓度之比为_______ 。
(3)在反应 3BrF3+5H2O=HBrO3+Br2+9HF+O2 中,当有5 mol水反应时,由H2O还原的BrF3为______________ mol。
III.将一定质量的铁粉加入到装有100 mL某浓度的稀硝酸溶液中充分反应。
(1)容器中剩有m g的铁粉,收集到NO气体448 mL(标准状况下)。
①所得溶液中的溶质的化学式为________________ 。
②原硝酸溶液的物质的量浓度为__________________________ 。
(2)向上述固液混合物中逐渐滴加稀硫酸至刚好不再产生遇空气变成红棕色气体为止,此时容器中有铁粉n g。
①此时溶液中溶质的化学式为__________________ 。
②(m-n)的值为________________ (精确到0.1 g)。
(2)将足量CO2气体通入水玻璃(Na2SiO3溶液)中,然后加热蒸干,再在高温下充分灼烧,最后得到的固体物质是
II.(1)120 mL含有0.20 mol碳酸钠的溶液和200 mL盐酸,不管将前者滴加入后者,还是将后者滴加入前者,都有气体产生,但最终生成的气体体积不同,则盐酸的浓度合理的范围是
(2)取体积相同的KI、Na2SO3、FeBr2溶液,分别通入足量氯气,当恰好完全反应时,三种溶液消耗氯气的物质的量相同,则KI、Na2SO3、FeBr2溶液的物质的量浓度之比为
(3)在反应 3BrF3+5H2O=HBrO3+Br2+9HF+O2 中,当有5 mol水反应时,由H2O还原的BrF3为
III.将一定质量的铁粉加入到装有100 mL某浓度的稀硝酸溶液中充分反应。
(1)容器中剩有m g的铁粉,收集到NO气体448 mL(标准状况下)。
①所得溶液中的溶质的化学式为
②原硝酸溶液的物质的量浓度为
(2)向上述固液混合物中逐渐滴加稀硫酸至刚好不再产生遇空气变成红棕色气体为止,此时容器中有铁粉n g。
①此时溶液中溶质的化学式为
②(m-n)的值为
您最近半年使用:0次
填空题
|
较难
(0.4)
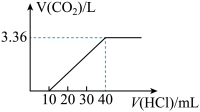
【推荐1】取一定质量NaHCO3和Na2O的固体混合物溶于适量的水,向所得溶液中缓慢逐滴加入某物质的量浓度的盐酸,产生的气体体积与所加盐酸体积之间的关系如图所示。试回答下列问题:

(1)盐酸的物质的量浓度为_____ 。
(2)固体混合物中NaHCO3与Na2O物质的量之比_____ 。

(1)盐酸的物质的量浓度为
(2)固体混合物中NaHCO3与Na2O物质的量之比
您最近半年使用:0次
填空题
|
较难
(0.4)
名校
【推荐2】向100 mL NaOH溶液中通入一定量的CO2气体,充分反应后,再向所得溶液中逐滴加入0.2 mol/L的盐酸,产生CO2的体积与所加盐酸体积之间关系如图所示。

(1)A-B段的离子反应方程式为__________________________ 。
(2)原NaOH溶液的浓度为__________ mol/L。
(3)通入CO2在标准状况下的体积为_______ mL。
(4)所得溶液的溶质成分是_______________ ,其物质的量之比为_________ 。

(1)A-B段的离子反应方程式为
(2)原NaOH溶液的浓度为
(3)通入CO2在标准状况下的体积为
(4)所得溶液的溶质成分是
您最近半年使用:0次
填空题
|
较难
(0.4)
名校
【推荐1】碳酸亚铁(白色固体,难溶于水)是一种重要的工业原料,可用于制备补血剂乳酸亚铁,也可用作可充电电池的电极。某研究小组通过下列实验,寻找利用复分解反应制备FeCO3的最佳方案:
(1)实验I中红褐色沉淀产生的原因可用如下反应表示,请补全反应:_____________
 Fe2++
Fe2++  +
+  +
+  H2O
H2O 
 Fe(OH)3 +
Fe(OH)3 +  HCO3−
HCO3−
(2)实验II中产生FeCO3的离子方程式为__________________ 。
(3)为了探究实验III中NH4+所起的作用,甲同学设计了实验IV进行探究:
实验IV中加入Na2SO4固体的目的是_________ 。
对比实验II、III、IV,甲同学得出结论:NH4+水解产生H+,降低溶液pH,减少了副产物Fe(OH)2的产生。
乙同学认为该实验方案不够严谨,应补充的对比实验操作是:_________ ,再取该溶液一滴管,与2mL 1mol/L NaHCO3溶液混合。
(4)小组同学进一步讨论认为,定性实验现象并不能直接证明实验III中FeCO3的纯度最高,需要利用如图所示的装置进行定量测定。分别将实验I、II、III中的沉淀进行过滤、洗涤、干燥后称量,然后转移至A处的广口瓶中。

① 补全A中装置并标明所用试剂。____________
② 为测定FeCO3的纯度,除样品总质量外,还需测定的物理量是____________ 。
(5)实验反思:经测定,实验III中的FeCO3纯度高于实验I和实验II。通过以上实验分析,制备FeCO3实验成功的关键因素是____________ 。
| 实验 | 试剂 | 现象 | |
| 滴管 | 试管 | ||
 | 0.8 mol/L FeSO4溶液 (pH=4.5) | 1 mol/L Na2CO3溶液 (pH=11.9) | 实验Ⅰ:立即产生灰绿色沉淀,5min后出现明显的红褐色 |
| 0.8 mol/L FeSO4溶液 (pH=4.5) | 1 mol/L NaHCO3溶液 (pH=8.6) | 实验Ⅱ:产生白色沉淀及少量无色气泡,2min后出现明显的灰绿色 | |
| 0.8 mol/L (NH4)2Fe(SO4)2 溶液(pH=4.0) | 1 mol/L NaHCO3溶液 (pH=8.6) | 实验Ⅲ:产生白色沉淀及无色气泡,较长时间保持白色 | |
(1)实验I中红褐色沉淀产生的原因可用如下反应表示,请补全反应:
 Fe2++
Fe2++  +
+  +
+  H2O
H2O 
 Fe(OH)3 +
Fe(OH)3 +  HCO3−
HCO3−(2)实验II中产生FeCO3的离子方程式为
(3)为了探究实验III中NH4+所起的作用,甲同学设计了实验IV进行探究:
| 操作 | 现象 | |
| 实验IV | 向0.8 mol/L FeSO4溶液中加入 | 与实验III现象相同 |
实验IV中加入Na2SO4固体的目的是
对比实验II、III、IV,甲同学得出结论:NH4+水解产生H+,降低溶液pH,减少了副产物Fe(OH)2的产生。
乙同学认为该实验方案不够严谨,应补充的对比实验操作是:
(4)小组同学进一步讨论认为,定性实验现象并不能直接证明实验III中FeCO3的纯度最高,需要利用如图所示的装置进行定量测定。分别将实验I、II、III中的沉淀进行过滤、洗涤、干燥后称量,然后转移至A处的广口瓶中。

① 补全A中装置并标明所用试剂。
② 为测定FeCO3的纯度,除样品总质量外,还需测定的物理量是
(5)实验反思:经测定,实验III中的FeCO3纯度高于实验I和实验II。通过以上实验分析,制备FeCO3实验成功的关键因素是
您最近半年使用:0次
填空题
|
较难
(0.4)
【推荐2】我国将力争2060年前实现碳中和,CO2的捕捉是减少碳排放的措施之一。
(1)一种利用NaOH溶液捕捉回收CO2的过程如图所示。
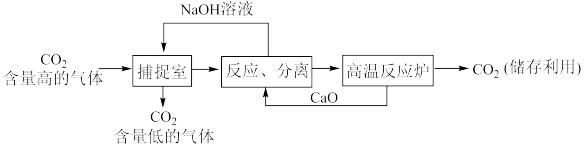
①捕捉室中NaOH溶液常喷成雾状,优点是___________ 。
②整个过程中可以循环利用的物质是___________ 。
(2)实验室模拟捕捉回收CO2,配制500mL1.000mol·L-1NaOH溶液。
①配制溶液需要的玻璃仪器是烧杯、玻璃棒和___________ 。根据计算用天平称量NaOH固体___________ g。
②在容量瓶的使用方法中,下列操作正确的是___________ 。
A.使用容量瓶前检验是否漏水
B.容量瓶用蒸馏水洗净,必须干燥后再配制溶液
C.配制溶液时,如果试样是固体,把称好的固体用纸条小心倒入容量瓶中,缓慢加水至接近刻度线1-2cm处,用胶头滴管加蒸馏水至刻度线。
D.配制溶液时,若试样是液体,用量筒取样后用玻璃棒引流倒入容量瓶中,缓慢加水至刻度线1-2cm处,用胶头滴管加蒸馏水至刻度线。
E.盖好瓶塞,用食指顶住瓶塞,另一只手托住瓶底,把容量瓶反复倒转多次,摇匀。
③配制过程中,定容时俯视刻度线,会造成所配制NaOH溶液的物质的量浓度___________ 。(偏小、不变、偏大)
(3)CaO固体也可以捕捉回收CO2.研究表明CaC2O4·H2O热分解制得的CaO疏松多孔,具有良好的CO2捕捉性能。取1.46gCaC2O4·H2O进行加热,固体质量随温度变化如图所示。
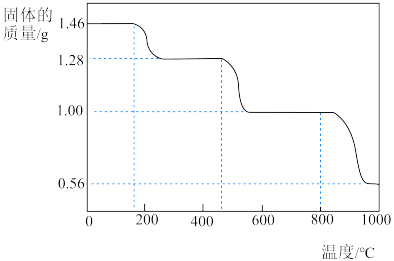
①写出400~600℃范围内分解反应的化学方程式:___________ (CaC2O4·H2O的相对分子质量:146)。
②据图分析,CaO捕捉CO2的反应温度应___________ (填“高于”或“低于”)800℃。
(1)一种利用NaOH溶液捕捉回收CO2的过程如图所示。

①捕捉室中NaOH溶液常喷成雾状,优点是
②整个过程中可以循环利用的物质是
(2)实验室模拟捕捉回收CO2,配制500mL1.000mol·L-1NaOH溶液。
①配制溶液需要的玻璃仪器是烧杯、玻璃棒和
②在容量瓶的使用方法中,下列操作正确的是
A.使用容量瓶前检验是否漏水
B.容量瓶用蒸馏水洗净,必须干燥后再配制溶液
C.配制溶液时,如果试样是固体,把称好的固体用纸条小心倒入容量瓶中,缓慢加水至接近刻度线1-2cm处,用胶头滴管加蒸馏水至刻度线。
D.配制溶液时,若试样是液体,用量筒取样后用玻璃棒引流倒入容量瓶中,缓慢加水至刻度线1-2cm处,用胶头滴管加蒸馏水至刻度线。
E.盖好瓶塞,用食指顶住瓶塞,另一只手托住瓶底,把容量瓶反复倒转多次,摇匀。
③配制过程中,定容时俯视刻度线,会造成所配制NaOH溶液的物质的量浓度
(3)CaO固体也可以捕捉回收CO2.研究表明CaC2O4·H2O热分解制得的CaO疏松多孔,具有良好的CO2捕捉性能。取1.46gCaC2O4·H2O进行加热,固体质量随温度变化如图所示。

①写出400~600℃范围内分解反应的化学方程式:
②据图分析,CaO捕捉CO2的反应温度应
您最近半年使用:0次
填空题
|
较难
(0.4)
【推荐3】铁是应用最广泛的金属,铁的卤化物也是一种重要化合物。
(1)在实验室中,FeCl2可用铁粉和___________ 反应制取,FeCl3可用铁粉和___________ 反应制取。现有含FeCl2和FeCl3的混合物样品,测得n(Fe):n(Cl)=1:2.4,则该样品中FeCl3的物质的量分数为________________ 。
(2)FeCl2易被氧化,检验一瓶FeCl2溶液是否被氧化的方法(写出操作步骤、现象及结论)是______________ 。向FeCl2溶液中加入NaOH溶液,开始时生成白色沉淀,后马上变成灰绿色,最终变成红褐色,沉淀变色发生反应的化学方程式为_________________ 。
(1)在实验室中,FeCl2可用铁粉和
(2)FeCl2易被氧化,检验一瓶FeCl2溶液是否被氧化的方法(写出操作步骤、现象及结论)是
您最近半年使用:0次
填空题
|
较难
(0.4)
【推荐1】过氧化钠与铝粉混合物18.3g,加入100mL水,充分反应后混合物完全溶解,并收集到5.6L气体(标准状况)。
(1)写出铝粉参加反应的离子方程式_______________ 。
(2)收集到的气体成分是________________ ,体积比是_______________ 。反应后溶液中NaAlO2的物质的量浓度是(设溶液体积不变)_________________________ 。
(1)写出铝粉参加反应的离子方程式
(2)收集到的气体成分是
您最近半年使用:0次
填空题
|
较难
(0.4)
解题方法
【推荐2】草酸亚铁晶体(FeC2O4·2H2O)常用做分析试剂及显影剂等。下图是将一定质量的草酸亚铁在氩气气氛中进行热重分析示意图(TG%表示残留固体质量占原样品总质量的百分数)。

请回答下列问题:
(l)B处时残留物的化学式为___________ 。
(2)A→C整个反应过程中总反应的化学方程式为___________ 。
(3)取上述分解得到的600℃时的固体放在空气中继续加热时其质量增加,发生反应的化学方程式为___________ 。由此说明上述FeC2O4·2H2O在氩气气氛中进行热重分析的原因是___________ 。
(4)若将分解得到的600℃时的固体与足量的稀硫酸反应后,将溶液浓缩、冷却,有带7个结晶水的晶体析出,该晶体的化学式为__________ ,该晶体与草酸亚铁晶体分解有类似,得到四种氧化物且物质的量之比为1:1:1:14,则该化学方程式为__________ 。

请回答下列问题:
(l)B处时残留物的化学式为
(2)A→C整个反应过程中总反应的化学方程式为
(3)取上述分解得到的600℃时的固体放在空气中继续加热时其质量增加,发生反应的化学方程式为
(4)若将分解得到的600℃时的固体与足量的稀硫酸反应后,将溶液浓缩、冷却,有带7个结晶水的晶体析出,该晶体的化学式为
您最近半年使用:0次
填空题
|
较难
(0.4)
解题方法
【推荐3】Ⅰ.固体化合物X由三种元素组成,是具有良好前景的储氢材料,为了研究它的组成与性质,设计并完成了如下实验。X的焰色反应为砖红色,溶液B中只有一种溶质,沉淀D可溶于NaOH溶液。
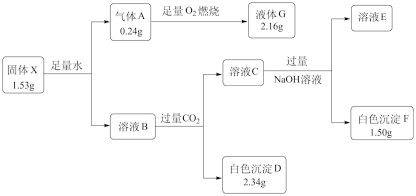
(1)X所含的三种元素为H、____ 、____ ,X化学式为______ 。
(2)溶液C与足量NaOH溶液反应的离子方程式为____ 。
II.利用图实验装置制取氯酸钾和饱和氯水。
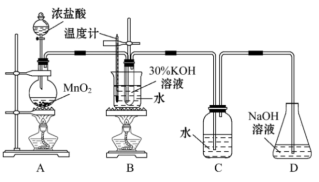
(3)装置D的作用____ 。
(4)请写出装置B中发生反应的化学方程式____ 。
(5)取少量C中溶液滴加到含有酚酞的NaOH溶液中,发现溶液褪色,该现象不能说明C中溶液具有漂白性的原因是____ 。

(1)X所含的三种元素为H、
(2)溶液C与足量NaOH溶液反应的离子方程式为
II.利用图实验装置制取氯酸钾和饱和氯水。

(3)装置D的作用
(4)请写出装置B中发生反应的化学方程式
(5)取少量C中溶液滴加到含有酚酞的NaOH溶液中,发现溶液褪色,该现象不能说明C中溶液具有漂白性的原因是
您最近半年使用:0次