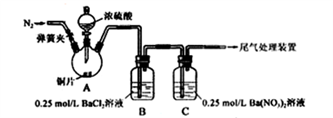
甲、乙两同学为探究SO2与可溶性钡的强酸盐能否反应生成白色BaSO3沉淀,用下图所示装置进行实验(夹持装置和A中加热装置已略,气密性已检验)。
实验操作和现象:
(1)A中反应的化学方程式是_________________ ;
(2)C中生成白色沉淀的离子方程式为__________________ ;
(3)分析B中不溶于稀盐酸的沉淀产生的原因,甲认为是空气参与反应,乙认为是白雾参与反应。为证实各自的观点,在原实验基础上,甲、乙两同学分别作了如下实验:甲在原有操作之前通N2,一段时间,B中产生大量白色沉淀。乙在A、B间增加盛放饱和NaHSO3溶液的洗气瓶,B中有少量白色沉淀。产生少量沉淀的原因是_____________ 。
(4)结合(3)中两同学的实验现象。你认为原实验B中产生大量白色沉淀的主要原因是_____________ 。

实验操作和现象:
| 操作 | 现象 |
| 关闭弹簧夹,滴加一定量浓硫酸,加热 | A中有白雾生成,铜片表面产生气泡 B中有气泡冒出,产生大量白色沉淀 C中产生白色沉淀,液面上方略显浅棕色并逐渐消失 |
| 打开弹簧夹,通入N2,停止加热,一段时间后关闭 | |
| 从B、C中分别取少量白色沉淀,加稀盐酸 | 均未发现白色沉淀溶解 |
(2)C中生成白色沉淀的离子方程式为
(3)分析B中不溶于稀盐酸的沉淀产生的原因,甲认为是空气参与反应,乙认为是白雾参与反应。为证实各自的观点,在原实验基础上,甲、乙两同学分别作了如下实验:甲在原有操作之前通N2,一段时间,B中产生大量白色沉淀。乙在A、B间增加盛放饱和NaHSO3溶液的洗气瓶,B中有少量白色沉淀。产生少量沉淀的原因是
(4)结合(3)中两同学的实验现象。你认为原实验B中产生大量白色沉淀的主要原因是
2017·内蒙古呼和浩特·一模 查看更多[2]
更新时间:2017/12/04 20:12:57
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
【推荐1】物质类别与元素化合价是研究物质性质的两个视角,图1是硫元素及其化合物的“价类二维图”。
Ⅰ.根据要求回答下列问题:


(1)写出图中A化学式___________ 。
(2)SO2属于___________ (填“酸性”或“碱性”)氧化物,可与CaO、Ca(OH)2等反应,Ca(OH)2的电子式___________ 。请写出用石灰石除去燃煤产生的SO2并生成CaSO4的化学方程式___________ 。
(3)某同学预测SO2具有还原性,其理论依据是___________ ,将SO2通入酸性高锰酸钾溶液中,下列实验事实能够证实SO2具有还原性的是___________ (填序号)。
①反应后溶液由紫色变为无色
②取反应后的溶液少许,加入BaCl2溶液,产生白色沉淀
③取反应后的溶液少许,加入Ba(NO3)2溶液,产生白色沉淀。
Ⅱ.探究SO2的性质
如图2先后四次加入同浓度同体积不同情况的钡盐溶液,控制食用油油层厚度一致、通入SO2流速一致。四次实验分别得到如表pH-t图:
(4)装置中覆盖食用油的目的是___________ 。
(5)分析pH-图,写出③中发生反应的离子方程式___________ ,上述四次实验中有白色沉淀生成的是___________ (填编号)。
Ⅰ.根据要求回答下列问题:


(1)写出图中A化学式
(2)SO2属于
(3)某同学预测SO2具有还原性,其理论依据是
①反应后溶液由紫色变为无色
②取反应后的溶液少许,加入BaCl2溶液,产生白色沉淀
③取反应后的溶液少许,加入Ba(NO3)2溶液,产生白色沉淀。
Ⅱ.探究SO2的性质
如图2先后四次加入同浓度同体积不同情况的钡盐溶液,控制食用油油层厚度一致、通入SO2流速一致。四次实验分别得到如表pH-t图:
| ① | ② | ③ | ④ |
| 已煮沸的BaCl2(aq) | 未煮沸的BaCl2(aq)| | 已煮沸的Ba(NO3)2(aq) | 未煮沸的Ba(NO3)2(aq) |
 |  |  |  |
(5)分析pH-图,写出③中发生反应的离子方程式
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐2】元素周期表是学习化学的重要工具。A-H为短周期主族元素,其原子半径→原子序数→最高正化合价(或最低负化合价)的关系如图所示。

回答下列问题:
(1)F原子的结构示意图为___________ ,写出质量数为35的H原子符号:___________ 。
(2)B、D形成的化合物BD2的电子式为___________ ,结构式为___________ 。
(3)A与H形成的化合物属于___________ (填“离子”或“共价”)化合物;元素B、G、H的最高价氧化物的水化物中,酸性由大到小的是___________ (用“>”连接化学式)。
(4)D、E的简单离子半径由大到小顺序为___________ (填离子符号)。
(5)元素G的简单气态氢化物与GD2的水溶液反应的实验现象为___________ 。
(6)单质F与E的最高价氧化物对应的水化物之间发生反应的离子方程式为___________ 。

回答下列问题:
(1)F原子的结构示意图为
(2)B、D形成的化合物BD2的电子式为
(3)A与H形成的化合物属于
(4)D、E的简单离子半径由大到小顺序为
(5)元素G的简单气态氢化物与GD2的水溶液反应的实验现象为
(6)单质F与E的最高价氧化物对应的水化物之间发生反应的离子方程式为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】硫酸亚铁在印染、医药、化肥等多个行业有广泛应用。已知: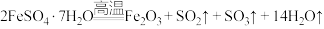 。某学习小组对硫酸亚铁晶体(
。某学习小组对硫酸亚铁晶体( )的热分解产物进行探究。回答下列问题:
)的热分解产物进行探究。回答下列问题:
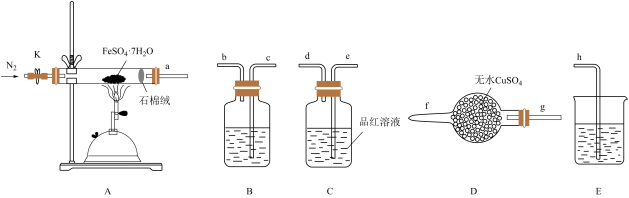
(1)装置A中石棉绒的作用为_______ 。
(2)按气流方向,上述装置合理的连接顺序为a→g、f→_______、_______→_______、_______→h(填装置口小写字母)。_______
(3)该小组同学按上述顺序连接各装置并进行实验,请为他们补全表格:
(4)设计实验证明A中得到的红色粉末不含+2价铁元素:_______ (简述实验操作及现象)。
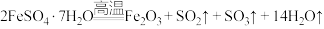 。某学习小组对硫酸亚铁晶体(
。某学习小组对硫酸亚铁晶体( )的热分解产物进行探究。回答下列问题:
)的热分解产物进行探究。回答下列问题:
(1)装置A中石棉绒的作用为
(2)按气流方向,上述装置合理的连接顺序为a→g、f→_______、_______→_______、_______→h(填装置口小写字母)。
(3)该小组同学按上述顺序连接各装置并进行实验,请为他们补全表格:
| 装置编号 | 填装试剂 | 实验现象 | 实验结论 |
| A |  | 绿色固体逐渐变为红色粉末 | |
| B | ① | ② | 分解产物中含有 |
| C | 品红溶液 | 溶液由红色褪为无色 | ③ |
| D | 无水 粉末 粉末 | 白色固体逐渐变为蓝色 | 分解产物中含有水蒸气 |
| E | NaOH溶液 |
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
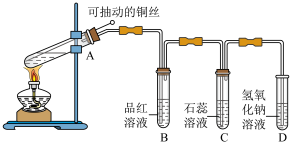
【推荐1】某同学用如图所示的装置进行铜与浓硫酸反应的实验。
(1)铜与浓硫酸反应的化学方程式是___________ 。
(2)实验过程中,观察到品红溶液褪色,石蕊溶液_________ (填现象),说明SO2________ (填选项)。
a.有氧化性 b.有还原性 c.有漂白性 d.水溶液显酸性
(3)为进一步确认产生的气体是二氧化硫气体,还应补充的操作是___________ 。
(4)结合离子方程式 说明试管D中氢氧化钠溶液的作用是___________ 。
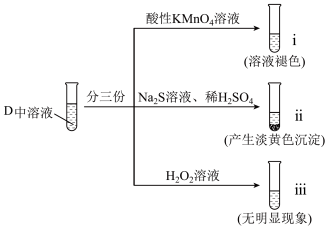
(5)反应结束后取D中溶液进行以下实验:___________ 性。
②ⅱ中产生淡黄色沉淀的离子方程式为___________ 。
③ⅲ中无明显现象,甲同学通过检测 的生成证明Na2SO3和H2O2发生反应:取1 mL ⅲ中溶液于试管中,
的生成证明Na2SO3和H2O2发生反应:取1 mL ⅲ中溶液于试管中,___________ (填试剂和操作),产生白色沉淀。
乙同学认为甲同学的实验没有排除O2的影响,设计对比实验:___________ 。
综合甲、乙同学的实验可知,H2O2能将Na2SO3氧化。
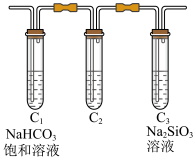
(6)将装置C替换为下图所示装置,并用来比较碳和硅的非金属性。
已知:①酸性:H2SO3>H2CO3。
②硅酸为玻璃状无色透明的无定形颗粒,难溶于水和醇。___________ ,其作用是___________ 。
②能说明碳的非金属性比硅强的实验现象是___________ 。
(1)铜与浓硫酸反应的化学方程式是
(2)实验过程中,观察到品红溶液褪色,石蕊溶液
a.有氧化性 b.有还原性 c.有漂白性 d.水溶液显酸性
(3)为进一步确认产生的气体是二氧化硫气体,还应补充的操作是
(4)
(5)反应结束后取D中溶液进行以下实验:
②ⅱ中产生淡黄色沉淀的离子方程式为
③ⅲ中无明显现象,甲同学通过检测
 的生成证明Na2SO3和H2O2发生反应:取1 mL ⅲ中溶液于试管中,
的生成证明Na2SO3和H2O2发生反应:取1 mL ⅲ中溶液于试管中,乙同学认为甲同学的实验没有排除O2的影响,设计对比实验:
综合甲、乙同学的实验可知,H2O2能将Na2SO3氧化。
(6)将装置C替换为下图所示装置,并用来比较碳和硅的非金属性。
已知:①酸性:H2SO3>H2CO3。
②硅酸为玻璃状无色透明的无定形颗粒,难溶于水和醇。
②能说明碳的非金属性比硅强的实验现象是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】某研究小组在实验室进行硫的化合物系列实验。
Ⅰ.验证H2SO3的酸性比H2CO3强,甲同学设计下图装置。________ 。
(2)当观察到________ ,即证明H2SO3的酸性比H2CO3强。
Ⅱ.研究铁与硫酸的反应。
已知:浓H2SO4的沸点为338.2℃。
a.乙同学设计如下表所示的实验1、2:
(3)上述实验中,铁丝绕成螺旋状的目的是________ 。
(4)实验1中,铁与稀硫酸反应的离子方程式为________ 。
(5)实验2中的现象常被称为________ 。
b.丙同学设计如图所示装置的实验3:
加热试管A,温度保持在250℃~300℃,产生大量气体,B中品红褪色,D处始终未检测到可燃性气体,实验结束后,检验到A的溶液中既有Fe3+又有Fe2+。________ ;检测装置A的溶液中含有Fe3+的试剂是_______ 。
(7)分析实验1、2、3,可知影响铁和硫酸反应产物多样性的因素有________ 。
Ⅰ.验证H2SO3的酸性比H2CO3强,甲同学设计下图装置。
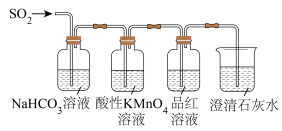
(2)当观察到
Ⅱ.研究铁与硫酸的反应。
已知:浓H2SO4的沸点为338.2℃。
a.乙同学设计如下表所示的实验1、2:
| 实验 | 试剂 | 现象 | |
| 1 | 螺旋状铁丝、稀硫酸 | 铁丝表面有大量气体产生。 |
| 2 | 螺旋状铁丝、浓硫酸 | 铁丝表面迅速发黑(Fe3O4),有少量气体产生,反应很快停止。 | |
(3)上述实验中,铁丝绕成螺旋状的目的是
(4)实验1中,铁与稀硫酸反应的离子方程式为
(5)实验2中的现象常被称为
b.丙同学设计如图所示装置的实验3:
加热试管A,温度保持在250℃~300℃,产生大量气体,B中品红褪色,D处始终未检测到可燃性气体,实验结束后,检验到A的溶液中既有Fe3+又有Fe2+。
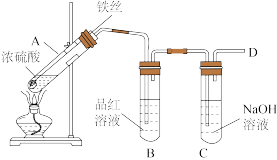
(7)分析实验1、2、3,可知影响铁和硫酸反应产物多样性的因素有
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】以Al和不同的铜盐溶液间的反应为实验对象,探索Al与不同铜盐溶液反应的多样性。
(1)对实验Ⅰ进行研究②④
①实验Ⅰ中生成红色物质的离子方程式为:____________________________
经检验实验Ⅰ中产生的气体为氢气,用离子方程式解释溶液中存在H+的原因:_____________________
③请写出60s后反应进一步加快可能的原因(写出两条)_____________________________
(2)对实验Ⅱ进行研究
实验Ⅱ反应明显比实验Ⅰ缓慢,说明Al与不同的铜盐溶液反应呈现多样性,其原因可能有:
假设一:SO42-对Al与Cu2+的置换反应存在一定的抑制作用。
假设二:________________________
(3)为进一步研究上述假设,设计如下实验:
_____________________________________
其中,实验Ⅰ与实验Ⅲ、Ⅳ做对比,结论为:______________________________________
其中,实验Ⅱ与实验Ⅴ、Ⅵ做对比,结论为:______________________________________
(4)请设计实验证明Cl-对Al与H+的反应同样起到相似的作用:_________________
实验 | 向试管中加入2ml溶液 | 实验现象 |
| 实验Ⅰ:0.5mol/LCuCl2溶液 | 15s:大量气泡且有红色物质析出 60s:反应进一步加快且反应剧烈放热,液体几乎沸腾 120s:铝片反应完,试管中析出大量蓬松的红色物质 |
| 实验Ⅱ:0.5mol/LCuSO4溶液 | 15s 无明显现象 60s:铝片表面有极少气泡 120s:有少量气泡溢出,铝片边缘有很少红色物质生成 |
(1)对实验Ⅰ进行研究②④
①实验Ⅰ中生成红色物质的离子方程式为:
经检验实验Ⅰ中产生的气体为氢气,用离子方程式解释溶液中存在H+的原因:
③请写出60s后反应进一步加快可能的原因(写出两条)
(2)对实验Ⅱ进行研究
实验Ⅱ反应明显比实验Ⅰ缓慢,说明Al与不同的铜盐溶液反应呈现多样性,其原因可能有:
假设一:SO42-对Al与Cu2+的置换反应存在一定的抑制作用。
假设二:
(3)为进一步研究上述假设,设计如下实验:
实验 | 向试管中加入2mL溶液 | 实验现象 |
| 实验Ⅲ:0.5mol/LCuCl2溶液+1g Na2SO4固体 | 加入 Na2SO4固体后速率几乎不变,仍有大量气泡产生,红色物质生成且剧烈放热,铝片反应完全,溶液沸腾 |
| 实验Ⅳ:0.5mol/L CuCl2溶液+5g Na2SO4固体 | 加入Na2SO4固体后速率几乎不变,仍有大量气泡产生,红色物质生成且剧烈放热,铝片反应完全,溶液沸腾 | |
| 实验Ⅴ:0.5mol/LCuSO4溶液+0.02mol NaCl固体 | 未加入 NaCl固体前几乎没现象,加入后,铝片表面迅速产生大量气体和红色物质,溶液温度上升至沸腾,铝反应完全 | |
| 实验Ⅵ:0.5mol/LCuSO4溶液+ | 未加入 NH4Cl固体前几乎没现象,加入后,铝片表面迅速产生大量气体和红色物质,溶液温度上升至沸腾,铝反应完全 |
其中,实验Ⅰ与实验Ⅲ、Ⅳ做对比,结论为:
其中,实验Ⅱ与实验Ⅴ、Ⅵ做对比,结论为:
(4)请设计实验证明Cl-对Al与H+的反应同样起到相似的作用:
您最近一年使用:0次