为了防止枪支生锈,常将枪支的钢铁零件放在NaNO2和NaOH的混合液中进行化学处理使钢铁零件表面生成Fe3O4的致密的保护层——“发蓝”。其过程可用下列化学方程式表示:
①3Fe+NaNO2+5NaOH=3Na2FeO2+H2O+NH3↑
②Na2FeO2+□NaNO2+□H2O →□Na2Fe2O4+□NH3↑+□NaOH
③Na2FeO2+Na2Fe2O4+2H2O=Fe3O4+4NaOH
请回答下列问题
(1)配平化学方程式②,各物质前的化学计量数依次为___________________ 。
(2)上述反应①中还原剂为_______ ,被还原的是________ 。若有1mol Na2FeO2生成,则反应①中有 ________ mol电子转移。
(3)关于形成“发蓝”的过程,下列说法正确的是_________ (填字母)。
A.该过程不会产生污染 B.反应③生成的四氧化三铁具有抗腐蚀作用
C.反应①②③均是氧化还原反应 D.反应①②中的氧化剂均为NaNO2
①3Fe+NaNO2+5NaOH=3Na2FeO2+H2O+NH3↑
②Na2FeO2+□NaNO2+□H2O →□Na2Fe2O4+□NH3↑+□NaOH
③Na2FeO2+Na2Fe2O4+2H2O=Fe3O4+4NaOH
请回答下列问题
(1)配平化学方程式②,各物质前的化学计量数依次为
(2)上述反应①中还原剂为
(3)关于形成“发蓝”的过程,下列说法正确的是
A.该过程不会产生污染 B.反应③生成的四氧化三铁具有抗腐蚀作用
C.反应①②③均是氧化还原反应 D.反应①②中的氧化剂均为NaNO2
更新时间:2018-01-09 07:48:58
|
相似题推荐
填空题
|
适中
(0.65)
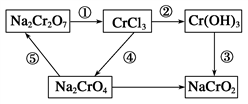
【推荐1】(1)化学实验中,如使某步中的有害产物作为另一步的反应物,形成一个循环,就可不再向环境排放该种有害物质。例如:在如图有编号的步骤中,发生氧化反应的是_________ (填编号,下同),发生还原反应的是___________ 。(提示:铬元素化合价有+6、+3价)
(2)饮用水中的NO3-对人类健康会产生危害,为了降低饮用水中NO3-的浓度,某饮用水研究人员提出,在碱性条件下用铝粉将NO3-还原为N2,其化学方程式为:10A1+6NaNO3+4NaOH==10NaA1O2+3N2↑+2H2O。请回答下列问题:
①其中被还原的元素是________ ,氧化剂是__________ ,还原剂是_________ ,氧化产物是__________ ,还原产物是__________ 。
②表示反应中电子转移的方向和数目:__________ 。
10 A1 + 6 NaNO3 + 4 NaOH == 10 NaA1O2 + 3 N2↑ + 2 H2O
(3)一个完整的氧化还原反应方程式可以拆开写成两个“半反应式”,一个是“氧化反应”式,一个是“还原反应”式。如2Fe3++Cu═2Fe2++Cu2+的拆写结果是:氧化反应为:Cu-2e-═Cu2+;还原反应为:2Fe3++2e-═2Fe2+。
请据此将反应:Fe+2H+===Fe2++H2↑拆写成两个“半反应式”:氧化反应为____________________ ;还原反应为____________________ 。

(2)饮用水中的NO3-对人类健康会产生危害,为了降低饮用水中NO3-的浓度,某饮用水研究人员提出,在碱性条件下用铝粉将NO3-还原为N2,其化学方程式为:10A1+6NaNO3+4NaOH==10NaA1O2+3N2↑+2H2O。请回答下列问题:
①其中被还原的元素是
②表示反应中电子转移的方向和数目:
10 A1 + 6 NaNO3 + 4 NaOH == 10 NaA1O2 + 3 N2↑ + 2 H2O
(3)一个完整的氧化还原反应方程式可以拆开写成两个“半反应式”,一个是“氧化反应”式,一个是“还原反应”式。如2Fe3++Cu═2Fe2++Cu2+的拆写结果是:氧化反应为:Cu-2e-═Cu2+;还原反应为:2Fe3++2e-═2Fe2+。
请据此将反应:Fe+2H+===Fe2++H2↑拆写成两个“半反应式”:氧化反应为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】根据所学知识回答下列问题:
(1)黄铁矿(主要成分为 ,其中Fe为+2价)的燃烧是工业上制硫酸时得到
,其中Fe为+2价)的燃烧是工业上制硫酸时得到 的途径之一,其反应为
的途径之一,其反应为 。
。
① 中硫元素的化合价为
中硫元素的化合价为___________ 价,该化合物中
___________ 。
②该反应中氧化剂与还原剂的质量之比为___________ 。
③该反应的氧化产物为___________ (填化学式)。
(2)次磷酸( )是一种精细的磷化工产品,具有较强的还原性,
)是一种精细的磷化工产品,具有较强的还原性, 可与溶液中的
可与溶液中的 发生反应,生成物为Ag和
发生反应,生成物为Ag和 ,从而可用于化学镀银。
,从而可用于化学镀银。
已知: 和
和 在溶液中均以分子的形成存在。
在溶液中均以分子的形成存在。
① 的相对分子质量为
的相对分子质量为___________ ,该分子中的磷原子和氧原子的个数之比为___________ 。
②该反应中 体现了
体现了___________ (填“还原”或“氧化”)性。
③该反应的离子方程式为___________ 。
(1)黄铁矿(主要成分为
 ,其中Fe为+2价)的燃烧是工业上制硫酸时得到
,其中Fe为+2价)的燃烧是工业上制硫酸时得到 的途径之一,其反应为
的途径之一,其反应为 。
。①
 中硫元素的化合价为
中硫元素的化合价为
②该反应中氧化剂与还原剂的质量之比为
③该反应的氧化产物为
(2)次磷酸(
 )是一种精细的磷化工产品,具有较强的还原性,
)是一种精细的磷化工产品,具有较强的还原性, 可与溶液中的
可与溶液中的 发生反应,生成物为Ag和
发生反应,生成物为Ag和 ,从而可用于化学镀银。
,从而可用于化学镀银。已知:
 和
和 在溶液中均以分子的形成存在。
在溶液中均以分子的形成存在。①
 的相对分子质量为
的相对分子质量为②该反应中
 体现了
体现了③该反应的离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.64)
【推荐3】工业电解饱和食盐水模拟装置的结构如图所示:
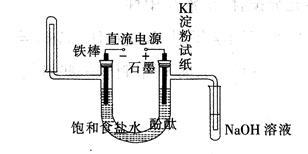
(1)写出电解饱和食盐水的化学方程式_____________________ ,该工业称为工业_____________________
(2)实际生产中使用的盐往往含有一些杂质,在电解食盐水之前,需要提纯食盐水。为了除去粗盐中的Ca2+、Mg2+、SO42-及泥沙,可将粗盐溶于水,然后进行下列五项操作,正确的操作顺序是_____________________
①过滤 ②加过量的NaOH溶液 ③加适量的盐酸 ④加过量的Na2CO3溶液 ⑤加过量的BaCl2溶液
(3)在该装置中写出装NaOH溶液试管中所发生的化学反应方程式(并用双线桥表示电子的转移的方向和数目)_____________________ 。

(1)写出电解饱和食盐水的化学方程式
(2)实际生产中使用的盐往往含有一些杂质,在电解食盐水之前,需要提纯食盐水。为了除去粗盐中的Ca2+、Mg2+、SO42-及泥沙,可将粗盐溶于水,然后进行下列五项操作,正确的操作顺序是
①过滤 ②加过量的NaOH溶液 ③加适量的盐酸 ④加过量的Na2CO3溶液 ⑤加过量的BaCl2溶液
| A.①④②⑤③ | B.④①②⑤③ | C.②⑤④①③ | D.⑤②④③① |
(3)在该装置中写出装NaOH溶液试管中所发生的化学反应方程式(并用双线桥表示电子的转移的方向和数目)
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】NaClO、 、
、 为常见高效的消毒剂和漂白剂。
为常见高效的消毒剂和漂白剂。
(1) 是国际上公认的安全绿色消毒剂。可用氯酸钠和H2O2溶液在酸性条件下制备,反应的化学方程式为
是国际上公认的安全绿色消毒剂。可用氯酸钠和H2O2溶液在酸性条件下制备,反应的化学方程式为 (未配平)。该反应中
(未配平)。该反应中 与
与 的化学计量数之比为
的化学计量数之比为___________ (不考虑 的分解)。
的分解)。
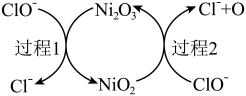
(2)①“84”消毒液的有效成分为NaClO。工业上常用碱性NaClO废液吸收 ,部分催化过程如图所示。“过程1”中
,部分催化过程如图所示。“过程1”中 是
是___________ (填“氧化剂”或“还原剂”),当 和
和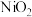 以物质的量之比1∶2发生“过程2”的反应,该反应的离子方程式为
以物质的量之比1∶2发生“过程2”的反应,该反应的离子方程式为___________ 。
②NaClO可在碱性条件下将 氧化为
氧化为 ,而自身被还原为NaCl,则
,而自身被还原为NaCl,则 与NaClO的个数比为
与NaClO的个数比为___________ 。
(3)以氯酸钠、硫酸和二氧化硫为原料制备 ,进而再利用
,进而再利用 与
与 溶液反应制备亚氯酸钠(
溶液反应制备亚氯酸钠( ),具体流程如下:
),具体流程如下:
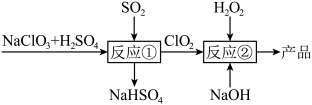
反应①的离子方程式为___________ ;理论上,该流程中参与反应的 与
与 的物质的量之比为
的物质的量之比为___________ 。
 、
、 为常见高效的消毒剂和漂白剂。
为常见高效的消毒剂和漂白剂。(1)
 是国际上公认的安全绿色消毒剂。可用氯酸钠和H2O2溶液在酸性条件下制备,反应的化学方程式为
是国际上公认的安全绿色消毒剂。可用氯酸钠和H2O2溶液在酸性条件下制备,反应的化学方程式为 (未配平)。该反应中
(未配平)。该反应中 与
与 的化学计量数之比为
的化学计量数之比为 的分解)。
的分解)。(2)①“84”消毒液的有效成分为NaClO。工业上常用碱性NaClO废液吸收
 ,部分催化过程如图所示。“过程1”中
,部分催化过程如图所示。“过程1”中 是
是 和
和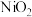 以物质的量之比1∶2发生“过程2”的反应,该反应的离子方程式为
以物质的量之比1∶2发生“过程2”的反应,该反应的离子方程式为
②NaClO可在碱性条件下将
 氧化为
氧化为 ,而自身被还原为NaCl,则
,而自身被还原为NaCl,则 与NaClO的个数比为
与NaClO的个数比为(3)以氯酸钠、硫酸和二氧化硫为原料制备
 ,进而再利用
,进而再利用 与
与 溶液反应制备亚氯酸钠(
溶液反应制备亚氯酸钠( ),具体流程如下:
),具体流程如下:
反应①的离子方程式为
 与
与 的物质的量之比为
的物质的量之比为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】完成并配平下列化学方程式__ FeO +__ HNO3——___ Fe(NO3)3 +___ NO↑+__ ____ ,该反应中氧化剂是________ ,当生成2mol NO时,转移的电子数为________ NA。
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】在工业上次磷酸(H3PO2)常用于化学镀银,发生的反应如下:_______Ag++_______H3PO2_______H2O→_______Ag↓+_______H3PO4+_______H+
请回答下列问题:
(1)H3PO2中,P元素的化合价为_______ ;该反应中,还原产物是_______ 。若有lmolH3PO2参加该反应,则反应中转移电子的物质的量为_______ mol。
(2)该反应中,表现氧化性与表现还原性的微粒物质的量之比为_______ 。
(3)已知H3PO2是一元弱酸,写出其与足量NaOH溶液反应的离子方程:_______ 。
(4)若改用氯气将溶液中的H3PO2氧化为H3PO4,其反应的化学方程式为_______ 。
请回答下列问题:
(1)H3PO2中,P元素的化合价为
(2)该反应中,表现氧化性与表现还原性的微粒物质的量之比为
(3)已知H3PO2是一元弱酸,写出其与足量NaOH溶液反应的离子方程:
(4)若改用氯气将溶液中的H3PO2氧化为H3PO4,其反应的化学方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】有 、Fe3+、
、Fe3+、 、Fe2+、H+和H2O六种微粒,分别属于一个氧化还原反应中的反应物和生成物.
、Fe2+、H+和H2O六种微粒,分别属于一个氧化还原反应中的反应物和生成物.
(1)氧化剂与还原剂的物质的量之比为________
(2)若有l mol NO3﹣参加反应,则转移________ mol e﹣
(3)若把该反应设计为原电池,则负极反应为________ .
 、Fe3+、
、Fe3+、 、Fe2+、H+和H2O六种微粒,分别属于一个氧化还原反应中的反应物和生成物.
、Fe2+、H+和H2O六种微粒,分别属于一个氧化还原反应中的反应物和生成物.(1)氧化剂与还原剂的物质的量之比为
(2)若有l mol NO3﹣参加反应,则转移
(3)若把该反应设计为原电池,则负极反应为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】亚硝酸钠( )是一种用途广泛的工业盐,因其外观和食盐相似容易误食中毒。亚硝酸钠加热到320℃以上会分解产生
)是一种用途广泛的工业盐,因其外观和食盐相似容易误食中毒。亚硝酸钠加热到320℃以上会分解产生 、
、 和
和 ,其水溶液呈碱性,能与
,其水溶液呈碱性,能与 溶液反应生成难溶于水、易溶于酸的
溶液反应生成难溶于水、易溶于酸的 。由于
。由于 有毒性,将含该物质的废水直接排放会引起水体严重污染,所以这种废水必须处理后才能排放。处理方法之一如下: _______
有毒性,将含该物质的废水直接排放会引起水体严重污染,所以这种废水必须处理后才能排放。处理方法之一如下: _______ _______
_______ _______
_______ _______
_______ _______
_______ _______
_______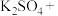 _______
_______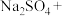 _______
_______
(1)请完成该化学方程式并配平。_______
(2) 中N的化合价为
中N的化合价为_______ ,由N的化合价推测 具有
具有_______ (填“氧化性”、“还原性”或“氧化性、还原性”)。
(3)用上述反应来处理 并不是最佳方法,其原因是
并不是最佳方法,其原因是_______ 。从环保角度来讲,要将 转化为氮气,所用物质的
转化为氮气,所用物质的_______ (填“氧化性”或“还原性”)应该比 更
更_______ (填“强”或“弱”)。
(4)下列方法不能用来区分固体 和
和 的是_______(填序号)。
的是_______(填序号)。
(5) 与
与 反应:
反应: ,若有0.5mol氧化剂被还原,则被氧化的还原剂的物质的量是
,若有0.5mol氧化剂被还原,则被氧化的还原剂的物质的量是_______ mol。
(6)已知亚硝酸钠可以与氯化铵反应生成氮气和氯化钠,写出该反应的化学反应方程式_______ 。
 )是一种用途广泛的工业盐,因其外观和食盐相似容易误食中毒。亚硝酸钠加热到320℃以上会分解产生
)是一种用途广泛的工业盐,因其外观和食盐相似容易误食中毒。亚硝酸钠加热到320℃以上会分解产生 、
、 和
和 ,其水溶液呈碱性,能与
,其水溶液呈碱性,能与 溶液反应生成难溶于水、易溶于酸的
溶液反应生成难溶于水、易溶于酸的 。由于
。由于 有毒性,将含该物质的废水直接排放会引起水体严重污染,所以这种废水必须处理后才能排放。处理方法之一如下: _______
有毒性,将含该物质的废水直接排放会引起水体严重污染,所以这种废水必须处理后才能排放。处理方法之一如下: _______ _______
_______ _______
_______ _______
_______ _______
_______ _______
_______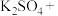 _______
_______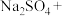 _______
_______
(1)请完成该化学方程式并配平。
(2)
 中N的化合价为
中N的化合价为 具有
具有(3)用上述反应来处理
 并不是最佳方法,其原因是
并不是最佳方法,其原因是 转化为氮气,所用物质的
转化为氮气,所用物质的 更
更(4)下列方法不能用来区分固体
 和
和 的是_______(填序号)。
的是_______(填序号)。| A.分别溶于水并滴加酚酞试液 | B.分别溶于水并滴加 酸化的 酸化的 溶液 溶液 |
| C.分别加强热并收集气体检验 | D.用筷子分别蘸取固体品尝味道 |
 与
与 反应:
反应: ,若有0.5mol氧化剂被还原,则被氧化的还原剂的物质的量是
,若有0.5mol氧化剂被还原,则被氧化的还原剂的物质的量是(6)已知亚硝酸钠可以与氯化铵反应生成氮气和氯化钠,写出该反应的化学反应方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】阅读下面一段材料并答问题。
高铁酸钾使用说明书
【化学式】K2FeO4
【性状】暗紫色具有金属光泽的粉末,无臭无味
【产品特点】干燥品在室温下稳定,在强碱溶液中稳定,随着pH减小,稳定性下降,与水反应放出氧气
K2FeO4通过强烈的氧化作用可迅速杀灭细菌,有消毒作用,同时不会产生有害物质。
K2FeO4与水反应还能产生具有强吸附性的Fe(OH)3胶体,可除去水中细微的悬浮物,有净水作用
【用途】主要用于饮用水消毒净化、城市生活污水和工业污水处理
【用量】消毒净化1L水投放5mgK2FeO4,即可达到卫生标准
(1)K2FeO4中铁元素的化合价为___________ 。
(2)制备K2FeO4需要在___________ (填“酸性”、“破性”或“中性”)环境中进行。
(3)下列关于K2FeO4的说法中,不正确的是___________
a.是强氧化性的盐 b.固体保存需要防潮
c.其消毒和净化水的原理相同 d.其净水优点有:作用快、安全性好、无异味
(4)高铁酸钠是一种新型的净水剂,可以通过下述反应制取:
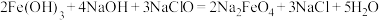
①该反应中的氧化剂是___________ ,___________ 元素被氧化,还原产物为___________ 。
②用双线桥法在化学方程式中标出电子转移的情况:___________ 。
高铁酸钾使用说明书
【化学式】K2FeO4
【性状】暗紫色具有金属光泽的粉末,无臭无味
【产品特点】干燥品在室温下稳定,在强碱溶液中稳定,随着pH减小,稳定性下降,与水反应放出氧气
K2FeO4通过强烈的氧化作用可迅速杀灭细菌,有消毒作用,同时不会产生有害物质。
K2FeO4与水反应还能产生具有强吸附性的Fe(OH)3胶体,可除去水中细微的悬浮物,有净水作用
【用途】主要用于饮用水消毒净化、城市生活污水和工业污水处理
【用量】消毒净化1L水投放5mgK2FeO4,即可达到卫生标准
(1)K2FeO4中铁元素的化合价为
(2)制备K2FeO4需要在
(3)下列关于K2FeO4的说法中,不正确的是
a.是强氧化性的盐 b.固体保存需要防潮
c.其消毒和净化水的原理相同 d.其净水优点有:作用快、安全性好、无异味
(4)高铁酸钠是一种新型的净水剂,可以通过下述反应制取:
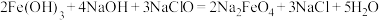
①该反应中的氧化剂是
②用双线桥法在化学方程式中标出电子转移的情况:
您最近一年使用:0次



