现有下列十种物质:①Na2O ②Cu(OH)2 ③Zn ④CaCO3 ⑤硫酸溶液 ⑥Ba(OH2 ⑦干冰 ⑧A12(SO4)3 ⑨HCl水溶液 ⑩KHSO4
(1)其中属于非电解质的有__________ (填序号).
(2)写出下列物质在水溶液中相互反应的离子方程式:
⑤+⑥__________
④+⑨__________
往②中加入过量的0.1mol/L⑩的水溶液,发生反应的离子方程式是__________ ,
往⑩中加入③,有气泡冒出,则此离子方程式是__________
(1)其中属于非电解质的有
(2)写出下列物质在水溶液中相互反应的离子方程式:
⑤+⑥
④+⑨
往②中加入过量的0.1mol/L⑩的水溶液,发生反应的离子方程式是
往⑩中加入③,有气泡冒出,则此离子方程式是
更新时间:2018-01-08 12:38:10
|
相似题推荐
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】现有以下物质:
①稀硫酸②蔗糖③熔融的KNO3④NaHSO4固体⑤BaSO4⑥NaOH⑦Cl2⑧CO2。
(1)属于电解质的是____ ,属于非电解质的是____ ,能导电的是____ 。
(2)写出NaOH和CO2按物质的量4∶3在水溶液中发生的离子方程式:____ 。
(3)在NaHSO4溶液中逐滴加入Ba(OH)2溶液,至溶液呈中性 时的离子方程式:____ ;在以上中性溶液中,继续滴加Ba(OH)2溶液,发生反应的离子方程式____ 。
①稀硫酸②蔗糖③熔融的KNO3④NaHSO4固体⑤BaSO4⑥NaOH⑦Cl2⑧CO2。
(1)属于电解质的是
(2)写出NaOH和CO2按物质的量4∶3在水溶液中发生的离子方程式:
(3)在NaHSO4溶液中逐滴加入Ba(OH)2溶液,至溶液
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐2】氧化还原反应在工农业生产、日常生活中具有广泛用途,贯穿古今。
(1)工业盐的主要成分是 ,以前有许多起因误食
,以前有许多起因误食 而中毒的事件,其原因是
而中毒的事件,其原因是 把人体内的
把人体内的 转化为
转化为 而失去与
而失去与 结合的能力,这说明
结合的能力,这说明 具有
具有___________ 性。工业盐中毒后,可服用维生素C来缓解中毒状况,这说明维生素C具有___________ 性。
(2) 常用于焊接,在焊接铜器时可用
常用于焊接,在焊接铜器时可用 除去铜器表面的氧化铜,便于焊接,其反应如下:
除去铜器表面的氧化铜,便于焊接,其反应如下:
____ +___
+___
 ____
____ +_____
+_____ +_____
+_____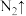 +_____
+_____
①配平上述氧化还原反应方程式______________ 。
②该反应中,氧化剂是___________ (填化学式),被氧化的元素是___________ (填元素名称)。
(3)二氧化氯是一种高效消毒剂。工业上制备 的反应为:
的反应为: 。
。
①该反应中的还原产物是___________ (写化学式),反应中每生成2个 分子,被氧化的
分子,被氧化的 为
为___________ 个,转移电子的数目为___________ 个。
②用“单线桥”标出反应中电子转移的方向与数目__________ 。
③ 在杀菌消毒的过程中会生成副产物亚氯酸盐(
在杀菌消毒的过程中会生成副产物亚氯酸盐( ),需要将其转化为
),需要将其转化为 除去,下列试剂能实现其转化过程的是
除去,下列试剂能实现其转化过程的是___________ (填字母)。
a. b.
b. c.
c. d.
d.
(4)双氧水是公认的绿色氧化剂。已知氧化性强弱顺序为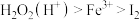 ,向
,向 溶液中加入足量硫酸酸化的双氧水,发生反应的离子方程式为
溶液中加入足量硫酸酸化的双氧水,发生反应的离子方程式为___________ 。
(1)工业盐的主要成分是
 ,以前有许多起因误食
,以前有许多起因误食 而中毒的事件,其原因是
而中毒的事件,其原因是 把人体内的
把人体内的 转化为
转化为 而失去与
而失去与 结合的能力,这说明
结合的能力,这说明 具有
具有(2)
 常用于焊接,在焊接铜器时可用
常用于焊接,在焊接铜器时可用 除去铜器表面的氧化铜,便于焊接,其反应如下:
除去铜器表面的氧化铜,便于焊接,其反应如下:____
 +___
+___
 ____
____ +_____
+_____ +_____
+_____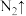 +_____
+_____
①配平上述氧化还原反应方程式
②该反应中,氧化剂是
(3)二氧化氯是一种高效消毒剂。工业上制备
 的反应为:
的反应为: 。
。①该反应中的还原产物是
 分子,被氧化的
分子,被氧化的 为
为②用“单线桥”标出反应中电子转移的方向与数目
③
 在杀菌消毒的过程中会生成副产物亚氯酸盐(
在杀菌消毒的过程中会生成副产物亚氯酸盐( ),需要将其转化为
),需要将其转化为 除去,下列试剂能实现其转化过程的是
除去,下列试剂能实现其转化过程的是a.
 b.
b. c.
c. d.
d.
(4)双氧水是公认的绿色氧化剂。已知氧化性强弱顺序为
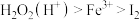 ,向
,向 溶液中加入足量硫酸酸化的双氧水,发生反应的离子方程式为
溶液中加入足量硫酸酸化的双氧水,发生反应的离子方程式为
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】按要求完成下列填空:
(1)硫酸钡的电离方程式:_______ 。
(2)盐酸和小苏打反应离子方程式:_______ 。
(3)向硫酸氢钠溶液中逐滴加入氢氧化钡,溶液恰好显中性时反应的离子方程式:_______ 。
(4)向澄清石灰水中通入过量CO2反应的离子方程式:_______ 。
(5)配平下列方程式,并用双线桥表示电子转移的数目与氧化还原、化合价变化之间的关系: +Fe2++____=Mn2++Fe3++____,
+Fe2++____=Mn2++Fe3++____,___________ 。
(1)硫酸钡的电离方程式:
(2)盐酸和小苏打反应离子方程式:
(3)向硫酸氢钠溶液中逐滴加入氢氧化钡,溶液恰好显中性时反应的离子方程式:
(4)向澄清石灰水中通入过量CO2反应的离子方程式:
(5)配平下列方程式,并用双线桥表示电子转移的数目与氧化还原、化合价变化之间的关系:
 +Fe2++____=Mn2++Fe3++____,
+Fe2++____=Mn2++Fe3++____,
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】某城市对大气进行监测,发现该市首要污染物为可吸入颗粒物PM2.5(直径小于等于2.5 μm的悬浮颗粒物),其主要来源为燃煤、机动车尾气等。因此,对PM2.5、SO2、NOx等进行研究具有重要意义。请回答下列问题:
(1)PM2.5分散在空气中形成的分散系________ (填“属于”或“不属于”)胶体。
(2)将PM2.5样本用蒸馏水处理制成待测试样。若测得该试样所含水溶性无机离子的化学组分及其平均浓度如下表:
根据表中数据判断待测试样为________ (填“酸”或“碱”)性,表示该试样酸碱性的c(H+)或c(OH-)=________ mol·L-1。
(3)煤燃烧排放的烟气含有SO2和NOx,形成酸雨,污染大气,采用NaClO2溶液在碱性条件下可对烟气进行脱硫,脱硝,效果非常好。完成下列对烟气脱硝过程的离子方程式。______  +
+______ NO+______ =______ Cl-+______  +
+______
(4)为减少SO2的排放,常采取的措施有:
①将煤转化为清洁气体燃料。写出焦炭与水蒸气反应的化学方程式:__________________ 。
②洗涤含SO2的烟气。以下物质可作洗涤剂的是______ (填字母)。
a.Ca(OH)2 b.Na2CO3 c.CaCl2 d.NaHSO3
(5)汽车尾气中NOx和CO的生成及转化。
①汽车启动后,汽缸温度越高,单位时间内NO排放量越大,写出汽缸中生成NO的化学方程式:_________________________________________________________________ 。
②汽车燃油不完全燃烧时产生CO,目前,在汽车尾气系统中装置催化转化器可减少CO和NO的污染,其化学反应方程式为__________________________________________________ 。
(1)PM2.5分散在空气中形成的分散系
(2)将PM2.5样本用蒸馏水处理制成待测试样。若测得该试样所含水溶性无机离子的化学组分及其平均浓度如下表:
| 离子 | K+ | Na+ |  |  |  | Cl- |
| 浓度/mol·L-1 | 4×10-6 | 6×10-6 | 2×10-5 | 4×10-5 | 3×10-5 | 2×10-5 |
根据表中数据判断待测试样为
(3)煤燃烧排放的烟气含有SO2和NOx,形成酸雨,污染大气,采用NaClO2溶液在碱性条件下可对烟气进行脱硫,脱硝,效果非常好。完成下列对烟气脱硝过程的离子方程式。
 +
+ +
+(4)为减少SO2的排放,常采取的措施有:
①将煤转化为清洁气体燃料。写出焦炭与水蒸气反应的化学方程式:
②洗涤含SO2的烟气。以下物质可作洗涤剂的是
a.Ca(OH)2 b.Na2CO3 c.CaCl2 d.NaHSO3
(5)汽车尾气中NOx和CO的生成及转化。
①汽车启动后,汽缸温度越高,单位时间内NO排放量越大,写出汽缸中生成NO的化学方程式:
②汽车燃油不完全燃烧时产生CO,目前,在汽车尾气系统中装置催化转化器可减少CO和NO的污染,其化学反应方程式为
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐1】以黄铁矿(主要成分是 ,含少量
,含少量 )和软锰矿(主要成分是
)和软锰矿(主要成分是 ,含少量
,含少量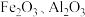 )为原料制备
)为原料制备 的工艺流程如下:
的工艺流程如下: 时,
时, 。
。
(1)沉锰过程需控制温度为 的原因是
的原因是_______ 。
(2)下图为 的溶解度曲线,操作A是加入足量稀硫酸充分反应后,
的溶解度曲线,操作A是加入足量稀硫酸充分反应后,_______ 洗涤干燥。
 ,含少量
,含少量 )和软锰矿(主要成分是
)和软锰矿(主要成分是 ,含少量
,含少量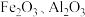 )为原料制备
)为原料制备 的工艺流程如下:
的工艺流程如下:
 时,
时, 。
。(1)沉锰过程需控制温度为
 的原因是
的原因是(2)下图为
 的溶解度曲线,操作A是加入足量稀硫酸充分反应后,
的溶解度曲线,操作A是加入足量稀硫酸充分反应后,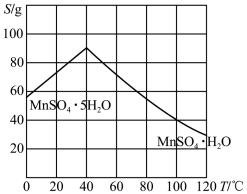
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】我国很早就使用青铜器,由于时间久远,其表面有一层“绿锈”,“绿锈”俗称“铜绿”,是铜和空气中的水蒸气、CO2、O2作用产生的,化学式为[Cu2(OH)2CO3],“铜绿”能跟酸反应生成铜盐、CO2和H2O。某同学利用以下反应实现了“铜→铜绿→……→铜”的转化。
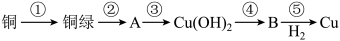
(1)从物质分类标准看,“铜绿”属于___ (填字母)。
A.酸 B.碱 C.盐 D.氧化物
(2)请写出铜绿与盐酸反应的离子方程式:___ 。
(3)上述转化过程中属于氧化还原反应的是___ (填序号)
(4)铜绿在受热时可直接分解生成物质B、CO2和水,其分解的化学方程式为___ 。

(1)从物质分类标准看,“铜绿”属于
A.酸 B.碱 C.盐 D.氧化物
(2)请写出铜绿与盐酸反应的离子方程式:
(3)上述转化过程中属于氧化还原反应的是
(4)铜绿在受热时可直接分解生成物质B、CO2和水,其分解的化学方程式为
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】钛(Ti)因为具有神奇的性能越来越引起人们的关注。常温下,钛不和非金属、强酸反应;红热时,却可与常见的非金属单质反应。钛是航空、军工、电力等方面的必需原料。地壳中含钛矿石之一称金红石(TiO2)目前大规模生产钛的方法是:
第一步:金红石、碳粉混合,在高温条件下通入氯气制得TiCl4和一种可燃性气体。该反应的化学方程式是______ ,该反应的还原剂是______ 。
第二步:在氩气的气氛中,用过量的镁在加热条件下与TiCl4反应制得金属钛。
(1)此反应的化学方程式是______ 。
(2)简述由上述所得产物中获取金属钛的步骤______ 。
第一步:金红石、碳粉混合,在高温条件下通入氯气制得TiCl4和一种可燃性气体。该反应的化学方程式是
第二步:在氩气的气氛中,用过量的镁在加热条件下与TiCl4反应制得金属钛。
(1)此反应的化学方程式是
(2)简述由上述所得产物中获取金属钛的步骤
您最近一年使用:0次




