若m g Na在足量氯气中燃烧,生成固体的质量为(m+3.55)g,则m g Na与氧气反应,生成固体的质量可能为
①(m+0.8)g ②(m+1.0)g ③(m+1.2)g ④(m+1.6)g ⑤(m+1.8)g
①(m+0.8)g ②(m+1.0)g ③(m+1.2)g ④(m+1.6)g ⑤(m+1.8)g
| A.仅①④ | B.仅①⑤ | C.仅③④ | D.仅①②③④ |
17-18高一上·江西南昌·阶段练习 查看更多[3]
福建省厦门外国语学校2019-2020学年高一上学期第一次月考(10月)化学试题(已下线)练习5 金属的化学性质-2020-2021学年【补习教材·寒假作业】高一化学(人教版)江西省南昌市八一中学2017-2018学年高一1月月考化学试题
更新时间:2018-01-12 20:07:25
|
相似题推荐
单选题
|
较难
(0.4)
名校
【推荐1】过氧化钠可与CO2作用,当0.2molNa218O2完全作用后,生成的Na2CO3的质量为
| A.21.2g | B.2l.6g | C.22.0g | D.22.4g |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】下列说法正确的是
①有单质参加或生成的反应一定是氧化还原反应
②向Al2(SO4)3溶液中逐滴滴加Ba(OH)2溶液,先生成白色沉淀,后沉淀消失
③向含有BaCl2和NaOH的混合溶液中通入少量的二氧化硫气体,有白色沉淀生成
④向CaCl2溶液中通入足量二氧化碳气体,先生成白色沉淀,后沉淀消失
⑤101kPa、150℃时,agCO和H2的混合气体在足量的O2中完全燃烧,将燃烧后的产物通入足量的Na2O2固体后,Na2O2增重ag
⑥为测定熔融氢氧化钠的导电性,可在刚玉(主要成分是Al2O3) 坩埚中熔化氢氧化钠固体后进行测量
⑦碱性氧化物一定是金属氧化物
⑧22.4L的CO气体和28gN2所含的电子数相等
①有单质参加或生成的反应一定是氧化还原反应
②向Al2(SO4)3溶液中逐滴滴加Ba(OH)2溶液,先生成白色沉淀,后沉淀消失
③向含有BaCl2和NaOH的混合溶液中通入少量的二氧化硫气体,有白色沉淀生成
④向CaCl2溶液中通入足量二氧化碳气体,先生成白色沉淀,后沉淀消失
⑤101kPa、150℃时,agCO和H2的混合气体在足量的O2中完全燃烧,将燃烧后的产物通入足量的Na2O2固体后,Na2O2增重ag
⑥为测定熔融氢氧化钠的导电性,可在刚玉(主要成分是Al2O3) 坩埚中熔化氢氧化钠固体后进行测量
⑦碱性氧化物一定是金属氧化物
⑧22.4L的CO气体和28gN2所含的电子数相等
| A.①②④⑥⑧ | B.③④⑤ | C.①⑤⑥⑦ | D.③⑤⑦ |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐3】下列关于有机化合物说法正确的是( )
A.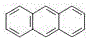 (蒽) (蒽)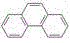 (菲)两者互为同分异构体,因1H-NMR谱(核磁共振氢谱)显示两者均有三种不同的氢原子,且比例均为2:2:1,故不能用1H-NMR谱鉴别它们 (菲)两者互为同分异构体,因1H-NMR谱(核磁共振氢谱)显示两者均有三种不同的氢原子,且比例均为2:2:1,故不能用1H-NMR谱鉴别它们 |
| B.天然纤维和合成纤维的主要成分都是纤维素 |
| C.一般不能使用过酸的洗涤剂洗涤棉织品有丝织品,不能使用过碱的洗涤剂洗涤氨纶(聚氨基甲酸酯纤维)、腈纶(聚丙烯腈)等合成纤维制品 |
| D.一定条件下将总质量相等的CH3OH,CH3COOH混合物或HCOOH、HOCOOCH2OH混合物在氧气中完全燃烧,燃烧后的全部产物通入足量过氧化钠层,过氧化钠层增加的质量之比为23:15 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐1】测定CuSO4·xH2O晶体的x值,数据如表中所示,已知x的理论值为5.0,产生误差的可能原因是
坩埚质量 | 坩埚+试样 | 失水后,坩埚+试样 |
11.70g | 20.82g | 16.50g |
| A.晶体中含不挥发杂质 | B.未做恒重操作 |
| C.加热前晶体未研磨 | D.加热时有晶体溅出 |
您最近一年使用:0次
单选题
|
较难
(0.4)
解题方法
【推荐2】将8.34 g FeSO4·7H2O样品隔绝空气加热脱水,其热重曲线(样品质量随温度变化的曲线)如图所示。则下列说法不正确的是( )


| A.在100℃时,M的化学式为FeSO4·4H2O |
| B.FeSO4·7H2O晶体中有4种不同结合力的水分子 |
| C.FeSO4·H2O存在的最高温度为373℃ |
D.380℃的P加热至650℃时的化学方程式为:2FeSO4 Fe2O3+SO2↑+SO3↑ Fe2O3+SO2↑+SO3↑ |
您最近一年使用:0次
单选题
|
较难
(0.4)
解题方法
【推荐3】工业碱的主要成分主要是NaOH和 或
或 和
和 (无其他杂质)。实验室用盐酸做标准溶液,酚酞和甲基橙双指示剂来滴定测定工业碱的组成和含量。已知室温下
(无其他杂质)。实验室用盐酸做标准溶液,酚酞和甲基橙双指示剂来滴定测定工业碱的组成和含量。已知室温下 溶液的pH为8.32,饱和
溶液的pH为8.32,饱和 溶液的pH为3.89。实验步骤如下:
溶液的pH为3.89。实验步骤如下:
①量取6.0 盐酸5.0mL加入到245mL蒸馏水中混合均匀备用。
盐酸5.0mL加入到245mL蒸馏水中混合均匀备用。
②称取1.06g无水 置于小烧杯中,加入适量蒸馏水溶解并转移到100mL容量瓶中,定容摇匀后转移到试剂瓶中备用。
置于小烧杯中,加入适量蒸馏水溶解并转移到100mL容量瓶中,定容摇匀后转移到试剂瓶中备用。
③量取15.00mL 溶液,加1~2滴甲基橙,用标准盐酸滴定至溶液由黄色变橙色,3次平行实验所用盐酸平均体积为V mL,计算标准盐酸浓度。
溶液,加1~2滴甲基橙,用标准盐酸滴定至溶液由黄色变橙色,3次平行实验所用盐酸平均体积为V mL,计算标准盐酸浓度。
④称取一定质量的工业碱置于烧杯中,加入适量蒸馏水溶解,配置成250mL溶液。量取25.00mL于锥形瓶中,加入指示剂1,用标准盐酸滴定至终点1,记录所用盐酸体积;再加入指示剂2,继续用标准盐酸滴定至终点2,记录所用盐酸体积。进行3次平行实验,终点1所用标准盐酸平均体积 mL,终点2所用标准盐酸平均体积为
mL,终点2所用标准盐酸平均体积为 mL。
mL。
下列说法正确的是
 或
或 和
和 (无其他杂质)。实验室用盐酸做标准溶液,酚酞和甲基橙双指示剂来滴定测定工业碱的组成和含量。已知室温下
(无其他杂质)。实验室用盐酸做标准溶液,酚酞和甲基橙双指示剂来滴定测定工业碱的组成和含量。已知室温下 溶液的pH为8.32,饱和
溶液的pH为8.32,饱和 溶液的pH为3.89。实验步骤如下:
溶液的pH为3.89。实验步骤如下:①量取6.0
 盐酸5.0mL加入到245mL蒸馏水中混合均匀备用。
盐酸5.0mL加入到245mL蒸馏水中混合均匀备用。②称取1.06g无水
 置于小烧杯中,加入适量蒸馏水溶解并转移到100mL容量瓶中,定容摇匀后转移到试剂瓶中备用。
置于小烧杯中,加入适量蒸馏水溶解并转移到100mL容量瓶中,定容摇匀后转移到试剂瓶中备用。③量取15.00mL
 溶液,加1~2滴甲基橙,用标准盐酸滴定至溶液由黄色变橙色,3次平行实验所用盐酸平均体积为V mL,计算标准盐酸浓度。
溶液,加1~2滴甲基橙,用标准盐酸滴定至溶液由黄色变橙色,3次平行实验所用盐酸平均体积为V mL,计算标准盐酸浓度。④称取一定质量的工业碱置于烧杯中,加入适量蒸馏水溶解,配置成250mL溶液。量取25.00mL于锥形瓶中,加入指示剂1,用标准盐酸滴定至终点1,记录所用盐酸体积;再加入指示剂2,继续用标准盐酸滴定至终点2,记录所用盐酸体积。进行3次平行实验,终点1所用标准盐酸平均体积
 mL,终点2所用标准盐酸平均体积为
mL,终点2所用标准盐酸平均体积为 mL。
mL。下列说法正确的是
A.标准盐酸的浓度为0.12 |
| B.步骤③中V可能等于12.50mL |
C.若 ,试样的成分为NaOH和 ,试样的成分为NaOH和 |
D.若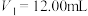 , ,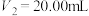 ,则 ,则 的质量分数为34.57% 的质量分数为34.57% |
您最近一年使用:0次



