(1)钠的金属活动性比铝的______ (填“强”或“弱)。
(2)Fe跟Cl2在一定条件下反应,所得产物的化学式是_____ 。
(3)Na、Mg、Al分别与足量的盐酸反应,当生成气体的质量相同时,消耗Na、Mg、Al的物质的量之比为________ 。
(4)等质量的铝分别与足量的盐酸、氢氧化钠反应产生氢气在同温同压的体积之比为______ 。
(2)Fe跟Cl2在一定条件下反应,所得产物的化学式是
(3)Na、Mg、Al分别与足量的盐酸反应,当生成气体的质量相同时,消耗Na、Mg、Al的物质的量之比为
(4)等质量的铝分别与足量的盐酸、氢氧化钠反应产生氢气在同温同压的体积之比为
更新时间:2018/01/16 21:04:06
|
相似题推荐
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】现有4.6gNa、2.4gMg、2.7gAl和6.4gCu,分别将其投入盛有100mL1.5mol/L盐酸的4个烧杯。
(1)各烧杯中可能发生反应的化学方程式为:___________ 、_____________ 、__________ 、______________ 。
(2)反应结束后,没有剩余的金属是:__________ (填元素符号);
(3)反应结束后,产生气体的物质的量分别为:
①投入Na的烧杯,生成气体________ mol;
②投入Mg的烧杯,生成气体________ mol;
③投入Al的烧杯,生成气体________ mol;
④投入Cu的烧杯,生成气体________ mol;
(1)各烧杯中可能发生反应的化学方程式为:
(2)反应结束后,没有剩余的金属是:
(3)反应结束后,产生气体的物质的量分别为:
①投入Na的烧杯,生成气体
②投入Mg的烧杯,生成气体
③投入Al的烧杯,生成气体
④投入Cu的烧杯,生成气体
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】某研究性学习小组设计了一组实验,验证元素周期律。
甲同学在a、b、c、d四只烧杯里分别加入50mL冷水,再分别滴加几滴酚酞溶液,依次加入大小相近的钠(Na)、镁(Mg)、铝(Al)、钾(K)金属块,观察现象。
(1)甲同学设计实验的目的是验证:同一主族,从上到下元素的元素金属性逐渐增强;同一周期,从左到右,元素金属性_______ ;
(2)反应最剧烈的烧杯里金属是_____ (填字母)
(3)写出a烧杯里发生反应的离子方程式_______ 。
(4)实验中发现b、c两只烧杯中几乎没有什么现象,要想达到实验的目的,请你帮助选择下列合适的方法 。
(5)写出铝和盐酸反应的化学方程式_______ 。
甲同学在a、b、c、d四只烧杯里分别加入50mL冷水,再分别滴加几滴酚酞溶液,依次加入大小相近的钠(Na)、镁(Mg)、铝(Al)、钾(K)金属块,观察现象。
(1)甲同学设计实验的目的是验证:同一主族,从上到下元素的元素金属性逐渐增强;同一周期,从左到右,元素金属性
(2)反应最剧烈的烧杯里金属是_____ (填字母)
| A.钠 | B.镁 | C.铝 | D.钾; |
(4)实验中发现b、c两只烧杯中几乎没有什么现象,要想达到实验的目的,请你帮助选择下列合适的方法 。
| A.把镁、铝的金属块换成金属粉末 |
| B.把烧杯中的冷水换成热水 |
| C.把烧杯中的冷水换成盐酸 |
| D.把烧杯中的冷水换成氢氧化钠溶液 |
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】钠和铝均是重要的金属。
(1) 铝的原子结构示意图是___________________ 。
(2) 铝与NaOH溶液反应的离子方程式为
铝与NaOH溶液反应的离子方程式为______________________________ ;
(3)同温同压下,在体积和浓度均为100 mL 0.2 mol·L-1的盐酸及NaOH溶液中各加入等质量的Al, 产生气体的体积之比为5∶6,则所加Al的质量为______________ 。
(4) 过氧化钠可做呼吸面具的供氧剂,其中Na2O2与CO2反应的化学方程式为________________ 。
(1) 铝的原子结构示意图是
(2)
 铝与NaOH溶液反应的离子方程式为
铝与NaOH溶液反应的离子方程式为(3)同温同压下,在体积和浓度均为100 mL 0.2 mol·L-1的盐酸及NaOH溶液中各加入等质量的Al, 产生气体的体积之比为5∶6,则所加Al的质量为
(4) 过氧化钠可做呼吸面具的供氧剂,其中Na2O2与CO2反应的化学方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】下表为元素周期表的一部分,用化学用语回答下列问题:
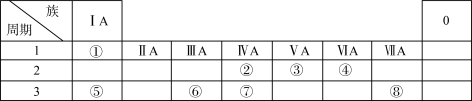
(1)化合物A是由⑤⑧两种元素构成的,用电子式表示其形成过程___________
(2)④、②元素形成的化合物的结构式__________
(3)②的最简单氢化物与氧气可以设计成燃料电池,写出在碱性条件下负极的电极方程式_____
(4)⑥的单质与⑤的最高价氧化物对应水化物的水溶液反应的离子方程式为:___________
(5)由①③⑧组成的M 物质中所含化学键的类型_________________
(6)M中的阳离子的鉴定方法是_______

(1)化合物A是由⑤⑧两种元素构成的,用电子式表示其形成过程
(2)④、②元素形成的化合物的结构式
(3)②的最简单氢化物与氧气可以设计成燃料电池,写出在碱性条件下负极的电极方程式
(4)⑥的单质与⑤的最高价氧化物对应水化物的水溶液反应的离子方程式为:
(5)由①③⑧组成的M 物质中所含化学键的类型
(6)M中的阳离子的鉴定方法是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】有以下物质:①石墨;②钠:③酒精;④氨气;⑤硫化氢;⑥碳酸氢钠固体;⑦氢氧化钡溶液;⑧纯醋酸;⑨氧化钠固体;⑩液态氯化氢。
(1)其中能导电的是___________ ;属于非电解质的是___________ 。
(2)等质量④和⑤中氢原子的数目之比为___________ ;若④和⑤中所含氢原子数相等,则④和⑤的质量之比为___________ 。
(3)写出⑥和⑩在水溶液中的离子方程式___________ 。
(4)雷雨天闪电时空气中有O3生成。O2与O3的关系是互为___________ ,等质量的O2和O3的分子数之比为___________ 。
(5)高温下Al粉与Fe2O3发生置换反应生成Fe,该反应能用来焊接钢轨,其中被还原的物质是___________ (填化学式)。NaOH溶液可检验反应后的固体中是否有Al残留,用离子方程式说明其原理___________ 。
(1)其中能导电的是
(2)等质量④和⑤中氢原子的数目之比为
(3)写出⑥和⑩在水溶液中的离子方程式
(4)雷雨天闪电时空气中有O3生成。O2与O3的关系是互为
(5)高温下Al粉与Fe2O3发生置换反应生成Fe,该反应能用来焊接钢轨,其中被还原的物质是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】对金属制品进行抗腐蚀处理,可延长其使用寿命。
(1)以下为铝材表面处理的一种方法。

①碱洗的目的是除去铝材表面的自然氧化膜,碱洗时常有气泡冒出,原因是__________ (用离子方程式表示)。为将碱洗槽液中的铝以沉淀形式回收,最好向槽液中加入(或通入)下列试剂中的______ 。
a. b.
b. c. NaOH溶液 d.硝酸
c. NaOH溶液 d.硝酸
②以铝材为阳极,在H2SO4溶液中电解,铝材表面形成氧化膜,阳极电极反应式为________ 。
(2)镀铜可防止铁制品腐蚀,电镀时用铜而不用石墨作阳极的原因是__________ 。
(3)用铝制饭盒盛放醋酸,一段时间后,饭盒被腐蚀,该种腐蚀属于__________ ,反应的化学方程式为__________ ;若用铝饭盒盛放食盐(含水)时,一段时间后,饭盒被腐蚀,这种腐蚀叫作__________ ,反应原理是__________ (写电极反应式)。
(1)以下为铝材表面处理的一种方法。

①碱洗的目的是除去铝材表面的自然氧化膜,碱洗时常有气泡冒出,原因是
a.
 b.
b. c. NaOH溶液 d.硝酸
c. NaOH溶液 d.硝酸②以铝材为阳极,在H2SO4溶液中电解,铝材表面形成氧化膜,阳极电极反应式为
(2)镀铜可防止铁制品腐蚀,电镀时用铜而不用石墨作阳极的原因是
(3)用铝制饭盒盛放醋酸,一段时间后,饭盒被腐蚀,该种腐蚀属于
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】一定量的铁粉在氯气中充分燃烧后,将所得固体完全溶于稀盐酸,制得溶液A。
(1)铁在氯气中燃烧的化学方程式是__________________________ 。
(2)推测A中可能含有的金属阳离子:① ;②只有
;②只有 ;③
;③_____________ 。
甲同学为探究溶液的组成,实验如下:
(3)乙同学继续探究溶液A的组成。
查阅资料:
实验过程:另取少量溶液A于试管中,逐滴加入酸性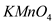 溶液,充分振荡,
溶液,充分振荡,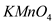 紫色褪去。
紫色褪去。
实验结论:_____________ (填字母序号)。
a. 可能有 b. 可能无
b. 可能无 c. 一定有
c. 一定有
(1)铁在氯气中燃烧的化学方程式是
(2)推测A中可能含有的金属阳离子:①
 ;②只有
;②只有 ;③
;③甲同学为探究溶液的组成,实验如下:
| 实验步骤 | 实验现象 | 实验结论及反应离子方程式 |
| 取少量溶液A于试管中,加入KSCN溶液 | 假设②不成立,假设①或③成立;反应的离子方程式是 |
(3)乙同学继续探究溶液A的组成。
查阅资料:

实验过程:另取少量溶液A于试管中,逐滴加入酸性
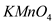 溶液,充分振荡,
溶液,充分振荡,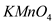 紫色褪去。
紫色褪去。实验结论:
a. 可能有
 b. 可能无
b. 可能无 c. 一定有
c. 一定有
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】A~G各物质间的关系如图,其中B、D为气态单质。
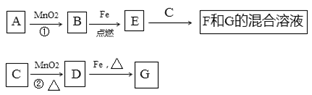
请回答下列问题:
(1)物质C、E分别为_____________ 、_____________ 。(填名称)
(2)反应①可选用不同的A进行,若反应在常温下进行,其化学方程式为_____________________ 。
(3)反应②的离子方程式为_____________________________________________________________ 。
(4)新配制的F溶液应加入________ 以防止其转化为G。请设计实验检验F、G的混合溶液中F的金属阳离子。(写出试剂、操作、现象、结论)_____________________________________________ 。
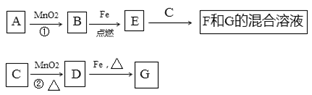
请回答下列问题:
(1)物质C、E分别为
(2)反应①可选用不同的A进行,若反应在常温下进行,其化学方程式为
(3)反应②的离子方程式为
(4)新配制的F溶液应加入
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】A、B、C均为中学化学常见的纯净物,它们之间存在如图转化关系,其中①②③均为有单质参与的反应。回答下列问题:
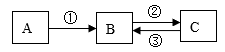
(1)若A是常见的金属,①③中均有同一种气态非金属单质参与反应,B溶液遇KSCN显血红色,且②为化合反应,写出反应②的离子方程式_______________________________________ 。
(2)若B是太阳能电池用的光伏材料,①②③为工业制备B的反应。C的化学式是___________ ,写出反应①的化学方程式_________________________________________ 。

(1)若A是常见的金属,①③中均有同一种气态非金属单质参与反应,B溶液遇KSCN显血红色,且②为化合反应,写出反应②的离子方程式
(2)若B是太阳能电池用的光伏材料,①②③为工业制备B的反应。C的化学式是
您最近一年使用:0次



