有关物质的转化关系如下图所示(部分生成物和反应条件已略去)。A 为由两种元素组成的固体,含非金属质量分数为39.13%;D、E、L均为无色气体,E 和L难溶于水;F 为常见金属;G、I、J焰色反应显黄色;M 为有颜色的固体。
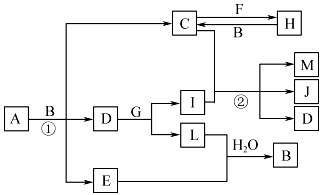
请回答下列问题:
(1)E的化学式为___________________ 。
(2)G的电子式为___________________ 。
(3)写出反应①的化学方程式:_______________________________ 。
(4)写出反应②的离子方程式:_______________________________ 。

请回答下列问题:
(1)E的化学式为
(2)G的电子式为
(3)写出反应①的化学方程式:
(4)写出反应②的离子方程式:
更新时间:2018-03-15 16:06:19
|
相似题推荐
解答题-实验探究题
|
较难
(0.4)
解题方法
【推荐1】铜是不活泼的金属,常见有 、
、 价。为探究铜及其化合物的性质,完成了两组实验,部分记录如下:
价。为探究铜及其化合物的性质,完成了两组实验,部分记录如下:
第一组:
完成下列填空:
(1)写出试管1中发生反应的离子方程式。___________
(2)试管2,预测步骤ⅱ后溶液不应呈红色,依据是___________ 。
(3)经测定试管2中得到的白色沉淀是 。
。
对生成 有两种猜测:
有两种猜测:
猜测① 和
和 反应生成
反应生成 ,根据
,根据___________ ,推知这一猜测错误。
猜测②生成白色沉淀是因为:Cu++SCN-=CuSCN↓。再请结合步骤ⅱ溶液出现红色的现象,解释生成沉淀的可能原因。___________ (用离子方程式表示)
第二组:水合肼(N2H4·H2O)和碱性铜氨[Cu(NH3)4]2+溶液混合反应,生成铜。
(4)水合肼溶液显弱碱性,其电离与NH3·H2O相似,写出水合肼的电离方程式:___________ 。
(5)将下列化学方程式补充完整、配平,并标出电子转移的数目和方向___________ 。
______N2H4·H2O+_____[Cu(NH3)4]2++_____OH-→_____Cu+_______N2↑+_______NH3+____H2O
(6)水合肼可用于还原锅炉水中溶解的O2,防止锅炉被腐蚀。与Na2SO3相比,使用水合肼处理水中溶解O2的优点是___________ (任写一点)。
 、
、 价。为探究铜及其化合物的性质,完成了两组实验,部分记录如下:
价。为探究铜及其化合物的性质,完成了两组实验,部分记录如下:第一组:
| 序号 | 试剂 | 实验步骤 | 实验现象 |
| 1 | 试管1中加2mL0.05mol·L-1Fe2(SO4)3溶液 | 加入1mL0.1mol·L-1KSCN溶液 | 溶液变为红色 |
| 2 | 试管2中加2mL0.05mol·L-1Fe2(SO4)3溶液 | ⅰ加入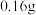 铜粉 铜粉 | 黄色溶液变为浅蓝色溶液 |
| ⅱ取上层清液,加入1滴0.1mol·L-1KSCN溶液 | 液滴接触上方变为红色,下方有白色沉淀生成 | ||
| 3 | 试管3中加2mL0.1mol·L-1 CuSO4溶液 | 加入1mL0.1mol·L-1KSCN溶液 | 溶液变成绿色 |
(1)写出试管1中发生反应的离子方程式。
(2)试管2,预测步骤ⅱ后溶液不应呈红色,依据是
(3)经测定试管2中得到的白色沉淀是
 。
。对生成
 有两种猜测:
有两种猜测:猜测①
 和
和 反应生成
反应生成 ,根据
,根据猜测②生成白色沉淀是因为:Cu++SCN-=CuSCN↓。再请结合步骤ⅱ溶液出现红色的现象,解释生成沉淀的可能原因。
第二组:水合肼(N2H4·H2O)和碱性铜氨[Cu(NH3)4]2+溶液混合反应,生成铜。
(4)水合肼溶液显弱碱性,其电离与NH3·H2O相似,写出水合肼的电离方程式:
(5)将下列化学方程式补充完整、配平,并标出电子转移的数目和方向
______N2H4·H2O+_____[Cu(NH3)4]2++_____OH-→_____Cu+_______N2↑+_______NH3+____H2O
(6)水合肼可用于还原锅炉水中溶解的O2,防止锅炉被腐蚀。与Na2SO3相比,使用水合肼处理水中溶解O2的优点是
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
名校
解题方法
【推荐2】 在磁性材料、电化学领域应用广泛,实验室中可以用
在磁性材料、电化学领域应用广泛,实验室中可以用 或
或 煅烧后制得。
煅烧后制得。
Ⅰ.实验室以 溶液和
溶液和 溶液为原料制备
溶液为原料制备 装置如图所示。
装置如图所示。

(1)写出基态 原子的价电子轨道表示式
原子的价电子轨道表示式______ 。
(2)仪器 的名称为
的名称为______ 。
(3)该反应需要控制温度在60-70℃,原因为______ ,选择加热的方式为______ 。
(4)制备 的离子方程式为
的离子方程式为______ 。
Ⅱ.测定 中钴的质量分数。
中钴的质量分数。
已知:
ii.电位滴定是利用溶液电位突变指示终点的滴定法
(5)经过过滤、洗涤、干燥得到沉淀 。某小组采用电位滴定法测定产品
。某小组采用电位滴定法测定产品 中钴的质量分数的实验步骤如下:准确称取10.000g产品溶于盐酸并配成1L溶液;取出20.00mL配得的溶液加入锥形瓶中,向其中加入
中钴的质量分数的实验步骤如下:准确称取10.000g产品溶于盐酸并配成1L溶液;取出20.00mL配得的溶液加入锥形瓶中,向其中加入
 溶液12.50mL(过量)充分反应后,用
溶液12.50mL(过量)充分反应后,用 的
的 标准溶液电位滴定过量的
标准溶液电位滴定过量的 ,三次滴定消耗
,三次滴定消耗 标准溶液的平均值为15.00mL。
标准溶液的平均值为15.00mL。
①滴定管在使用前需要______ 、用蒸馏水洗涤、______ 。
②该滴定实验的指示剂为______ (填字母)。
A.甲基橙 B. 溶液 C.不需要指示剂
溶液 C.不需要指示剂
③则产品中钴的质量分数为______ (保留两位有效数字)。
Ⅲ.制备
(6)取 在空气中加热制备
在空气中加热制备 ,请写出制备
,请写出制备 的化学方程式
的化学方程式______
 在磁性材料、电化学领域应用广泛,实验室中可以用
在磁性材料、电化学领域应用广泛,实验室中可以用 或
或 煅烧后制得。
煅烧后制得。Ⅰ.实验室以
 溶液和
溶液和 溶液为原料制备
溶液为原料制备 装置如图所示。
装置如图所示。
(1)写出基态
 原子的价电子轨道表示式
原子的价电子轨道表示式(2)仪器
 的名称为
的名称为(3)该反应需要控制温度在60-70℃,原因为
(4)制备
 的离子方程式为
的离子方程式为Ⅱ.测定
 中钴的质量分数。
中钴的质量分数。已知:

ii.电位滴定是利用溶液电位突变指示终点的滴定法
(5)经过过滤、洗涤、干燥得到沉淀
 。某小组采用电位滴定法测定产品
。某小组采用电位滴定法测定产品 中钴的质量分数的实验步骤如下:准确称取10.000g产品溶于盐酸并配成1L溶液;取出20.00mL配得的溶液加入锥形瓶中,向其中加入
中钴的质量分数的实验步骤如下:准确称取10.000g产品溶于盐酸并配成1L溶液;取出20.00mL配得的溶液加入锥形瓶中,向其中加入
 溶液12.50mL(过量)充分反应后,用
溶液12.50mL(过量)充分反应后,用 的
的 标准溶液电位滴定过量的
标准溶液电位滴定过量的 ,三次滴定消耗
,三次滴定消耗 标准溶液的平均值为15.00mL。
标准溶液的平均值为15.00mL。①滴定管在使用前需要
②该滴定实验的指示剂为
A.甲基橙 B.
 溶液 C.不需要指示剂
溶液 C.不需要指示剂③则产品中钴的质量分数为
Ⅲ.制备
(6)取
 在空气中加热制备
在空气中加热制备 ,请写出制备
,请写出制备 的化学方程式
的化学方程式
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
名校
解题方法
【推荐3】水合肼( )是一种用途广泛的化工原料,在空气中会与
)是一种用途广泛的化工原料,在空气中会与 反应产生烟雾。利用尿素制备
反应产生烟雾。利用尿素制备 的实验流程如下图所示:
的实验流程如下图所示:

回答下列问题:
(1)步骤Ⅰ制备 溶液的离子方程式为
溶液的离子方程式为_______ ;该反应为放热反应,为避免副反应发生,需控制温度不高于40℃,可采取的措施是_______ (任答一条)。
(2)由步骤Ⅱ和步骤Ⅲ获得 的装置如图1所示,反应原理为:
的装置如图1所示,反应原理为:


①仪器X的名称为_______ ,干燥管中盛装的试剂为_______ 。
② 的电子式为
的电子式为_______ 。
③反应过程中,如果分液漏斗中溶液滴速过快,部分 与
与 反应产生大量氮气,该化学反应方程式为
反应产生大量氮气,该化学反应方程式为_______ 。
④蒸馏获得水合肼粗品后,剩余溶液进一步处理还可获得副产品 和
和 ,
, 和
和 的溶解度曲线如图2所示。获得
的溶解度曲线如图2所示。获得 粗品的操作是蒸发结晶、
粗品的操作是蒸发结晶、_______ 、洗涤、干燥。

(3)馏分中水合肼含量的测定方法:称取馏分0.2500g,加入适量 固体,配成溶液,滴入0.1500
固体,配成溶液,滴入0.1500 的
的 溶液。实验测得消耗溶液的体积为18.00
溶液。实验测得消耗溶液的体积为18.00 ,则馏分中
,则馏分中 的质量分数为
的质量分数为_______ 。( )
)
 )是一种用途广泛的化工原料,在空气中会与
)是一种用途广泛的化工原料,在空气中会与 反应产生烟雾。利用尿素制备
反应产生烟雾。利用尿素制备 的实验流程如下图所示:
的实验流程如下图所示:
回答下列问题:
(1)步骤Ⅰ制备
 溶液的离子方程式为
溶液的离子方程式为(2)由步骤Ⅱ和步骤Ⅲ获得
 的装置如图1所示,反应原理为:
的装置如图1所示,反应原理为:


①仪器X的名称为
②
 的电子式为
的电子式为③反应过程中,如果分液漏斗中溶液滴速过快,部分
 与
与 反应产生大量氮气,该化学反应方程式为
反应产生大量氮气,该化学反应方程式为④蒸馏获得水合肼粗品后,剩余溶液进一步处理还可获得副产品
 和
和 ,
, 和
和 的溶解度曲线如图2所示。获得
的溶解度曲线如图2所示。获得 粗品的操作是蒸发结晶、
粗品的操作是蒸发结晶、
(3)馏分中水合肼含量的测定方法:称取馏分0.2500g,加入适量
 固体,配成溶液,滴入0.1500
固体,配成溶液,滴入0.1500 的
的 溶液。实验测得消耗溶液的体积为18.00
溶液。实验测得消耗溶液的体积为18.00 ,则馏分中
,则馏分中 的质量分数为
的质量分数为 )
)
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
【推荐1】硫酸羟胺 为无色晶体,易溶于水,是一种重要的化工原料,在农药、医药行业中有广泛用途。合成硫酸羟胺的流程如下:
为无色晶体,易溶于水,是一种重要的化工原料,在农药、医药行业中有广泛用途。合成硫酸羟胺的流程如下:

模拟上述流程的实验装置如下(夹持装置与加热装置省略):

已知:羟胺 为白色片状晶体,易溶于水、甲醇等,受热易分解。
为白色片状晶体,易溶于水、甲醇等,受热易分解。
回答下列问题:
(1)仪器a的作用为___________ ,三颈烧瓶中的试剂是___________
(2)装置A中反应的主要化学方程式为___________ 。
(3)开始实验时,应最先打开___________ (填“ ”“
”“ ”或“
”或“ ”)。
”)。
(4)流程中步骤Ⅰ的化学方程式是___________ 。
(5)分离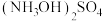 和
和 操作:①向二者混合溶液中加入氨水,生成
操作:①向二者混合溶液中加入氨水,生成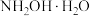 ,②再加入甲醇,加入甲醇的目的是
,②再加入甲醇,加入甲醇的目的是___________ ③过滤,将滤液进行___________ (填“常压”或“减压”)蒸馏,④接着加入硫酸,得到硫酸羟胺产品,写出发生反应的化学方程式___________
(6)测定硫酸羟胺的含量:称取一定量样品,溶于水中,移入 的三颈烧瓶中,加入足量硫酸铁溶液,充分反应后,煮沸
的三颈烧瓶中,加入足量硫酸铁溶液,充分反应后,煮沸 ,
, 气体全部逸出。将所得溶液冷却后,用
气体全部逸出。将所得溶液冷却后,用 酸性高锰酸钾溶液滴定。则硫酸羟胺物质的量(n)与消耗高锰酸钾溶液的体积(VmL)的关系是n=
酸性高锰酸钾溶液滴定。则硫酸羟胺物质的量(n)与消耗高锰酸钾溶液的体积(VmL)的关系是n=___________ mol。
 为无色晶体,易溶于水,是一种重要的化工原料,在农药、医药行业中有广泛用途。合成硫酸羟胺的流程如下:
为无色晶体,易溶于水,是一种重要的化工原料,在农药、医药行业中有广泛用途。合成硫酸羟胺的流程如下:
模拟上述流程的实验装置如下(夹持装置与加热装置省略):

已知:羟胺
 为白色片状晶体,易溶于水、甲醇等,受热易分解。
为白色片状晶体,易溶于水、甲醇等,受热易分解。回答下列问题:
(1)仪器a的作用为
(2)装置A中反应的主要化学方程式为
(3)开始实验时,应最先打开
 ”“
”“ ”或“
”或“ ”)。
”)。(4)流程中步骤Ⅰ的化学方程式是
(5)分离
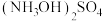 和
和 操作:①向二者混合溶液中加入氨水,生成
操作:①向二者混合溶液中加入氨水,生成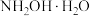 ,②再加入甲醇,加入甲醇的目的是
,②再加入甲醇,加入甲醇的目的是(6)测定硫酸羟胺的含量:称取一定量样品,溶于水中,移入
 的三颈烧瓶中,加入足量硫酸铁溶液,充分反应后,煮沸
的三颈烧瓶中,加入足量硫酸铁溶液,充分反应后,煮沸 ,
, 气体全部逸出。将所得溶液冷却后,用
气体全部逸出。将所得溶液冷却后,用 酸性高锰酸钾溶液滴定。则硫酸羟胺物质的量(n)与消耗高锰酸钾溶液的体积(VmL)的关系是n=
酸性高锰酸钾溶液滴定。则硫酸羟胺物质的量(n)与消耗高锰酸钾溶液的体积(VmL)的关系是n=
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
名校
解题方法
【推荐2】红磷可用于制备半导体化合物,还可以用于制造火柴、烟火,以及三氯化磷等。
Ⅰ.研究小组以无水甲苯为溶剂, (易水解)和
(易水解)和 (叠氮化钠)为反应物制备红磷。
(叠氮化钠)为反应物制备红磷。
实验步骤如下:
①甲苯的干燥和收集:装置如图1所示(夹持及加热装置略)
已知:二苯甲酮为指示剂,无水时体系呈蓝色,甲苯的沸点为110.6℃。 的作用是
的作用是___________ 。
(2)先小火加热控温100℃一段时间,打开活塞___________ ,达到除水的目的。再升温至120℃左右,打开活塞___________ ,达到分离收集甲苯的目的。
②红磷的制备:装置如图2所示(夹持、搅拌、加热装置已略)。___________ 。用氩气赶走空气的目的是___________ 。
(4)离心分离和洗涤得到产品,洗涤时先后使用乙醇和水,依次洗去的物质是___________ 。
Ⅱ.该实验所需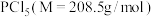 的纯度要求极高,对于的纯度测定如下:
的纯度要求极高,对于的纯度测定如下:
步骤Ⅰ:取 上述所用样品,置于盛有蒸馏水的水解瓶中摇动至完全水解,将水解液配成
上述所用样品,置于盛有蒸馏水的水解瓶中摇动至完全水解,将水解液配成 溶液;
溶液;
步骤Ⅱ:取 上述溶液于锥形瓶中,先加入足量稀硝酸,一段时间后再加入
上述溶液于锥形瓶中,先加入足量稀硝酸,一段时间后再加入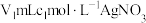 溶液(过量),使
溶液(过量),使 完全转化为
完全转化为 沉淀(
沉淀( 可溶于稀硝酸);
可溶于稀硝酸);
步骤Ⅲ:加入少量硝基苯,振荡,使沉淀表面被有机物覆盖。以硫酸铁溶液为指示剂,用 溶液滴定过量的
溶液滴定过量的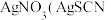 难溶于水),达到滴定终点时,共用去
难溶于水),达到滴定终点时,共用去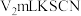 溶液。
溶液。
(5)产品中 的质量分数为
的质量分数为___________  ,若测定过程中没有加入硝基苯,则所测
,若测定过程中没有加入硝基苯,则所测 的含量会
的含量会___________ (填“偏大”“偏小”或“不变”)。
Ⅰ.研究小组以无水甲苯为溶剂,
 (易水解)和
(易水解)和 (叠氮化钠)为反应物制备红磷。
(叠氮化钠)为反应物制备红磷。实验步骤如下:
①甲苯的干燥和收集:装置如图1所示(夹持及加热装置略)
已知:二苯甲酮为指示剂,无水时体系呈蓝色,甲苯的沸点为110.6℃。
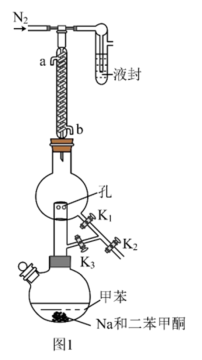
 的作用是
的作用是(2)先小火加热控温100℃一段时间,打开活塞
②红磷的制备:装置如图2所示(夹持、搅拌、加热装置已略)。
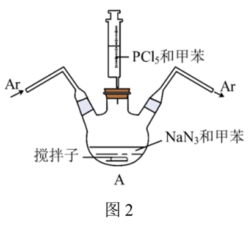
(4)离心分离和洗涤得到产品,洗涤时先后使用乙醇和水,依次洗去的物质是
Ⅱ.该实验所需
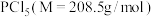 的纯度要求极高,对于的纯度测定如下:
的纯度要求极高,对于的纯度测定如下:步骤Ⅰ:取
 上述所用样品,置于盛有蒸馏水的水解瓶中摇动至完全水解,将水解液配成
上述所用样品,置于盛有蒸馏水的水解瓶中摇动至完全水解,将水解液配成 溶液;
溶液;步骤Ⅱ:取
 上述溶液于锥形瓶中,先加入足量稀硝酸,一段时间后再加入
上述溶液于锥形瓶中,先加入足量稀硝酸,一段时间后再加入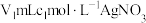 溶液(过量),使
溶液(过量),使 完全转化为
完全转化为 沉淀(
沉淀( 可溶于稀硝酸);
可溶于稀硝酸);步骤Ⅲ:加入少量硝基苯,振荡,使沉淀表面被有机物覆盖。以硫酸铁溶液为指示剂,用
 溶液滴定过量的
溶液滴定过量的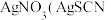 难溶于水),达到滴定终点时,共用去
难溶于水),达到滴定终点时,共用去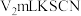 溶液。
溶液。(5)产品中
 的质量分数为
的质量分数为 ,若测定过程中没有加入硝基苯,则所测
,若测定过程中没有加入硝基苯,则所测 的含量会
的含量会
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
名校
解题方法
【推荐3】六聚偏磷酸钠[(NaPO3)6]是偏磷酸钠(NaPO3)的一种聚合体,其主要用于水处理、造纸、食品行业。工业上由Ca3(PO4)2、焦炭、石英砂为原料制备六偏磷酸钠的方法如下:
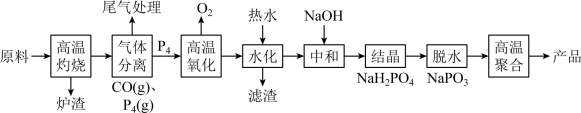
回答下列问题:
(1)“高温灼烧”发生反应的化学方程式是___________ 。
(2)因白磷(P4)易自燃,通常保存在冷水中,在“气体分离”环节中得到白磷固体比较合理的操作是___________ 。
(3)经分析,所得到的白磷中含有相对较多的Pb和含量相对少量的As元素。在“高温氧化”时As、Pb会被氧化成As2O5、PbO,随后在“水化”(产物是H3PO4)过程中转化为两种难溶性盐被除去,则两种滤渣的主要成分是___________ 、___________ (填化学式)。
(4)已知室温下H3PO4的Ka1=7.5×10-3、Ka2=6.4×10-8、Ka3=4.4×10-13,且lg3.2=0.5。
①若直接将白磷与足量NaOH溶液直接混合加热,则得到的是次磷酸钠(NaH2PO2),但同时会得到一种剧毒气体(PH3),写出该化学方程式___________ 。
②欲得到室温下0.5mol/LNaH2PO4溶液,则“中和”时需加适量NaOH固体调溶液pH约为_________ (结果保留两位小数)。
(5)将白磷的氧化产物(P4O10)与纯碱混合加热是工业上制备偏磷酸钠的另一种方法,该方法的化学方程式是___________ 。

回答下列问题:
(1)“高温灼烧”发生反应的化学方程式是
(2)因白磷(P4)易自燃,通常保存在冷水中,在“气体分离”环节中得到白磷固体比较合理的操作是
(3)经分析,所得到的白磷中含有相对较多的Pb和含量相对少量的As元素。在“高温氧化”时As、Pb会被氧化成As2O5、PbO,随后在“水化”(产物是H3PO4)过程中转化为两种难溶性盐被除去,则两种滤渣的主要成分是
(4)已知室温下H3PO4的Ka1=7.5×10-3、Ka2=6.4×10-8、Ka3=4.4×10-13,且lg3.2=0.5。
①若直接将白磷与足量NaOH溶液直接混合加热,则得到的是次磷酸钠(NaH2PO2),但同时会得到一种剧毒气体(PH3),写出该化学方程式
②欲得到室温下0.5mol/LNaH2PO4溶液,则“中和”时需加适量NaOH固体调溶液pH约为
(5)将白磷的氧化产物(P4O10)与纯碱混合加热是工业上制备偏磷酸钠的另一种方法,该方法的化学方程式是
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
【推荐1】已知A~K所代表的各物质都是中学化学里常见的物质,且I是具有磁性的物质,D和K都具有两性。一定条件下,各物质间的相互反应转化关系如下图所示:

请回答:
(1)写出有关物质化学式:D是__________ ,H是__________ 。
(2)写出下列反应的方程式:
①化合物G的溶液呈__________ (酸性,碱性,中性),其原因用离子方程式表示为__________
②写出C+F H+I的化学方程式并用单线桥表示反应过程中电子转移的方向和数目
H+I的化学方程式并用单线桥表示反应过程中电子转移的方向和数目________ 。
③G+J K用离子方程式表示为
K用离子方程式表示为____________ 。

请回答:
(1)写出有关物质化学式:D是
(2)写出下列反应的方程式:
①化合物G的溶液呈
②写出C+F
 H+I的化学方程式并用单线桥表示反应过程中电子转移的方向和数目
H+I的化学方程式并用单线桥表示反应过程中电子转移的方向和数目③G+J
 K用离子方程式表示为
K用离子方程式表示为
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
【推荐2】钒和五氧化二钒在工业应用中广泛,某工厂从钒渣中回收金属,钒渣中主要成分有V2O3、FeO,还含有少量的CuO、Al2O3,工艺流程如图:
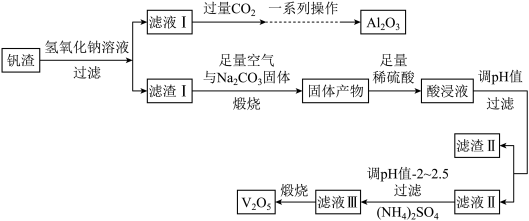
已知:①KspCu(OH)2=1.0×10−21;KspFe(OH)3=4.0×10−38;KspFe(OH)2=8.0×10−16。
②NH4VO3难溶于水,(VO2)2SO4易溶于水。
(1)写出滤液I中加入过量的CO2时发生反应的离子方程式;制取纯净的Al2O3需要经过一系列操作:过滤、___ 、___ 。
(2)煅烧时,滤渣I的主要成分V2O3转化为可溶性NaVO3,写出其反应的化学方程式___ 。
(3)加入稀硫酸后,酸浸液中VO3−与VO2+能大量共存的原因是___ (用离子方程式解释)。
(4)常温下调节酸浸液的pH=___ ,即可以完全除去铁、铜两种元素对应的离子___ ;实际pH值要调整到8,其目的是___ ;调pH=2~2.5后过滤,滤渣III的主要成分为___ 。
(5)请写出煅烧滤渣III时,发生反应的化学方程式___ 。

已知:①KspCu(OH)2=1.0×10−21;KspFe(OH)3=4.0×10−38;KspFe(OH)2=8.0×10−16。
②NH4VO3难溶于水,(VO2)2SO4易溶于水。
(1)写出滤液I中加入过量的CO2时发生反应的离子方程式;制取纯净的Al2O3需要经过一系列操作:过滤、
(2)煅烧时,滤渣I的主要成分V2O3转化为可溶性NaVO3,写出其反应的化学方程式
(3)加入稀硫酸后,酸浸液中VO3−与VO2+能大量共存的原因是
(4)常温下调节酸浸液的pH=
(5)请写出煅烧滤渣III时,发生反应的化学方程式
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
名校
解题方法
【推荐3】化合物 是一种由三种元素组成的重要化工原料,其
是一种由三种元素组成的重要化工原料,其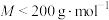 ,进行如图所示操作,已知
,进行如图所示操作,已知 、
、 含有一种相同的元素且在常温下均为气态化合物,其中气体
含有一种相同的元素且在常温下均为气态化合物,其中气体 可使品红溶液褪色(部分反应条件省略)。请回答:
可使品红溶液褪色(部分反应条件省略)。请回答:
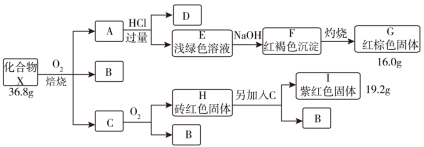
(1)组成 的元素有
的元素有___________ ,化合物 的化学式是
的化学式是___________ 。
(2)溶液 中溶质的主要成分是
中溶质的主要成分是___________ (用化学式表示)。
(3)写出 与
与 反应生成
反应生成 、
、 、
、 的化学方程式:
的化学方程式:___________ 。
(4)写出 与
与 反应生成
反应生成 和
和 的化学方程式:
的化学方程式:___________ 。
(5)请设计实验确定气体 的成分:
的成分:___________ 。
 是一种由三种元素组成的重要化工原料,其
是一种由三种元素组成的重要化工原料,其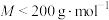 ,进行如图所示操作,已知
,进行如图所示操作,已知 、
、 含有一种相同的元素且在常温下均为气态化合物,其中气体
含有一种相同的元素且在常温下均为气态化合物,其中气体 可使品红溶液褪色(部分反应条件省略)。请回答:
可使品红溶液褪色(部分反应条件省略)。请回答:
(1)组成
 的元素有
的元素有 的化学式是
的化学式是(2)溶液
 中溶质的主要成分是
中溶质的主要成分是(3)写出
 与
与 反应生成
反应生成 、
、 、
、 的化学方程式:
的化学方程式:(4)写出
 与
与 反应生成
反应生成 和
和 的化学方程式:
的化学方程式:(5)请设计实验确定气体
 的成分:
的成分:
您最近一年使用:0次



