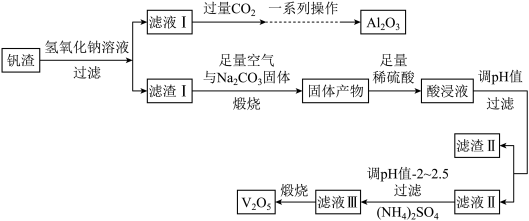
钒和五氧化二钒在工业应用中广泛,某工厂从钒渣中回收金属,钒渣中主要成分有V2O3、FeO,还含有少量的CuO、Al2O3,工艺流程如图:
已知:①KspCu(OH)2=1.0×10−21;KspFe(OH)3=4.0×10−38;KspFe(OH)2=8.0×10−16。
②NH4VO3难溶于水,(VO2)2SO4易溶于水。
(1)写出滤液I中加入过量的CO2时发生反应的离子方程式;制取纯净的Al2O3需要经过一系列操作:过滤、___ 、___ 。
(2)煅烧时,滤渣I的主要成分V2O3转化为可溶性NaVO3,写出其反应的化学方程式___ 。
(3)加入稀硫酸后,酸浸液中VO3−与VO2+能大量共存的原因是___ (用离子方程式解释)。
(4)常温下调节酸浸液的pH=___ ,即可以完全除去铁、铜两种元素对应的离子___ ;实际pH值要调整到8,其目的是___ ;调pH=2~2.5后过滤,滤渣III的主要成分为___ 。
(5)请写出煅烧滤渣III时,发生反应的化学方程式___ 。

已知:①KspCu(OH)2=1.0×10−21;KspFe(OH)3=4.0×10−38;KspFe(OH)2=8.0×10−16。
②NH4VO3难溶于水,(VO2)2SO4易溶于水。
(1)写出滤液I中加入过量的CO2时发生反应的离子方程式;制取纯净的Al2O3需要经过一系列操作:过滤、
(2)煅烧时,滤渣I的主要成分V2O3转化为可溶性NaVO3,写出其反应的化学方程式
(3)加入稀硫酸后,酸浸液中VO3−与VO2+能大量共存的原因是
(4)常温下调节酸浸液的pH=
(5)请写出煅烧滤渣III时,发生反应的化学方程式
更新时间:2020-05-10 15:37:35
|
相似题推荐
解答题-无机推断题
|
较难
(0.4)
名校
解题方法
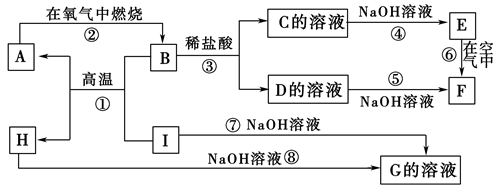
【推荐1】A~I分别表示中学化学中常见的一种物质,它们之间相互关系如下图所示(部分反应物、生成物没有列出)。已知H为固态氧化物,F是红褐色难溶于水的沉淀,且A、B、C、D、E、F六种物质中均含同一种元素。
请填写下列空白:
(1)A、B、C、D、E、F六种物质中所含的同一种元素的名称是________ 。
(2)反应①的化学方程式为_____________________________________
反应③的离子方程式为________________________
反应⑧的化学方程式为_____________________________________
(3)反应⑥过程中的现象是______________________________ 。
(4)1molI发生反应后生成的A高温下与足量的水蒸气反应,生成的气体换算成标准状况下占______ L。

请填写下列空白:
(1)A、B、C、D、E、F六种物质中所含的同一种元素的名称是
(2)反应①的化学方程式为
反应③的离子方程式为
反应⑧的化学方程式为
(3)反应⑥过程中的现象是
(4)1molI发生反应后生成的A高温下与足量的水蒸气反应,生成的气体换算成标准状况下占
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
解题方法
【推荐2】根据下列框图回答问题:
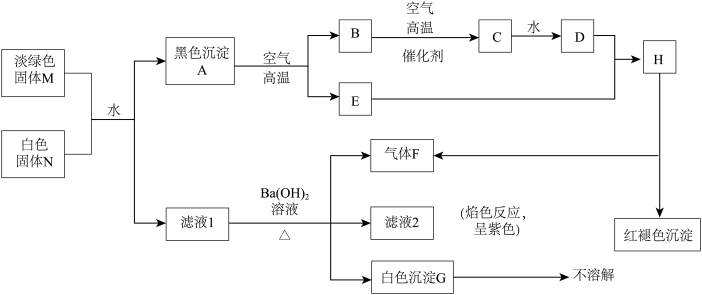
已知白色固体N中阴、阳离子具有相同的核外电子层结构。
(1)写出M中存在的离子:_____________________________________________
(2)请写出M与N反应的离子方程式:_____________________ 。
(3)写出A在空气中煅烧的化学方程式:____________________ 。
(4)某同学取H的溶液,通入气体B,所得溶液中仍只有一种阴离子。请写出上
述变化过程中的离子方程式_____________________ 。

已知白色固体N中阴、阳离子具有相同的核外电子层结构。
(1)写出M中存在的离子:
(2)请写出M与N反应的离子方程式:
(3)写出A在空气中煅烧的化学方程式:
(4)某同学取H的溶液,通入气体B,所得溶液中仍只有一种阴离子。请写出上
述变化过程中的离子方程式
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
名校
解题方法
【推荐3】下图中A~H均为中学化学中常见的物质,A、B、H是气体,A是有刺激性气味的气体,B、H是无色无味气体,它们之间有如下转化关系。(反应中生成的水已略去)

请回答以下问题:
(1)E是___________ (填化学式)。
(2)C物质在日常生活中可作___________ 剂。
(3)写出反应①的化学方程式:___________ 。写出反应④的化学方程式:___________ 。
(4)写出工业制取A气体的化学反应方程式:___________ 。

请回答以下问题:
(1)E是
(2)C物质在日常生活中可作
(3)写出反应①的化学方程式:
(4)写出工业制取A气体的化学反应方程式:
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
名校
【推荐1】六氟锑酸钠( )广泛用于有机合成、光化学反应中的催化剂、蚀刻剂及医药中间体,一种由锑矿粉(主要含
)广泛用于有机合成、光化学反应中的催化剂、蚀刻剂及医药中间体,一种由锑矿粉(主要含 、
、 ,还含有少量
,还含有少量 、
、 、
、 等)合成六氟锑酸钠的工艺流程如图所示:
等)合成六氟锑酸钠的工艺流程如图所示:
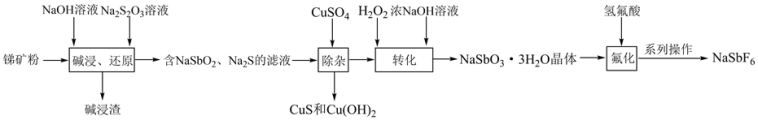
已知:①Sb的氧化物及氢氧化物的性质与Al的类似; 可溶于NaOH溶液。
可溶于NaOH溶液。
②常温下, 、
、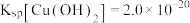 。
。
③ 难溶于水。
难溶于水。
请回答下列问题:
(1) 中Sb的化合价为
中Sb的化合价为_______ 。
(2)“碱浸”时,若 转化为
转化为 ,则
,则 与
与 反应的离子方程式为
反应的离子方程式为_______ 。
(3)“碱浸渣”的主要成分为_______ (填化学式)。
(4)“除杂”时,当溶液中出现蓝色沉淀,停止加入 溶液,测得此时溶液的
溶液,测得此时溶液的 ,则此时溶液中残留的
,则此时溶液中残留的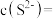
_______ 。
(5)“转化”过程中需先向溶液中加入浓NaOH溶液,加热至适当温度后,慢慢滴入30% 溶液进行氧化回流。则“转化”步骤发生反应的化学方程式为
溶液进行氧化回流。则“转化”步骤发生反应的化学方程式为_______ 。
(6)已知“系列操作”为蒸发浓缩、冷却结晶、过滤、洗涤、干燥,则“氟化”时发生反应的离子方程式为_______ 。
(7)以六氟锑酸钠为离子导体的新型钠离子可充电电池的结构如图,该电池放电时的工作原理为 ,则充电时,
,则充电时, 向
向_______ 移动(填“左”或“右”);放电时,石墨电极上的电极反应式为_______ 。

 )广泛用于有机合成、光化学反应中的催化剂、蚀刻剂及医药中间体,一种由锑矿粉(主要含
)广泛用于有机合成、光化学反应中的催化剂、蚀刻剂及医药中间体,一种由锑矿粉(主要含 、
、 ,还含有少量
,还含有少量 、
、 、
、 等)合成六氟锑酸钠的工艺流程如图所示:
等)合成六氟锑酸钠的工艺流程如图所示:
已知:①Sb的氧化物及氢氧化物的性质与Al的类似;
 可溶于NaOH溶液。
可溶于NaOH溶液。②常温下,
 、
、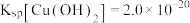 。
。③
 难溶于水。
难溶于水。请回答下列问题:
(1)
 中Sb的化合价为
中Sb的化合价为(2)“碱浸”时,若
 转化为
转化为 ,则
,则 与
与 反应的离子方程式为
反应的离子方程式为(3)“碱浸渣”的主要成分为
(4)“除杂”时,当溶液中出现蓝色沉淀,停止加入
 溶液,测得此时溶液的
溶液,测得此时溶液的 ,则此时溶液中残留的
,则此时溶液中残留的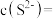
(5)“转化”过程中需先向溶液中加入浓NaOH溶液,加热至适当温度后,慢慢滴入30%
 溶液进行氧化回流。则“转化”步骤发生反应的化学方程式为
溶液进行氧化回流。则“转化”步骤发生反应的化学方程式为(6)已知“系列操作”为蒸发浓缩、冷却结晶、过滤、洗涤、干燥,则“氟化”时发生反应的离子方程式为
(7)以六氟锑酸钠为离子导体的新型钠离子可充电电池的结构如图,该电池放电时的工作原理为
 ,则充电时,
,则充电时, 向
向
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
解题方法
【推荐2】铍是火箭、导弹、航空以及冶金工业中不可缺少的宝贵材料。以绿柱石[Be3Al2(SiO3)6]为原料制备两性金属铍的工艺流程如图所示。

回答下列问题:
(1)绿柱石中Be的化合价为_______ 。
(2)750℃烧结时,Na3FeF6仅与绿柱若中BeO作用生成易溶于水的Na2BeF4,则滤渣的主要成分是Fe2O3和_______ 。
(3)“水浸”时“粉碎”的目的是_______ 。
(4)加适量氢氧化钠溶液使铍元素完全转化为氢氧化铍沉淀,已知25℃时Ksp[Be(OH)2]=4×10-22,计算25℃时,饱和氢氧化铍溶液的pH=_______ (可用对数表示),“沉氟”的化学方程式为_______ 。
(5)镍作阴极、石墨作阳极,350~400℃电解NaCl—BeCl2熔融混合物得到金属铍,阳极反应式为_______ ;不能用该电解槽电解熔融氯化铍制金属铍的原因可能是_______ 。

回答下列问题:
(1)绿柱石中Be的化合价为
(2)750℃烧结时,Na3FeF6仅与绿柱若中BeO作用生成易溶于水的Na2BeF4,则滤渣的主要成分是Fe2O3和
(3)“水浸”时“粉碎”的目的是
(4)加适量氢氧化钠溶液使铍元素完全转化为氢氧化铍沉淀,已知25℃时Ksp[Be(OH)2]=4×10-22,计算25℃时,饱和氢氧化铍溶液的pH=
(5)镍作阴极、石墨作阳极,350~400℃电解NaCl—BeCl2熔融混合物得到金属铍,阳极反应式为
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
【推荐3】已知25℃时草酸(H2C2O4)的电离常数为K1=5.0×10-2,K2=5.4×10-5,草酸钙的Ksp=4.0×10-8,碳酸钙的Ksp=2.5×10-9。不同温度下水的离子积常数见下表:
(1)常温下将0.2 mol/L的KOH溶液20 mL与0.2 mol/L的草酸溶液20 mL混合后溶液显酸性,则混合后溶液中各离子浓度的大小顺序为__________________________________ ;
(2)已知草酸能使酸性高锰酸钾溶液(稀硫酸酸化)褪色,试写出反应的离子方程式:________________________________ 。若在锥形瓶中放入20.00mL未知浓度的草酸,用0.1mol/L高锰酸钾溶液滴定,当到达滴定终点时,溶液颜色的变化是___________________________________________________ ;若共消耗VmL高锰酸钾溶液,则草酸的物质的量浓度为__________ mol/L。
(3)90℃时,将0.005 mol/L的氢氧化钙溶液20 mL与0.0012 mol/L的草酸溶液20 mL混合,混合后溶液的pH=___________ ;
(4)25℃时若向20 mL草酸钙的饱和溶液中逐滴加入8.0×10-4 mol/L的碳酸钾溶液10 mL,能否产生沉淀,___________ (填“能”或“否”)。
| t/℃ | 0 | 10 | 20 | 25 | 40 | 50 | 90 | 100 |
| Kw/10-14 | 0.134 | 0.292 | 0.681 | 1.00 | 2.92 | 5.57 | 38.0 | 55.0 |
(1)常温下将0.2 mol/L的KOH溶液20 mL与0.2 mol/L的草酸溶液20 mL混合后溶液显酸性,则混合后溶液中各离子浓度的大小顺序为
(2)已知草酸能使酸性高锰酸钾溶液(稀硫酸酸化)褪色,试写出反应的离子方程式:
(3)90℃时,将0.005 mol/L的氢氧化钙溶液20 mL与0.0012 mol/L的草酸溶液20 mL混合,混合后溶液的pH=
(4)25℃时若向20 mL草酸钙的饱和溶液中逐滴加入8.0×10-4 mol/L的碳酸钾溶液10 mL,能否产生沉淀,
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
名校
【推荐1】某大型企业以工业烧渣(主要含ZnO,还含少量Fe3O4、Al2O3、CuO及SiO2等)为原料制取有机高分子材料的阻燃剂——磷酸锌[Zn3(PO4)2]的工艺流程如图所示。

已知:室温下,几种金属离子开始沉淀与沉淀完全的pH如下表所示。
(1)在180 °C对“烧渣灰”进行酸溶最适合的酸是_______ (填“盐酸”、“硫酸”或“硝酸”)。
(2)加入双氧水的作用是作氧化剂,则发生反应的离子方程式为_______ ;可用NaClO代替双氧水,两者相比,_______ (填化学式)的氧化效率更高。(氧化效率以单位质量的氧化剂得到的电子数表示)
(3)加氨水过程中加热的目的是_______ ;“过滤2”得到的滤渣的主要成分为_______ (填化学式)。
(4)通入H2S的目的是_______ ;加入Na2 HPO4发生反应的离子方程式为_______ 。
(5)确认磷酸锌洗涤干净的操作是_______ 。
(6)在通入H2S之前,“溶液3”中A13+的浓度为_______ mol·L-1。

已知:室温下,几种金属离子开始沉淀与沉淀完全的pH如下表所示。
| 金属离子 | Al3+ | Fe3+ | Cu2+ | Zn2+ |
| 开始沉淀的pH | 3.7 | 2.2 | 5.2 | 6.5 |
| 沉淀完全(c=1.0×10-5mol· L-1)的pH | 4.2 | 3.2 | 6.7 | 8.0 |
(2)加入双氧水的作用是作氧化剂,则发生反应的离子方程式为
(3)加氨水过程中加热的目的是
(4)通入H2S的目的是
(5)确认磷酸锌洗涤干净的操作是
(6)在通入H2S之前,“溶液3”中A13+的浓度为
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
【推荐2】铍有“超级金属”之称。以绿柱石 为原料制备金属铍的工艺如下:
为原料制备金属铍的工艺如下:
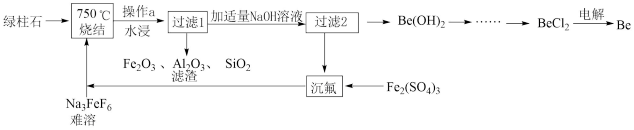
已知 可与
可与 、
、 结合成配位数为4的配离子。回答下列问题:
结合成配位数为4的配离子。回答下列问题:
(1)烧结冷却后,水浸之前“操作a”的名称是___ 。
(2)750℃烧结时,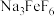 与绿柱石作用生成易溶于水的
与绿柱石作用生成易溶于水的 ,写出该反应的化学方程式
,写出该反应的化学方程式___ 。
(3)已知25℃时 ,计算室温时
,计算室温时 开始沉淀时的pH=
开始沉淀时的pH=__ ,“沉氟”反应的离子方程式为_ 。
(4)上述流程中,“ ”可有两种方案:
”可有两种方案:
I: 溶液A
溶液A
II:
I中操作b是___ 。II中 转化为
转化为 的化学方程式为
的化学方程式为___ 。
(5) 在气态时常以二聚体形式存在,此二聚体分子的结构式为
在气态时常以二聚体形式存在,此二聚体分子的结构式为__ ;工业上电解 与
与 熔融体制得金属铍,
熔融体制得金属铍, 的作用是
的作用是___ ,阴极反应式为__ 。
 为原料制备金属铍的工艺如下:
为原料制备金属铍的工艺如下:
已知
 可与
可与 、
、 结合成配位数为4的配离子。回答下列问题:
结合成配位数为4的配离子。回答下列问题:(1)烧结冷却后,水浸之前“操作a”的名称是
(2)750℃烧结时,
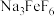 与绿柱石作用生成易溶于水的
与绿柱石作用生成易溶于水的 ,写出该反应的化学方程式
,写出该反应的化学方程式(3)已知25℃时
 ,计算室温时
,计算室温时 开始沉淀时的pH=
开始沉淀时的pH=(4)上述流程中,“
 ”可有两种方案:
”可有两种方案:I:
 溶液A
溶液A
II:

I中操作b是
 转化为
转化为 的化学方程式为
的化学方程式为(5)
 在气态时常以二聚体形式存在,此二聚体分子的结构式为
在气态时常以二聚体形式存在,此二聚体分子的结构式为 与
与 熔融体制得金属铍,
熔融体制得金属铍, 的作用是
的作用是
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
名校
【推荐3】 常用作制革工业的鞣革剂,工业上以铬铁矿(主要成分为
常用作制革工业的鞣革剂,工业上以铬铁矿(主要成分为 ,含
,含 、
、 氧化物等杂质)为主要原料制备
氧化物等杂质)为主要原料制备 的工艺流程如图。回答下列问题:
的工艺流程如图。回答下列问题:
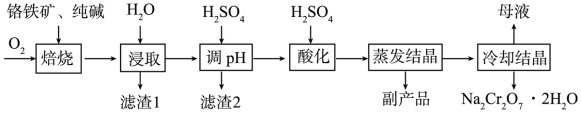
(1)铬铁矿“焙烧”前,为提高焙烧效率,可采取的措施有___________ (任写一点)。
(2)基态 原子的价电子排布式为
原子的价电子排布式为___________ 。
(3)“滤渣1”的主要成分为 等难溶于水的物质,则“滤渣2”的主要成分为
等难溶于水的物质,则“滤渣2”的主要成分为___________ (填化学式)。
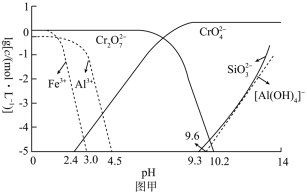
(4)已知各离子浓度的对数 与
与 的关系如图甲所示。当溶液中某种粒子浓度
的关系如图甲所示。当溶液中某种粒子浓度 时,可认为该离子已除尽,则“调
时,可认为该离子已除尽,则“调 ”时
”时 的理论范围为
的理论范围为___________ ;“酸化”的目的是___________ 。
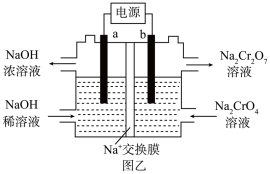
(5)利用膜电解技术,以 为主要原料制备
为主要原料制备 的工作原理如图乙所示(a、b电极材料均为石墨):a极与电源的
的工作原理如图乙所示(a、b电极材料均为石墨):a极与电源的___________ 极相连,制备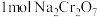 时,理论上左侧溶液总质量增重
时,理论上左侧溶液总质量增重___________ g。
(6)为了测定 产品的纯度,可采用
产品的纯度,可采用 标准溶液通过氧化还原反应滴定
标准溶液通过氧化还原反应滴定 溶液。下列关于滴定分析的操作,正确的是___________(填标号)。
溶液。下列关于滴定分析的操作,正确的是___________(填标号)。
 常用作制革工业的鞣革剂,工业上以铬铁矿(主要成分为
常用作制革工业的鞣革剂,工业上以铬铁矿(主要成分为 ,含
,含 、
、 氧化物等杂质)为主要原料制备
氧化物等杂质)为主要原料制备 的工艺流程如图。回答下列问题:
的工艺流程如图。回答下列问题:
(1)铬铁矿“焙烧”前,为提高焙烧效率,可采取的措施有
(2)基态
 原子的价电子排布式为
原子的价电子排布式为(3)“滤渣1”的主要成分为
 等难溶于水的物质,则“滤渣2”的主要成分为
等难溶于水的物质,则“滤渣2”的主要成分为(4)已知各离子浓度的对数
 与
与 的关系如图甲所示。当溶液中某种粒子浓度
的关系如图甲所示。当溶液中某种粒子浓度 时,可认为该离子已除尽,则“调
时,可认为该离子已除尽,则“调 ”时
”时 的理论范围为
的理论范围为

(5)利用膜电解技术,以
 为主要原料制备
为主要原料制备 的工作原理如图乙所示(a、b电极材料均为石墨):a极与电源的
的工作原理如图乙所示(a、b电极材料均为石墨):a极与电源的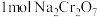 时,理论上左侧溶液总质量增重
时,理论上左侧溶液总质量增重(6)为了测定
 产品的纯度,可采用
产品的纯度,可采用 标准溶液通过氧化还原反应滴定
标准溶液通过氧化还原反应滴定 溶液。下列关于滴定分析的操作,正确的是___________(填标号)。
溶液。下列关于滴定分析的操作,正确的是___________(填标号)。A.用移液管量取 待测液转移至锥形瓶中 待测液转移至锥形瓶中 |
| B.滴定开始时可以让液体成线状快速流下,接近滴定终点时减慢滴加速率,必要时采用半滴操作 |
| C.排气泡时应使管尖弯曲向上,用右手挤压玻璃珠上方,使液体充满管尖 |
| D.读数时应将滴定管从架上取下,捏住管上端无刻度处,使滴定管保持垂直 |
您最近一年使用:0次



