钾是活泼的碱金属,钾和氧有氧化钾(K2O)、过氧化钾(K2O2)和超氧化钾(KO2)等多种化合物。
⑴钾和硝酸钾反应可制得氧化钾:K+KNO3→K2O+N2(未配平),每生成9.4gK2O消耗的还原剂有___________ g
⑵超氧化钾和过氧化钾都能与二氧化碳反应均生成氧气和K2CO3,在医院、矿井、潜水、高空飞行中用作供氧剂。写出超氧化钾与二氧化碳反应的化学方程式______________________ ,为了维持气压稳定,可以使用超氧化钾和过氧化钾的混合物使吸收的CO2与生成的O2体积相同(同温同压),则它们的物质的量之比为n(KO2) :n(K2O2)=____________
⑶KO2加热至600℃部分分解得到产物A。6.30g产物A充分吸收二氧化碳生成碳酸钾并产生氧气1.12L(标准状况),试确定产物A中钾氧两种原子个数之比_______ 。如果产物A只含有两种化合物,写出所有可能的化学式并计算A中两种化合物的物质的量之比_______ 。
⑴钾和硝酸钾反应可制得氧化钾:K+KNO3→K2O+N2(未配平),每生成9.4gK2O消耗的还原剂有
⑵超氧化钾和过氧化钾都能与二氧化碳反应均生成氧气和K2CO3,在医院、矿井、潜水、高空飞行中用作供氧剂。写出超氧化钾与二氧化碳反应的化学方程式
⑶KO2加热至600℃部分分解得到产物A。6.30g产物A充分吸收二氧化碳生成碳酸钾并产生氧气1.12L(标准状况),试确定产物A中钾氧两种原子个数之比
2011·上海长宁·二模 查看更多[2]
更新时间:2011-04-27 11:32:58
|
相似题推荐
计算题
|
适中
(0.65)
名校
【推荐1】同温同压下,A2气体与B2气体等体积化合,生成AxBy气体,已知反应前后气体的密度不变,则x=______ ,y=______ 。你的推理依据是_________ 。
您最近一年使用:0次
计算题
|
适中
(0.65)
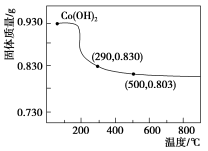
【推荐2】在空气中加热Co(OH)2,使其转化为钴的氧化物。加热过程中,固体质量与温度的关系如图所示。290~500℃,发生反应的化学方程式为___ 。

您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐3】(1)2molO3和3molO2的质量之比为____ ,分子数之比为____ ;同温同压下的密度之比为____ ,含氧原子数之比为_____ ,体积之比为____ 。
(2)气体化合物A的化学式可表示为OxFy,已知同温同压下10mLA受热分解生成15mLO2和10mLF2,则A的化学式为____ ,推断的依据是____ 。
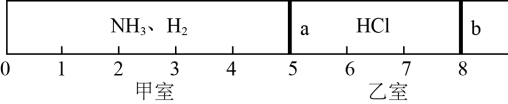
(3)标准状况下,在乙室中充入1.2molHCl,甲室中充入NH3、H2的混合气体,静止时活塞如图。已知甲室中气体的质量比乙室中气体的质量少33.8g。
请回答下列问题:
①甲室中气体的物质的量为____ mol。
②甲室中气体的质量为____ g。
③甲室中NH3、H2的物质的量之比为___ ,质量之比为____ 。
④如果将活塞a去掉,当HCl与NH3完全反应后,活塞b将静止于刻度“____ ”(填数字)处。
(2)气体化合物A的化学式可表示为OxFy,已知同温同压下10mLA受热分解生成15mLO2和10mLF2,则A的化学式为
(3)标准状况下,在乙室中充入1.2molHCl,甲室中充入NH3、H2的混合气体,静止时活塞如图。已知甲室中气体的质量比乙室中气体的质量少33.8g。

请回答下列问题:
①甲室中气体的物质的量为
②甲室中气体的质量为
③甲室中NH3、H2的物质的量之比为
④如果将活塞a去掉,当HCl与NH3完全反应后,活塞b将静止于刻度“
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐1】一定量的炭粉与足量18mol/L的浓硫酸充分反应。如果该反应过程中转移了0.2mol电子,试求反应中生成的气体在标准状况下的体积。____________________
您最近一年使用:0次
【推荐2】氧化还原反应对我们的生产和生活同时具有正负两方面的影响,如果我们能够掌握化学变化的规律,就有可能做到趋利避害,使之更好地为社会发展服务。下面我们逐一分析:
(1)黑火药是我国古代的四大发明之一,黑火药着火时,发生如下氧化还原反应: 。在此反应中,还原剂为
。在此反应中,还原剂为_______ (填化学式),还原产物是_______ (填化学式),当该反应转移2.4mol电子时,产生气体的体积为_______ L(标况下)。
(2)湿法制备高铁酸钾 是在碱性环境中进行,反应体系中有六种反应微粒:
是在碱性环境中进行,反应体系中有六种反应微粒: 、
、 、
、 、
、 、
、 、
、 。请依据上述信息,写出并配平湿法制高铁酸钾的离子方程式:
。请依据上述信息,写出并配平湿法制高铁酸钾的离子方程式:_______ 。
(3)汽车剧烈碰撞时,安全气囊中发生反应: 。若反应得到的氧化产物比还原产物多2.8mol,则此过程中转移电子的个数为
。若反应得到的氧化产物比还原产物多2.8mol,则此过程中转移电子的个数为_______ 。
(4)在第一次世界大战期间,德军在比利时的伊普雷战役中使用了氯气制造的毒气弹。现代工业常用氯气制备漂白粉、消毒液等物质。写出制备漂白粉的化学反应方程式_______ 。
(1)黑火药是我国古代的四大发明之一,黑火药着火时,发生如下氧化还原反应:
 。在此反应中,还原剂为
。在此反应中,还原剂为(2)湿法制备高铁酸钾
 是在碱性环境中进行,反应体系中有六种反应微粒:
是在碱性环境中进行,反应体系中有六种反应微粒: 、
、 、
、 、
、 、
、 、
、 。请依据上述信息,写出并配平湿法制高铁酸钾的离子方程式:
。请依据上述信息,写出并配平湿法制高铁酸钾的离子方程式:(3)汽车剧烈碰撞时,安全气囊中发生反应:
 。若反应得到的氧化产物比还原产物多2.8mol,则此过程中转移电子的个数为
。若反应得到的氧化产物比还原产物多2.8mol,则此过程中转移电子的个数为(4)在第一次世界大战期间,德军在比利时的伊普雷战役中使用了氯气制造的毒气弹。现代工业常用氯气制备漂白粉、消毒液等物质。写出制备漂白粉的化学反应方程式
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐3】2.0g Cu2S和CuS的混合物在酸性溶液中用400 mL 0.075 mol·L-1KMnO4溶液处理,发生反应如下:
8MnO4-+5Cu2S+44H+ =10Cu2++5SO2+8Mn2++22H2O
6MnO4-+5CuS+28H+ =5Cu2++5SO2+6Mn2++14H2O
(1)上述两个反应具有完全相同的_____________ (可多选)
A.氧化剂 B.还原剂 C.氧化产物 D.还原产物
(2)反应后煮沸溶液,赶尽SO2,剩余的KMnO4恰好与350 mL 0.10 mol/L(NH4)2Fe(SO4)2溶液完全反应。配平KMnO4与(NH4)2Fe(SO4)2反应的离子方程式:
____ MnO4- +___ Fe2++___ H+——___ Mn2++___ Fe3++ ___ ___
KMnO4溶液与混合物反应后,剩余KMnO4的物质的量为_________ mol。
(3)混合物中Cu2S的质量分数为_________ %。(写出解题过程)
8MnO4-+5Cu2S+44H+ =10Cu2++5SO2+8Mn2++22H2O
6MnO4-+5CuS+28H+ =5Cu2++5SO2+6Mn2++14H2O
(1)上述两个反应具有完全相同的
A.氧化剂 B.还原剂 C.氧化产物 D.还原产物
(2)反应后煮沸溶液,赶尽SO2,剩余的KMnO4恰好与350 mL 0.10 mol/L(NH4)2Fe(SO4)2溶液完全反应。配平KMnO4与(NH4)2Fe(SO4)2反应的离子方程式:
KMnO4溶液与混合物反应后,剩余KMnO4的物质的量为
(3)混合物中Cu2S的质量分数为
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐1】配平并完成方程式。
(1)_____ Pt+ _____ HNO3+ _____ HCl
_____ H2PtCl6+_____ NO↑+_____ ( )
(2)_____ Fe+ _____ HNO3(稀)
_____ Fe(NO3)3+ _____ NO↑+ _____ H2O,被还原与未被还原的氮元素质量之比__________ 。
(3)_____ Cu2S+_____ HNO3
_____ Cu(NO3)2+ _____ NO↑+_____ S↓+ _____ H2O,被还原与未被还原硝酸物质的量之比是_______ 被还原的元素是_____ 。
(1)

(2)

(3)

您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】8.7g二氧化锰粉末与足量浓盐酸共热,可以生成标况下的氯气的体积为__ L,参与反应的盐酸中被氧化的物质的量为___ mol。
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐3】Ⅰ.高铁酸钾(K2FeO4)是一种新型、高效、多功能绿色水处理剂,工业上是先制得高铁酸钠,然后在低温下,向高铁酸钠溶液中加入KOH至饱和,使高铁酸钾析出。
(1)干法制备高铁酸钠的主要反应为:2FeSO4 + 6 Na2O2 = 2Na2FeO4 + 2Na2O + 2Na2SO4 + O2↑,该反应中Na2O2 是___________ (填氧化剂、还原剂)
(2)湿法制备高铁酸钾的反应体系中有六种微粒:Fe(OH)3、ClO-、OH-、FeO42-、Cl-、H2O。
①碱性条件下,氧化剂和还原剂的物质的量的比为3:2发生反应,写出并配平湿法制高铁酸钾的离子反应方程式:__________________ 。
②若反应过程中转移了0.3mol电子,则还原产物的物质的量为__________ mol。
Ⅱ.已知:2Fe3++2I-=2Fe2++I2,2Fe2++Br2=2Fe3++2Br-。
(1)含有1 mol FeI2和2 mol FeBr2的溶液中通入2 mol Cl2,此时被氧化的离子是______ 。
(2)若向含a mol FeI2和b mol FeBr2的溶液中通入c mol Cl2,当I-、Fe2+、Br-完全被氧化时,c=__________ (用含a、b的代数式表示)。
(1)干法制备高铁酸钠的主要反应为:2FeSO4 + 6 Na2O2 = 2Na2FeO4 + 2Na2O + 2Na2SO4 + O2↑,该反应中Na2O2 是
(2)湿法制备高铁酸钾的反应体系中有六种微粒:Fe(OH)3、ClO-、OH-、FeO42-、Cl-、H2O。
①碱性条件下,氧化剂和还原剂的物质的量的比为3:2发生反应,写出并配平湿法制高铁酸钾的离子反应方程式:
②若反应过程中转移了0.3mol电子,则还原产物的物质的量为
Ⅱ.已知:2Fe3++2I-=2Fe2++I2,2Fe2++Br2=2Fe3++2Br-。
(1)含有1 mol FeI2和2 mol FeBr2的溶液中通入2 mol Cl2,此时被氧化的离子是
(2)若向含a mol FeI2和b mol FeBr2的溶液中通入c mol Cl2,当I-、Fe2+、Br-完全被氧化时,c=
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐1】(1)某溶液中Cl-、Br-、I-三种离子的物质的量之比为1:2:3,要使它们的物质的量之比变为4:3:2,则需通入Cl2的物质的量是原溶液中I-的物质的量的 倍。
(2)KBr和KCl的混合物3.87g,溶于水并加入过量AgNO3溶液后,产生6.63g沉淀,则混合物中含K的质量分数
(3)5mL18%氢氧化钠溶液(d=1.2g/mL)最多能吸收 L标准状况下的CO2。
(2)KBr和KCl的混合物3.87g,溶于水并加入过量AgNO3溶液后,产生6.63g沉淀,则混合物中含K的质量分数
(3)5mL18%氢氧化钠溶液(d=1.2g/mL)最多能吸收 L标准状况下的CO2。
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】将一定量NaHCO3和Na2CO3的混合物充分加热,使NaHCO3完全分解,混合物质量减少了3.1g,将加热后剩余的固体物质与足量盐酸反应,收集到8.8g气体。计算原固体混合物中Na2CO3和NaHCO3的物质的量各为多少?
您最近一年使用:0次
计算题
|
适中
(0.65)
真题
【推荐3】氨和联氨(N2H4)是氮的两种常见化合物,在科学技术和生产中有重要的应用。
根据题意完成下列计算:
(1)联氨用亚硝酸氧化生成氮的另一种氢化物,该氢化物的相对分子质量为43.0,其中氮原子的质量分数为0.977,计算确定该氢化物的分子式___________ 。该氢化物受撞击则完全分解为氮气和氢气。4.30 g该氢化物受撞击后产生的气体在标准状况下的体积为___________ L。
(2)联氨和四氧化二氮可用作火箭推进剂,联氨是燃料,四氧化二氮作氧化剂,反应产物是氮气和水。
由联氨和四氧化二氮组成的火箭推进剂完全反应生成72.0 kg水,计算推进剂中联氨的质量___________ 。
(3)氨的水溶液可用于吸收NO与NO2混合气体,反应方程式为6NO+ 4NH3=5N2+6H2O,6NO2+ 8NH3=7N2+12H2O;NO与NO2混合气体180 mol被8.90×103g氨水(质量分数0.300)完全吸收,产生156 mol氮气。吸收后氨水密度为0.980 g/cm3。计算:①该混合气体中NO与NO2的体积比____________ 。②吸收后氨水的物质的量浓度_______________ (答案保留1位小数)。
(4)氨和二氧化碳反应可生成尿素CO(NH2)2。尿素在一定条件下会失去氨而缩合,如两分子尿素失去一分子氨形成二聚物:
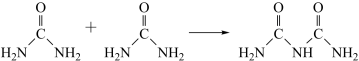 +NH3
+NH3
已知常压下120 mol CO(NH2)2在熔融状态发生缩合反应,失去80 mol NH3,生成二聚物(C2H5N3O2)和三聚物。测得缩合产物中二聚物的物质的量分数为0.60,推算缩合产物中各缩合物的物质的量之比__________ 。
根据题意完成下列计算:
(1)联氨用亚硝酸氧化生成氮的另一种氢化物,该氢化物的相对分子质量为43.0,其中氮原子的质量分数为0.977,计算确定该氢化物的分子式
(2)联氨和四氧化二氮可用作火箭推进剂,联氨是燃料,四氧化二氮作氧化剂,反应产物是氮气和水。
由联氨和四氧化二氮组成的火箭推进剂完全反应生成72.0 kg水,计算推进剂中联氨的质量
(3)氨的水溶液可用于吸收NO与NO2混合气体,反应方程式为6NO+ 4NH3=5N2+6H2O,6NO2+ 8NH3=7N2+12H2O;NO与NO2混合气体180 mol被8.90×103g氨水(质量分数0.300)完全吸收,产生156 mol氮气。吸收后氨水密度为0.980 g/cm3。计算:①该混合气体中NO与NO2的体积比
(4)氨和二氧化碳反应可生成尿素CO(NH2)2。尿素在一定条件下会失去氨而缩合,如两分子尿素失去一分子氨形成二聚物:
 +NH3
+NH3已知常压下120 mol CO(NH2)2在熔融状态发生缩合反应,失去80 mol NH3,生成二聚物(C2H5N3O2)和三聚物。测得缩合产物中二聚物的物质的量分数为0.60,推算缩合产物中各缩合物的物质的量之比
您最近一年使用:0次



