现有四种元素,分别位于元素周期表的前四个不同周期,其原子序数总和为48。由它们可组成甲、乙、丙、丁四种单质和A、B、C、D四种化合物,其中甲、乙为非金属单质,丙、丁为金属单质;这些物质间的转化关系如下图所示(反应条件已省略)。
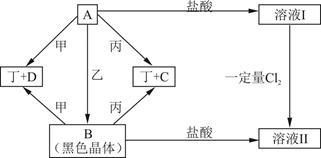
请回答下列问题:
(1)组成丁的元素在周期表中的位置________ ,B的俗名__________ ,C物质的用途之一___________ 。
(2)写出A+乙 B的化学方程式
B的化学方程式________________ 。
(3)在加热条件下,丁与气态D可发生反应,该反应的化学方程式为__________ 。
(4)若21.6g A与适量的乙反应生成B,A、B按上述图示转化为溶液I和溶液II(假设各步反应均恰好进行完全);向溶液I中通入________ mol Cl2,经充分反应可恰好使溶质的组成与溶液II完全相同。

请回答下列问题:
(1)组成丁的元素在周期表中的位置
(2)写出A+乙
 B的化学方程式
B的化学方程式(3)在加热条件下,丁与气态D可发生反应,该反应的化学方程式为
(4)若21.6g A与适量的乙反应生成B,A、B按上述图示转化为溶液I和溶液II(假设各步反应均恰好进行完全);向溶液I中通入
2011·江西·三模 查看更多[1]
(已下线)2011届江西省师大附中高三第三次模拟考试(理综)化学部分
更新时间:2016-12-09 01:49:48
|
相似题推荐
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐1】利用某粗 矿(含有杂质MnO和
矿(含有杂质MnO和 )制取纯
)制取纯 的流程如图。请回答下列问题:
的流程如图。请回答下列问题:

(1)操作X是_______ ;写出一种能够提高酸浸率的方法_______ 。
(2)“酸浸”过程中发生的反应均为复分解反应,写出“酸浸”步骤所涉及的反应离子方程式_______ 。
(3)“氧化”步骤中氧化剂与还原剂的物质的量之比为_______ ,上述流程中能够循环利用的物质是_______ (写名称)。
(4)若氯气与氢氧化钠溶液反应除了生成 外,还有部分NaClO,且二者的物质的量之比为3∶1,则氧化产物与还原产物物质的量之比为
外,还有部分NaClO,且二者的物质的量之比为3∶1,则氧化产物与还原产物物质的量之比为_______ 。
 矿(含有杂质MnO和
矿(含有杂质MnO和 )制取纯
)制取纯 的流程如图。请回答下列问题:
的流程如图。请回答下列问题:
(1)操作X是
(2)“酸浸”过程中发生的反应均为复分解反应,写出“酸浸”步骤所涉及的反应离子方程式
(3)“氧化”步骤中氧化剂与还原剂的物质的量之比为
(4)若氯气与氢氧化钠溶液反应除了生成
 外,还有部分NaClO,且二者的物质的量之比为3∶1,则氧化产物与还原产物物质的量之比为
外,还有部分NaClO,且二者的物质的量之比为3∶1,则氧化产物与还原产物物质的量之比为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐2】某小组同学欲探究浓硝酸的性质,设计并完成了下列2个实验:
实验Ⅰ:将玻璃棒在酒精灯上烧至红热,迅速插入热的浓硝酸中,有红棕色气体产生。
实验Ⅱ:将小块木炭在酒精灯上灼烧,木炭红热,迅速将其投入到热的浓硝酸中,发生剧烈反应,有大量红棕色气体产生,液面上方的木炭迅速燃烧发出光亮。
(1)实验Ⅰ中浓硝酸受热分解时,除了产生NO2外还有O2生成,生成O2的原因是(根据氧化还原规律分析)_______ ;产生的O2与NO2在同温同压下的体积比是_______ 。
(2)木炭与浓硝酸反应生成二氧化碳,体现浓硝酸的_______ 性。
(3)该小组同学对实验Ⅱ中“木炭在液面上迅速燃烧发出光亮”的原因做出了如下3种猜想:
猜想一:甲同学认为是空气中的O2支持木炭燃烧。
猜想二:乙同学认为是浓硝酸分解产生的_______ 支持木炭燃烧。
猜想三:丙同学认为是反应中产生的NO2支持木炭燃烧。
①根据木炭在空气中燃烧的现象,甲同学的猜想明显不合理,理由是_______ 。
②经分析,乙同学的猜想也不合理。要证实丙同学的猜想可能是合理的,还需补充的实验是:把木炭在酒精灯上烧至红热,_______ (请写出实验操作、现象)。
实验Ⅰ:将玻璃棒在酒精灯上烧至红热,迅速插入热的浓硝酸中,有红棕色气体产生。
实验Ⅱ:将小块木炭在酒精灯上灼烧,木炭红热,迅速将其投入到热的浓硝酸中,发生剧烈反应,有大量红棕色气体产生,液面上方的木炭迅速燃烧发出光亮。
(1)实验Ⅰ中浓硝酸受热分解时,除了产生NO2外还有O2生成,生成O2的原因是(根据氧化还原规律分析)
(2)木炭与浓硝酸反应生成二氧化碳,体现浓硝酸的
(3)该小组同学对实验Ⅱ中“木炭在液面上迅速燃烧发出光亮”的原因做出了如下3种猜想:
猜想一:甲同学认为是空气中的O2支持木炭燃烧。
猜想二:乙同学认为是浓硝酸分解产生的
猜想三:丙同学认为是反应中产生的NO2支持木炭燃烧。
①根据木炭在空气中燃烧的现象,甲同学的猜想明显不合理,理由是
②经分析,乙同学的猜想也不合理。要证实丙同学的猜想可能是合理的,还需补充的实验是:把木炭在酒精灯上烧至红热,
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐3】硫酸亚铁是一种补铁剂,某兴趣小组利用经初步处理的含有 的废液制备硫酸亚铁晶体的流程如下:
的废液制备硫酸亚铁晶体的流程如下:

(1)加入饱和 溶液后,得到白色沉淀,则操作1为
溶液后,得到白色沉淀,则操作1为___________ ,若 溶液浓度偏低可能会形成胶体,验证的方法为
溶液浓度偏低可能会形成胶体,验证的方法为___________ 。
(2)加入铁粉的作用是___________ 。
(3)测定废液中 的浓度可使用已知浓度的酸性高锰酸钾溶液,请配平以下方程式,并用单线桥法表示电子转移过程:
的浓度可使用已知浓度的酸性高锰酸钾溶液,请配平以下方程式,并用单线桥法表示电子转移过程:___________
___________ ___________
___________ ___________
___________ ___________
___________ ___________
___________ ___________
___________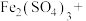 ___________
___________
(4)该兴趣小组在研究硫酸亚铁(FeSO4)热稳定性时,作出了两种假设:
①假设一:按 受热分解的方式分解,则
受热分解的方式分解,则 受热分解的化学方程式为
受热分解的化学方程式为___________ ;
②假设二:按 受热分解的方式分解,且产物中有一种碱性氧化物和两种酸性氧化物生成,则
受热分解的方式分解,且产物中有一种碱性氧化物和两种酸性氧化物生成,则 受热分解的化学方程式为
受热分解的化学方程式为___________ 。
(5) 和
和 的相互转化可用于物质含量的测定,如测定某氯化亚铜样品中CuCl的含量,流程如下:准确称取氯化亚铜样品mg,将其置于过量的
的相互转化可用于物质含量的测定,如测定某氯化亚铜样品中CuCl的含量,流程如下:准确称取氯化亚铜样品mg,将其置于过量的 溶液中,发生以下反应:
溶液中,发生以下反应: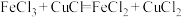 ,待固体完全溶解后,加入适量稀硫酸,用
,待固体完全溶解后,加入适量稀硫酸,用 的
的 溶液氧化反应生成的
溶液氧化反应生成的 (该条件下
(该条件下 不被氧化),消耗
不被氧化),消耗 溶液bmL,反应中
溶液bmL,反应中 被还原为
被还原为 。则样品中CuCl的质量分数为
。则样品中CuCl的质量分数为___________ 。
 的废液制备硫酸亚铁晶体的流程如下:
的废液制备硫酸亚铁晶体的流程如下:
(1)加入饱和
 溶液后,得到白色沉淀,则操作1为
溶液后,得到白色沉淀,则操作1为 溶液浓度偏低可能会形成胶体,验证的方法为
溶液浓度偏低可能会形成胶体,验证的方法为(2)加入铁粉的作用是
(3)测定废液中
 的浓度可使用已知浓度的酸性高锰酸钾溶液,请配平以下方程式,并用单线桥法表示电子转移过程:
的浓度可使用已知浓度的酸性高锰酸钾溶液,请配平以下方程式,并用单线桥法表示电子转移过程:___________
 ___________
___________ ___________
___________ ___________
___________ ___________
___________ ___________
___________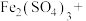 ___________
___________
(4)该兴趣小组在研究硫酸亚铁(FeSO4)热稳定性时,作出了两种假设:
①假设一:按
 受热分解的方式分解,则
受热分解的方式分解,则 受热分解的化学方程式为
受热分解的化学方程式为②假设二:按
 受热分解的方式分解,且产物中有一种碱性氧化物和两种酸性氧化物生成,则
受热分解的方式分解,且产物中有一种碱性氧化物和两种酸性氧化物生成,则 受热分解的化学方程式为
受热分解的化学方程式为(5)
 和
和 的相互转化可用于物质含量的测定,如测定某氯化亚铜样品中CuCl的含量,流程如下:准确称取氯化亚铜样品mg,将其置于过量的
的相互转化可用于物质含量的测定,如测定某氯化亚铜样品中CuCl的含量,流程如下:准确称取氯化亚铜样品mg,将其置于过量的 溶液中,发生以下反应:
溶液中,发生以下反应: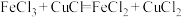 ,待固体完全溶解后,加入适量稀硫酸,用
,待固体完全溶解后,加入适量稀硫酸,用 的
的 溶液氧化反应生成的
溶液氧化反应生成的 (该条件下
(该条件下 不被氧化),消耗
不被氧化),消耗 溶液bmL,反应中
溶液bmL,反应中 被还原为
被还原为 。则样品中CuCl的质量分数为
。则样品中CuCl的质量分数为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐1】已知在温度低于570°C时,还原铁粉与水蒸气反应的产物是FeO;高于570°C时,生成Fe3O4。老师用如图所示实验装置,完成了还原铁粉与水蒸气反应的演示实验。

甲同学为探究实验后试管内固体的成分,进行了下列实验:
试回答下列问题:
(1)湿棉花的作用是_______________________________________________________ 。
(2)写出高于570°C时,Fe与水蒸气反应的化学方程式:______________________________________ 。
(3)乙同学认为加入KSCN溶液没有出现血红色原因可能是固体中没有Fe3O4,也有可能是因为______ (填物质名称)过量造成的。该物质过量时,溶液中还会发生反应,导致加入KSCN溶液时没有出现血红色,该反应的离子方程式是___________________________________________________ 。
(4)丙同学利用上述实验①加盐酸后的溶液制取白色的Fe(OH)2沉淀,向滤液中加入足量NaOH溶液后,观察到的实验现象为_____________________________________________________________ 。

甲同学为探究实验后试管内固体的成分,进行了下列实验:
| 实验编号 | 实验操作 | 实验现象 |
| ① | 取少量黑色粉末放入试管中,加入盐酸,微热 | 黑色粉末逐渐溶解,溶液呈浅绿色;有少量气泡产生 |
| ② | 向试管中滴加几滴KSCN溶液,振荡 | 溶液没有出现血红色 |
(1)湿棉花的作用是
(2)写出高于570°C时,Fe与水蒸气反应的化学方程式:
(3)乙同学认为加入KSCN溶液没有出现血红色原因可能是固体中没有Fe3O4,也有可能是因为
(4)丙同学利用上述实验①加盐酸后的溶液制取白色的Fe(OH)2沉淀,向滤液中加入足量NaOH溶液后,观察到的实验现象为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】学生利用下图所列装置进行“铁与水蒸气反应”的实验,并利用产物进一步制取FeCl3·6H2O晶体。(图中夹持及尾气处理装置均已略去)

回答下列问题:
(1)所用铁粉中若有杂质,欲除去不纯铁粉中混有的铝粉可以选用的试剂为_____________ (填序号)。
A.稀盐酸 B.氢氧化钠溶液 C.浓硫酸 D.FeCl3溶液
此步涉及反应的离子方程式为_____________________________________ 。
(2)反应发生后装置B中发生反应的化学方程式是______________________________ 。D装置的作用:________________________________________________ 。
(3)该小组学生把B中反应后的产物加入足量的盐酸,过滤,用上述滤液制取FeCl3·6H2O晶体,设计流程如下:

①用离子方程式表示步骤I中通入Cl2的作用__________________________________ ;
②为了检验某未知溶液是否是FeCl2溶液,同学们设计了以下实验方案加以证明。向一支装有该未 知溶液的试管中先通入氯气,再滴加KSCN溶液,溶液呈现红色,证明该未知溶液是FeCl2溶液。你认为此方案是否合理_______________ (填“合理”或“不合理”)。

回答下列问题:
(1)所用铁粉中若有杂质,欲除去不纯铁粉中混有的铝粉可以选用的试剂为
A.稀盐酸 B.氢氧化钠溶液 C.浓硫酸 D.FeCl3溶液
此步涉及反应的离子方程式为
(2)反应发生后装置B中发生反应的化学方程式是
(3)该小组学生把B中反应后的产物加入足量的盐酸,过滤,用上述滤液制取FeCl3·6H2O晶体,设计流程如下:

①用离子方程式表示步骤I中通入Cl2的作用
②为了检验某未知溶液是否是FeCl2溶液,同学们设计了以下实验方案加以证明。向一支装有该未 知溶液的试管中先通入氯气,再滴加KSCN溶液,溶液呈现红色,证明该未知溶液是FeCl2溶液。你认为此方案是否合理
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐3】树德中学高2016级研究性学习小组请你参与“研究铁与水反应所得固体物质的成分,性质及再利用”实验探究,并共同解答下列问题:
探究一 设计如图所示装置进行“铁与水反应”的实验
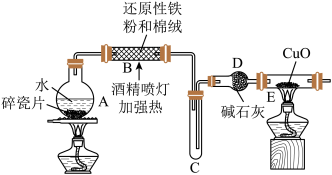
(1)硬质玻璃管中发生反应的化学方程式为__________________ 。
(2)反应前A中投放碎瓷片的目的是__________________ 。
(3)装置E中的现象是__________________ 。
探究二 设计如下实验方案确定反应后硬质玻璃管中黑色固体的成分。
(4)硬质玻璃管B冷却后,取少许其中的固体物质溶于_____ 后,将所得溶液分成两份。
(5)一份滴加几滴KSCN溶液。若溶液变红色,推断硬质玻璃管B中固体物质的成分为______________ (选填序号,①一定有Fe3O4 ②一定有Fe ③只有Fe3O4④只有Fe,下同);若溶液未变血红色,推断硬质玻璃管B中固体物质的成分为______________ 。
(6)另—份用胶头滴管加入_______________ ,若出现______________ 现象,可以证明溶液中存在Fe2+,其反应的离子方程式是_____________ 。
探究三 设计如下流程测定反应后硬质玻璃管B中固体含铁元素的质量分数。
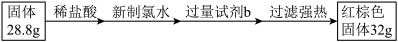
(7)试剂b的化学式是_________ 。
(8)计算反应后B装置中铁元素的质量分数为_______________ 。(保留小数点后—位)
探究一 设计如图所示装置进行“铁与水反应”的实验

(1)硬质玻璃管中发生反应的化学方程式为
(2)反应前A中投放碎瓷片的目的是
(3)装置E中的现象是
探究二 设计如下实验方案确定反应后硬质玻璃管中黑色固体的成分。
(4)硬质玻璃管B冷却后,取少许其中的固体物质溶于
(5)一份滴加几滴KSCN溶液。若溶液变红色,推断硬质玻璃管B中固体物质的成分为
(6)另—份用胶头滴管加入
探究三 设计如下流程测定反应后硬质玻璃管B中固体含铁元素的质量分数。

(7)试剂b的化学式是
(8)计算反应后B装置中铁元素的质量分数为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐1】为探究不溶性盐A(仅含四种元素)的组成和性质,设计并完成如下实验:(假设各步反应均完全发生,生成的气体全部逸出)

请回答:
(1)A的组成元素除H、O外,还含有_______ (用元素符号表示),其化学式为_______ ;
(2)红棕色固体B的一种用途_______ ;
(3)往溶液D中通入SO2的离子方程式_______ 。

请回答:
(1)A的组成元素除H、O外,还含有
(2)红棕色固体B的一种用途
(3)往溶液D中通入SO2的离子方程式
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐2】某二元化合物X是锂硫电池的电极材料,为探究其组成进行了如下实验:

固体乙是一种单质,固体丙呈红棕色,将气体A通入溶液C中也能生成固体乙。
请回答:
(1)X的化学式是_________________ ,步骤①的化学方程式是_________________________ 。
(2)气体A通入溶液C发生反应的离子方程式是_________________________ 。

固体乙是一种单质,固体丙呈红棕色,将气体A通入溶液C中也能生成固体乙。
请回答:
(1)X的化学式是
(2)气体A通入溶液C发生反应的离子方程式是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐1】利用硫酸渣(主要含Fe2O3、FeO,杂质为Al2O3和SiO2等)生产铁基颜料铁黄(FeOOH)的流程如下:

(1)FeOOH中Fe的化合价为______ 。
(2)“酸溶”时,Fe2O3与硫酸反应的化学方程式为______ 。
(3)滤渣Ⅰ的主要成分是FeS2、S和______ (填化学式);Fe3+被FeS2还原的离子方程式为______ 。
(4)“氧化”时,生成FeOOH的离子方程式为______ 。

(1)FeOOH中Fe的化合价为
(2)“酸溶”时,Fe2O3与硫酸反应的化学方程式为
(3)滤渣Ⅰ的主要成分是FeS2、S和
(4)“氧化”时,生成FeOOH的离子方程式为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐2】在人类社会的发展进程中,金属起着重要的作用。请回答下列问题:
(1)人类最早使用的金属材料的主要成分是铜。下列有关铜元素的说法中,错误的是_______(填标号)。
(2)生铁中含有一种铁碳化合物X(Fe3C)。X在足量的空气中高温煅烧,生成有磁性的固体Y,将Y溶于过量盐酸后溶液中大量存在的阳离子是_______ (填离子符号)。
(3)铁及其化合物在生产生活中具有广泛应用。一定条件下,铁及其化合物之间发生相互转化。NaFeO2可完全溶于水且与水反应生成两种碱,写出发生反应的离子方程式:_______ 。
(4)某溶液中有Mg2+、Fe2+、Cu2+等离子,向其中加入过量的NaOH溶液后,过滤,将滤渣高温灼烧,并将灼烧后的固体投入过量的稀盐酸中,所得溶液与原溶液相比,溶液中大量减少的阳离子是_______ (填离子符号)。
(5)氧化铁是重要的工业颜料,用废铁屑制备它的流程如图:
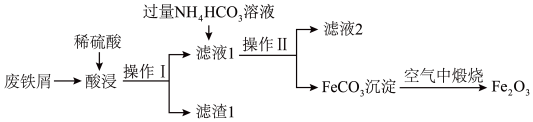
①完成“操作Ⅰ”所需要的玻璃仪器除烧杯外,还需要的是_______ 。
②加入稍过量NH4HCO3溶液时,不仅有沉淀生成,还有无色无味的气体生成,请写出生成FeCO3沉淀的离子方程式:_______ 。
③FeCO3在空气中加热反应生成Fe2O3时,氧化剂和还原剂的物质的量之比为_______ 。
(1)人类最早使用的金属材料的主要成分是铜。下列有关铜元素的说法中,错误的是_______(填标号)。
| A.青铜、不锈钢、硬铝都是合金 |
| B.铜表面易形成致密的氧化膜 |
| C.铜与O2反应可生成黑色的CuO |
D. 是一种混合物,加热后变为白色固体 是一种混合物,加热后变为白色固体 |
(3)铁及其化合物在生产生活中具有广泛应用。一定条件下,铁及其化合物之间发生相互转化。NaFeO2可完全溶于水且与水反应生成两种碱,写出发生反应的离子方程式:
(4)某溶液中有Mg2+、Fe2+、Cu2+等离子,向其中加入过量的NaOH溶液后,过滤,将滤渣高温灼烧,并将灼烧后的固体投入过量的稀盐酸中,所得溶液与原溶液相比,溶液中大量减少的阳离子是
(5)氧化铁是重要的工业颜料,用废铁屑制备它的流程如图:

①完成“操作Ⅰ”所需要的玻璃仪器除烧杯外,还需要的是
②加入稍过量NH4HCO3溶液时,不仅有沉淀生成,还有无色无味的气体生成,请写出生成FeCO3沉淀的离子方程式:
③FeCO3在空气中加热反应生成Fe2O3时,氧化剂和还原剂的物质的量之比为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】取少量Fe2O3粉末(红棕色)加入适量盐酸,发生反应的化学方程式为________________ ,反应后得到的溶液呈________ 色。用此溶液分别做如下实验:
(1)取少量溶液置于试管中,滴入几滴NaOH溶液,可观察到有红褐色沉淀生成,反应的化学方程式为____________________________________ ,此反应属于________________ 。
(2)在小烧杯中加入20 mL蒸馏水,加热至沸腾后,向沸水中滴入几滴饱和FeCl3溶液,继续煮沸至溶液呈________ 色,即制得Fe(OH)3胶体。
(3)取另一只小烧杯也加入20 mL蒸馏水,向烧杯中加入1 mL FeCl3溶液,振荡均匀后,将此烧杯(编号甲)与盛有Fe(OH)3胶体的烧杯(编号乙)一起放置于暗处,分别用激光笔照射烧杯中的液体,可以看到__________ 烧杯中的液体产生丁达尔效应,这个实验可以用来区别________________________ 。
(4)取乙烧杯中少量Fe(OH)3胶体置于试管中,向试管中滴加一定量的稀HI溶液,边滴加边振荡,会出现一系列变化。
a.先出现红褐色沉淀,原因是__________________________________________ 。
b.随后沉淀溶解,溶液呈黄色,写出此反应的离子方程式:________________ 。
c.最后溶液颜色加深,原因是_________________________ (用离子方程式表示)。
d.用稀盐酸代替稀HI溶液,能出现上述哪些相同的变化现象?________ (填序号)。
(1)取少量溶液置于试管中,滴入几滴NaOH溶液,可观察到有红褐色沉淀生成,反应的化学方程式为
(2)在小烧杯中加入20 mL蒸馏水,加热至沸腾后,向沸水中滴入几滴饱和FeCl3溶液,继续煮沸至溶液呈
(3)取另一只小烧杯也加入20 mL蒸馏水,向烧杯中加入1 mL FeCl3溶液,振荡均匀后,将此烧杯(编号甲)与盛有Fe(OH)3胶体的烧杯(编号乙)一起放置于暗处,分别用激光笔照射烧杯中的液体,可以看到
(4)取乙烧杯中少量Fe(OH)3胶体置于试管中,向试管中滴加一定量的稀HI溶液,边滴加边振荡,会出现一系列变化。
a.先出现红褐色沉淀,原因是
b.随后沉淀溶解,溶液呈黄色,写出此反应的离子方程式:
c.最后溶液颜色加深,原因是
d.用稀盐酸代替稀HI溶液,能出现上述哪些相同的变化现象?
您最近一年使用:0次


 红棕色化合物的化学方程式是
红棕色化合物的化学方程式是

