中科院官方微信中科院之于2017年3月9日发表《一个“网红”的转化-灰霾专题》,提出灰霾细颗粒物的成因,部分分析如下图所示。
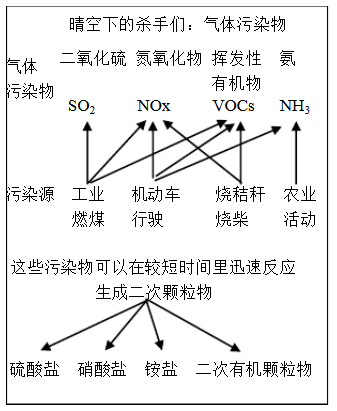
(1)根据上图信息可以看出,下列哪种污染源不产生NOx_________ .
A.工业燃煤 B.机动车尾气 C.烧秸秆 D.农业活动
(2)若某地空气潮湿,且空气含有的大气污染物主要是SO2、NH3,根据上图中所举的“SO2 SO32-
SO32- 盐
盐 SO42-
SO42- 盐”的流程,请写出该地形成二次颗粒物硫酸盐的化学反应方程式:
盐”的流程,请写出该地形成二次颗粒物硫酸盐的化学反应方程式:_____________ 。
(3)当前频繁出现的雾霾天气与汽车尾气的排放有一定的关系,为了减少污染,可尝试使用汽车尾气净化装置,其原理如图所示。

写出净化过程中的总化学方程式:________
(4)将装有amLNO和NO2混合气体的集气瓶倒立在水槽中,然后鼓入一定量O2,最终集气瓶里面剩余气体体积为bmL,则集气瓶内所得HNO3的物质的量浓度为______ mol/L(不考虑集气瓶内硝酸扩散到水槽中,设气体摩尔体积为Vm)。

(1)根据上图信息可以看出,下列哪种污染源不产生NOx
A.工业燃煤 B.机动车尾气 C.烧秸秆 D.农业活动
(2)若某地空气潮湿,且空气含有的大气污染物主要是SO2、NH3,根据上图中所举的“SO2
 SO32-
SO32- 盐
盐 SO42-
SO42- 盐”的流程,请写出该地形成二次颗粒物硫酸盐的化学反应方程式:
盐”的流程,请写出该地形成二次颗粒物硫酸盐的化学反应方程式:(3)当前频繁出现的雾霾天气与汽车尾气的排放有一定的关系,为了减少污染,可尝试使用汽车尾气净化装置,其原理如图所示。

写出净化过程中的总化学方程式:
(4)将装有amLNO和NO2混合气体的集气瓶倒立在水槽中,然后鼓入一定量O2,最终集气瓶里面剩余气体体积为bmL,则集气瓶内所得HNO3的物质的量浓度为
更新时间:2018-04-07 10:05:05
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】完成下列填空:
(1)0.3molNH3分子中所含原子数与___ 个H2O分子中所含原子数相等。
(2)在一定的温度和压强下,1体积气体X2跟3体积气体Y2刚好化合生成2体积气体A,则A的化学式可表示为___ 。
(3)在同温同压同体积的条件下,H2与气体B的质量之比是1:8,则B的摩尔质量为___ 。
(4)在25℃、101kPa的条件下,同质量的CH4和气体C的体积之比是15:8,则C的摩尔质量为___ 。
(5)在两个相同容积的密闭容器D、E中,分别充入相同质量的X气体和CO气体,D和E中的压强之比是7:16,则X的摩尔质量为___ 。
(6)物质的量浓度相同的NaCl、MgCl2、AlCl3,溶液中Cl-的物质的量浓度之比为___ ;体积相同的、物质的量浓度之比为1:2:3的NaCl、MgCl2、AlCl3三种溶液中Cl-的物质的量之比为___ 。
(1)0.3molNH3分子中所含原子数与
(2)在一定的温度和压强下,1体积气体X2跟3体积气体Y2刚好化合生成2体积气体A,则A的化学式可表示为
(3)在同温同压同体积的条件下,H2与气体B的质量之比是1:8,则B的摩尔质量为
(4)在25℃、101kPa的条件下,同质量的CH4和气体C的体积之比是15:8,则C的摩尔质量为
(5)在两个相同容积的密闭容器D、E中,分别充入相同质量的X气体和CO气体,D和E中的压强之比是7:16,则X的摩尔质量为
(6)物质的量浓度相同的NaCl、MgCl2、AlCl3,溶液中Cl-的物质的量浓度之比为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】I.下图是抚州市某儿童微量元素体检报告单的部分数据:
根据上表的数据,回答下列问题:
(1)该儿童_____ 元素含量偏低。
(2)报告单中“μmol/L”是__________ (填“质量”、“体积”或“浓度”)的单位。
(3)服用维生素C可使食物中的Fe3+转化为Fe2+。在这个过程中体现维生素C的________ (填“氧化性”或“还原性”)。
II.高铁酸钾(K2FeO4,铁元素为+6价)是一种新型、高效、多功能绿色水处理剂,无二次污染。制备高铁酸钾的离子反应方程式为:___ Fe(OH)3+__ ClO-+___ OH-=___ FeO42-+___ Cl-+__ H2O
回答下列问题:
(4)配平该离子方程式。
(5)每生成1molFeO42-转移的电子数为___________ ,若反应过程中转移了0.3mol电子,则还原产物的物质的量为________ mol。
抚州市某医疗机构临床检验结果报告单 | ||||
分析项目 | 检测结果 | 单位 | 正常值参考范围 | |
1 | 锌(Zn) | 109.62 | μmol/L | 66-120 |
2 | 铁(Fe) | 5.92↓ | mmol/L | 7.52-11.82 |
3 | 钙(Ca) | 1.68 | mmol/L | 1.55-2.10 |
…… | ||||
根据上表的数据,回答下列问题:
(1)该儿童
(2)报告单中“μmol/L”是
(3)服用维生素C可使食物中的Fe3+转化为Fe2+。在这个过程中体现维生素C的
II.高铁酸钾(K2FeO4,铁元素为+6价)是一种新型、高效、多功能绿色水处理剂,无二次污染。制备高铁酸钾的离子反应方程式为:
回答下列问题:
(4)配平该离子方程式。
(5)每生成1molFeO42-转移的电子数为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】现有下列十二种物质:①NH3 ②Na2O2 ③H2SO4 ④氨水 ⑤稀硝酸 ⑥NH4Cl ⑦熔融NaOH ⑧NaHCO3
(1)按物质的分类方法填写下列的空白处:
电解质___________ 非电解质___________ 既含有离子键又含有共价键的化合物___________
(2)上述物质中有两种物质之间可发生离子反应:H++OH-=H2O,该离子反应对应的化方程式(写一个)为:___________
(3)⑧在水中的电离方程式为___________
(4)标况112 mL①溶于水配成250 mL溶液,所得溶液物质的量浓度为___________
(1)按物质的分类方法填写下列的空白处:
电解质
(2)上述物质中有两种物质之间可发生离子反应:H++OH-=H2O,该离子反应对应的化方程式(写一个)为:
(3)⑧在水中的电离方程式为
(4)标况112 mL①溶于水配成250 mL溶液,所得溶液物质的量浓度为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】为消除燃煤烟气中含有的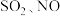 ,研究者提出如下烟气“脱硫”、“脱硝”的方法。回答下列问题:
,研究者提出如下烟气“脱硫”、“脱硝”的方法。回答下列问题:
【方法一】以 作为吸收剂进行一体化“脱硫”“脱硝”,将烟气中的
作为吸收剂进行一体化“脱硫”“脱硝”,将烟气中的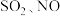 转化为
转化为 。
。
(1) 溶液理论上最多能吸收标准状况下
溶液理论上最多能吸收标准状况下 的体积为
的体积为_________________  。
。
(2)实验室利用模拟烟气(模拟烟气中 和
和 的物质的量之比为
的物质的量之比为 )探究该方法“脱硫”“脱硝”的效果,一定时间内,温度对硫、硝脱除率的影响曲线如图所示:
)探究该方法“脱硫”“脱硝”的效果,一定时间内,温度对硫、硝脱除率的影响曲线如图所示: 的脱除率高于
的脱除率高于 ,其原因除
,其原因除 的还原性比
的还原性比 强外,还可能是
强外,还可能是_____________________________ 。
② 时,吸收液中烟气转化生成的
时,吸收液中烟气转化生成的 和
和 的物质的量之比为
的物质的量之比为_________________ 。
【方法二】 技术(
技术( 选择性催化还原氮氧化物)
选择性催化还原氮氧化物)
研究表明,铁基催化剂在 范围内实现
范围内实现 技术的过程如图所示:
技术的过程如图所示: 在整个反应过程中的作用为
在整个反应过程中的作用为_____________ ;等物质的量的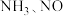 在有氧条件下转化为
在有氧条件下转化为 的总反应化学方程式为
的总反应化学方程式为_____________________ 。
(4)若使用锰基催化剂(活性物质为 )代替铁基催化剂,烟气中含有的
)代替铁基催化剂,烟气中含有的 会使催化剂失效而降低
会使催化剂失效而降低 脱除率,用化学方程式表示催化剂失效的原因:
脱除率,用化学方程式表示催化剂失效的原因:_________________________ 。
(5)向反应体系中添加 可显著提高
可显著提高 脱除率,原因是
脱除率,原因是 与
与 反应生成
反应生成 和
和 ;
; 再与
再与 发生反应转化为
发生反应转化为 ,则
,则 的离子符号为
的离子符号为_____________ 。
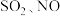 ,研究者提出如下烟气“脱硫”、“脱硝”的方法。回答下列问题:
,研究者提出如下烟气“脱硫”、“脱硝”的方法。回答下列问题:【方法一】以
 作为吸收剂进行一体化“脱硫”“脱硝”,将烟气中的
作为吸收剂进行一体化“脱硫”“脱硝”,将烟气中的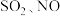 转化为
转化为 。
。(1)
 溶液理论上最多能吸收标准状况下
溶液理论上最多能吸收标准状况下 的体积为
的体积为 。
。(2)实验室利用模拟烟气(模拟烟气中
 和
和 的物质的量之比为
的物质的量之比为 )探究该方法“脱硫”“脱硝”的效果,一定时间内,温度对硫、硝脱除率的影响曲线如图所示:
)探究该方法“脱硫”“脱硝”的效果,一定时间内,温度对硫、硝脱除率的影响曲线如图所示: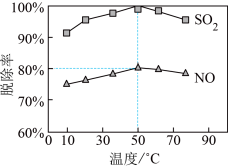
 的脱除率高于
的脱除率高于 ,其原因除
,其原因除 的还原性比
的还原性比 强外,还可能是
强外,还可能是②
 时,吸收液中烟气转化生成的
时,吸收液中烟气转化生成的 和
和 的物质的量之比为
的物质的量之比为【方法二】
 技术(
技术( 选择性催化还原氮氧化物)
选择性催化还原氮氧化物)研究表明,铁基催化剂在
 范围内实现
范围内实现 技术的过程如图所示:
技术的过程如图所示:
 在整个反应过程中的作用为
在整个反应过程中的作用为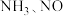 在有氧条件下转化为
在有氧条件下转化为 的总反应化学方程式为
的总反应化学方程式为(4)若使用锰基催化剂(活性物质为
 )代替铁基催化剂,烟气中含有的
)代替铁基催化剂,烟气中含有的 会使催化剂失效而降低
会使催化剂失效而降低 脱除率,用化学方程式表示催化剂失效的原因:
脱除率,用化学方程式表示催化剂失效的原因:(5)向反应体系中添加
 可显著提高
可显著提高 脱除率,原因是
脱除率,原因是 与
与 反应生成
反应生成 和
和 ;
; 再与
再与 发生反应转化为
发生反应转化为 ,则
,则 的离子符号为
的离子符号为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】N元素的单质及其化合物之间的转化关系:NH3 N2 NO NO2 HNO3。回答下列问题:
(1)工业上利用合成氨实现人工固氮的化学反应方程式___________ ;盛放硝酸的瓶子用棕色试剂瓶原因___________ ;
(2)近几年来关于氮污染的治理倍受关注,根据氮的性质回答以下问题;Ertl(获2007年诺贝尔化学奖)对合成氨机理进行深入研究,并将研究成果用于汽车尾气处理中,在催化剂存在下可将NO和CO反应转化为两种无色无毒气体,用化学反应方程式表示这个过程___________ ;
(3)潜艇中使用的液氨-液氧燃料电池工作原理如图所示:
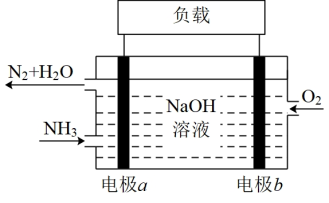
①电极a名称是___________ 。
②电解质溶液中OH-离子向___________ 移动(填“电极a”或 “电极b”)。
③电极b的电极反应式为___________ 。
(1)工业上利用合成氨实现人工固氮的化学反应方程式
(2)近几年来关于氮污染的治理倍受关注,根据氮的性质回答以下问题;Ertl(获2007年诺贝尔化学奖)对合成氨机理进行深入研究,并将研究成果用于汽车尾气处理中,在催化剂存在下可将NO和CO反应转化为两种无色无毒气体,用化学反应方程式表示这个过程
(3)潜艇中使用的液氨-液氧燃料电池工作原理如图所示:

①电极a名称是
②电解质溶液中OH-离子向
③电极b的电极反应式为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】硝酸工业尾气中氮氧化物(NO 和NO2)是主要的大气污染物之一,可用氨氧混合气体进行选择性还原处理。其主要反应原理如下:4NO+4NH3+O2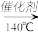 4N2+6H2O 6NO2+8NH3
4N2+6H2O 6NO2+8NH3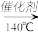 7N2+12H2O,某硝酸厂排放的尾气中氮氧化合物的含量为2490mg/m3(体积已换算成标准状况),其中NO NO2的物质的量比为4:1。设尾气中氮氧化物与氨氧混合气恰好完全反应。
7N2+12H2O,某硝酸厂排放的尾气中氮氧化合物的含量为2490mg/m3(体积已换算成标准状况),其中NO NO2的物质的量比为4:1。设尾气中氮氧化物与氨氧混合气恰好完全反应。
(1)尾气中氮氧化物的平均相对原子量为_____________ ;尾气中NO的含量为_____ mg/m3。
(2)要处理5m3的尾气,需要氨氧混合气的体积为_______ L。
另一种处理氮氧化物的方法是用烧碱进行吸收,产物为NaNO2、NaNO3和H2O。现有含0.5mol氮氧化物的尾气,恰好被一定体积25%NaOH溶液(密度1.28g/cm3)完全吸收。
(3)NaOH溶液的物质的量浓度为_____________ mol/L,体积为_____ mL。
(4)已知反应后溶液含有0.35molNaNO2。若将尾气NO 和NO2的平均组成用NOx表示,则x=______
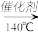 4N2+6H2O 6NO2+8NH3
4N2+6H2O 6NO2+8NH3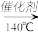 7N2+12H2O,某硝酸厂排放的尾气中氮氧化合物的含量为2490mg/m3(体积已换算成标准状况),其中NO NO2的物质的量比为4:1。设尾气中氮氧化物与氨氧混合气恰好完全反应。
7N2+12H2O,某硝酸厂排放的尾气中氮氧化合物的含量为2490mg/m3(体积已换算成标准状况),其中NO NO2的物质的量比为4:1。设尾气中氮氧化物与氨氧混合气恰好完全反应。(1)尾气中氮氧化物的平均相对原子量为
(2)要处理5m3的尾气,需要氨氧混合气的体积为
另一种处理氮氧化物的方法是用烧碱进行吸收,产物为NaNO2、NaNO3和H2O。现有含0.5mol氮氧化物的尾气,恰好被一定体积25%NaOH溶液(密度1.28g/cm3)完全吸收。
(3)NaOH溶液的物质的量浓度为
(4)已知反应后溶液含有0.35molNaNO2。若将尾气NO 和NO2的平均组成用NOx表示,则x=
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】我国农业因遭受酸雨而造成的损失每年高达15亿多元,为了有效控制酸雨,目前国务院已批准了《酸雨控制区和二氧化硫污染控制区划分方案》等法规。
(1)现有雨水样品1份,每隔一段时间测定该雨水样品的pH所得数据如下:
分析数据,回答以下问题:
①雨水样品呈酸性的原因是________________________________ (用化学方程式表示)。
②如果将刚取样的上述雨水和自来水(含有氯气)混合,pH将________ (填“变大”“变小”或“不变”)。
(2)测定雨水样品时,每隔一定时间测定一次pH,发现pH逐渐变小,其原因可能是_______ (用化学方程式表示)。
(3)举一例说明这种雨水将给环境中的生物或非生物造成的影响________________ 。
(1)现有雨水样品1份,每隔一段时间测定该雨水样品的pH所得数据如下:
测试时间/h | 0 | 1 | 2 | 3 | 4 |
雨水的pH | 4.75 | 4.62 | 4.56 | 4.55 | 4.54 |
分析数据,回答以下问题:
①雨水样品呈酸性的原因是
②如果将刚取样的上述雨水和自来水(含有氯气)混合,pH将
(2)测定雨水样品时,每隔一定时间测定一次pH,发现pH逐渐变小,其原因可能是
(3)举一例说明这种雨水将给环境中的生物或非生物造成的影响
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】化学与资源利用、材料研制、环境保护等密切相关。
(1)海水中蕴含的元素有80多种,它是一个巨大的宝藏。
①海水中镁的总储量约为1.8×1015 t,海水里镁的存在形式主要是_________ 。(填“游离态”或“化合态”)
②下列物质不经过化学变化就能从海水中获得的是_______ 。(填字母)
A.单质钠 B.单质钾 C.氯化钠
(2)保持洁净安全的生存环境已成为全人类的共识。
①pH<________ 的雨水称为酸雨。
②下列物质中,会破坏臭氧层的是________ 。(填字母)
A.氮气 B.一氧化碳 C.氟氯烃
③在生产中,人们曾用浓氨水来检验氯气管道是否漏气,已知能发生的反应为(在有水蒸气存在时):2NH3 +3Cl2=6HCl + N2,则如果氯气管道某处漏气,用该方法检查时的现象是________ 。
(1)海水中蕴含的元素有80多种,它是一个巨大的宝藏。
①海水中镁的总储量约为1.8×1015 t,海水里镁的存在形式主要是
②下列物质不经过化学变化就能从海水中获得的是
A.单质钠 B.单质钾 C.氯化钠
(2)保持洁净安全的生存环境已成为全人类的共识。
①pH<
②下列物质中,会破坏臭氧层的是
A.氮气 B.一氧化碳 C.氟氯烃
③在生产中,人们曾用浓氨水来检验氯气管道是否漏气,已知能发生的反应为(在有水蒸气存在时):2NH3 +3Cl2=6HCl + N2,则如果氯气管道某处漏气,用该方法检查时的现象是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】氮的氧化物是主要的大气污染物,必须脱除才能排放。
(1)臭氧与空气中的氮氧化物和_______ (填字母)在紫外线照射下产生光化学烟雾。
a.二氧化硫 b.碳氢化合物 c.二氧化碳
(2)汽车排气管内的催化剂能将CO和 转化为无害气体,发生的反应方程式为
转化为无害气体,发生的反应方程式为_______ 。
(3)工业上在催化剂作用下用 还原废气中
还原废气中 生成
生成 和
和 达到脱除目的,但当温度高于400℃时,
达到脱除目的,但当温度高于400℃时, 脱除率下降,原因可能是
脱除率下降,原因可能是_______ 。
(4)工业上氮的氧化物通常是用碱性溶液吸收。
①用 溶液吸收硝酸工业尾气中的
溶液吸收硝酸工业尾气中的 ,生成等物质的量的两种钠盐(一种为
,生成等物质的量的两种钠盐(一种为 )及一种气体,反应的离子方程式为
)及一种气体,反应的离子方程式为_______ 。
②NaOH溶液浓度越大黏稠度越高,用不同浓度的NaOH溶液吸收 (混有NO)含量不同的工业尾气,氮氧化物的吸收率随NaOH溶液浓度的变化如题图所示,曲线II表示NO的物质的量
(混有NO)含量不同的工业尾气,氮氧化物的吸收率随NaOH溶液浓度的变化如题图所示,曲线II表示NO的物质的量_______ (填:“大于”、“小于”、“等于”) 物质的量:当NaOH溶液浓度高于
物质的量:当NaOH溶液浓度高于 后,氮氧化物的吸收率随NaOH溶液浓度的升高而降低的原因是
后,氮氧化物的吸收率随NaOH溶液浓度的升高而降低的原因是_______ 。

(1)臭氧与空气中的氮氧化物和
a.二氧化硫 b.碳氢化合物 c.二氧化碳
(2)汽车排气管内的催化剂能将CO和
 转化为无害气体,发生的反应方程式为
转化为无害气体,发生的反应方程式为(3)工业上在催化剂作用下用
 还原废气中
还原废气中 生成
生成 和
和 达到脱除目的,但当温度高于400℃时,
达到脱除目的,但当温度高于400℃时, 脱除率下降,原因可能是
脱除率下降,原因可能是(4)工业上氮的氧化物通常是用碱性溶液吸收。
①用
 溶液吸收硝酸工业尾气中的
溶液吸收硝酸工业尾气中的 ,生成等物质的量的两种钠盐(一种为
,生成等物质的量的两种钠盐(一种为 )及一种气体,反应的离子方程式为
)及一种气体,反应的离子方程式为②NaOH溶液浓度越大黏稠度越高,用不同浓度的NaOH溶液吸收
 (混有NO)含量不同的工业尾气,氮氧化物的吸收率随NaOH溶液浓度的变化如题图所示,曲线II表示NO的物质的量
(混有NO)含量不同的工业尾气,氮氧化物的吸收率随NaOH溶液浓度的变化如题图所示,曲线II表示NO的物质的量 物质的量:当NaOH溶液浓度高于
物质的量:当NaOH溶液浓度高于 后,氮氧化物的吸收率随NaOH溶液浓度的升高而降低的原因是
后,氮氧化物的吸收率随NaOH溶液浓度的升高而降低的原因是
您最近一年使用:0次



