下列说法正确的是( )
| A.碱金属元素单质的熔点随原子序数递增而降低 |
| B.同种元素的原子均有相同的质子数和中子数 |
| C.族序数等于其周期序数的元素一定是金属元素 |
| D.ⅦA 族元素的阴离子还原性越强,其最高价氧化物对应水化物的酸性越强 |
17-18高一下·湖北襄阳·期中 查看更多[3]
【全国校级联考】湖北省襄阳市四校(襄州一中、枣阳一中、宜城一中、曾都一中)2017-2018学年高一下学期期中联考化学试题河北省衡水市桃城区第十四中学2019-2020学年高一下学期一调考试化学试题(已下线)练习15 元素周期表的应用-2020-2021学年【补习教材·寒假作业】高一化学(鲁科版2019)
更新时间:2018/05/01 11:05:26
|
相似题推荐
单选题
|
较易
(0.85)
名校
解题方法
【推荐1】下列事实不能说明元素的金属性或非金属性相对强弱的是
| 选项 | 事实 | 推论 |
| A | 与冷水反应,Na比Mg剧烈 | 金属性:Na>Mg |
| B | Ca(OH)2的碱性强于Mg(OH)2 | 金属性:Ca>Mg |
| C | 氧化性:HClO>H2CO3 | 金属性:Cl>C |
| D | 热稳定性强弱:HBr>HI | 非金属性:Br>I |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐2】下列单质最难与氢气化合的是
| A.S | B.O2 | C.Cl2 | D.F2 |
您最近一年使用:0次
单选题
|
较易
(0.85)
解题方法
【推荐1】下列有关性质的比较,不能用元素周期律解释的是( )
| A.非金属性:Cl > Br | B.酸性:HCl> H2S |
| C.离子半径:O2->Na+ | D.热稳定性:NH3 > PH3 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐2】1911年卢瑟福用α粒子(即氦核 )轰击
)轰击 ,得到
,得到 ,由此发现了质子(
,由此发现了质子( ):
): +
+ →
→ +
+ 。下列叙述
。下列叙述不正确 的是
 )轰击
)轰击 ,得到
,得到 ,由此发现了质子(
,由此发现了质子( ):
): +
+ →
→ +
+ 。下列叙述
。下列叙述A. 的中子数为9 的中子数为9 | B.原子半径:O>N |
| C.非金属性:O>N | D.稳定性:H2O>NH3 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐3】下列说法正确的有
①在周期表中,同周期第ⅡA族和第ⅢA族元素质子数相差可能是1、11或25
②同主族元素从上至下,单质的氧化性逐渐减弱,熔点逐渐降低
③碱性:LiOH>NaOH>KOH>RbOH
④酸性:H2SO4>HClO4>HBrO4>HIO4
⑤卤族元素由上至下,阴离子的还原性增强,单质的颜色加深
⑥碱金属单质物理通性是硬度小,密度小,熔点低
⑦碱金属元素的原子半径和离子半径都随核电荷数的增大而增大
⑧可以利用非金属单质与H2反应的难易程度来证明其元素非金属性的强弱
①在周期表中,同周期第ⅡA族和第ⅢA族元素质子数相差可能是1、11或25
②同主族元素从上至下,单质的氧化性逐渐减弱,熔点逐渐降低
③碱性:LiOH>NaOH>KOH>RbOH
④酸性:H2SO4>HClO4>HBrO4>HIO4
⑤卤族元素由上至下,阴离子的还原性增强,单质的颜色加深
⑥碱金属单质物理通性是硬度小,密度小,熔点低
⑦碱金属元素的原子半径和离子半径都随核电荷数的增大而增大
⑧可以利用非金属单质与H2反应的难易程度来证明其元素非金属性的强弱
| A.4个 | B.5个 | C.6个 | D.7个 |
您最近一年使用:0次
单选题
|
较易
(0.85)
解题方法
【推荐1】X、Y、Z、W均为短周期元素,它们在元素周期表中的相对位置如图所示,Z的原子为所在周期中未成对电子数最多的原子。下列说法正确的是


A.第一电离能: | B.Z、W最高价氧化物对应水化物均为一元酸 |
| C.X、Y、W的最高正化合价依次增大 | D.氢化物的熔沸点: |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐2】短周期主族元素W、X、Y、Z的原子序数依次增大,W与Y同族,X的单质既能与盐酸反应也能与NaOH溶液反应,Y原子的最外层电子数是次外层电子数的一半,X、Y、Z原子的最外层电子数之和为14。下列说法错误的是
| A.原子半径:X> Y> Z> W |
| B.X与Z形成的化合物能促进水电离 |
| C.最高价氧化物对应的水化物的酸性:Z> W> Y |
| D.W与Y可形成离子化合物YW |
您最近一年使用:0次

 和
和 向外界泄漏。下列相关说法正确的是
向外界泄漏。下列相关说法正确的是 与
与 可发生反应:
可发生反应: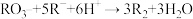 下列关于R元素的叙述中,正确的是(
下列关于R元素的叙述中,正确的是(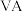 族
族 在常温常压下一定是气体
在常温常压下一定是气体

