黄铜矿(CuFeS2)是制取铜及其化合物的主要原料之一,还可制备硫和铁的化合物。
(1)冶炼铜的反应为8CuFeS2+21O2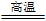 8Cu+4FeO+2Fe2O3+16SO2。若CuFeS2中Fe的化合价为+2,反应中被还原的元素是
8Cu+4FeO+2Fe2O3+16SO2。若CuFeS2中Fe的化合价为+2,反应中被还原的元素是________ (填元素符号)。
(2)上述冶炼过程产生大量SO2。下列处理方案中合理的是________ (填代号)。
a.高空排放 b.用于制备硫酸
c.用纯碱溶液吸收制Na2SO3 d.用浓硫酸吸收
(3)利用黄铜矿冶炼铜产生的炉渣(含Fe2O3、FeO、SiO2、Al2O3)可制备Fe2O3。方法为:
①用稀盐酸浸取炉渣,过滤。
②滤液先氧化,再加入过量NaOH溶液,过滤,将沉淀洗涤、干燥、煅烧得Fe2O3。
根据以上信息回答下列问题:
a.除去Al3+的离子方程式是_____________________________________________________ 。
b.选用提供的试剂,设计实验验证炉渣中含有FeO。
提供的试剂:稀盐酸 稀硫酸 KSCN溶液 KMnO4溶液 NaOH溶液 碘水
所选试剂为________ 。证明炉渣中含有FeO的实验现象为_______________________ 。
(1)冶炼铜的反应为8CuFeS2+21O2
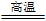 8Cu+4FeO+2Fe2O3+16SO2。若CuFeS2中Fe的化合价为+2,反应中被还原的元素是
8Cu+4FeO+2Fe2O3+16SO2。若CuFeS2中Fe的化合价为+2,反应中被还原的元素是(2)上述冶炼过程产生大量SO2。下列处理方案中合理的是
a.高空排放 b.用于制备硫酸
c.用纯碱溶液吸收制Na2SO3 d.用浓硫酸吸收
(3)利用黄铜矿冶炼铜产生的炉渣(含Fe2O3、FeO、SiO2、Al2O3)可制备Fe2O3。方法为:
①用稀盐酸浸取炉渣,过滤。
②滤液先氧化,再加入过量NaOH溶液,过滤,将沉淀洗涤、干燥、煅烧得Fe2O3。
根据以上信息回答下列问题:
a.除去Al3+的离子方程式是
b.选用提供的试剂,设计实验验证炉渣中含有FeO。
提供的试剂:稀盐酸 稀硫酸 KSCN溶液 KMnO4溶液 NaOH溶液 碘水
所选试剂为
13-14高一·全国·课时练习 查看更多[4]
苏教版高一化学必修2专题4《化学科学与人类文明》测试卷苏教版高中化学必修2专题四《化学科学与人类文明》测试卷【全国市级联考】贵州省毕节市2017-2018学年高一毕业学业达标模拟考试化学试题(已下线)2014年高一化学人教版必修二 4-1-1金属矿物的开发利用练习卷
更新时间:2018-06-27 11:37:16
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】氧化还原反应原理在生产生活和科学研究中应用广泛。
(1)下列表述中没有氧化还原反应发生的是_____ 。
a.滴水成冰 b.蜡炬成灰 c.百炼成钢
(2)NH3和Cl2反应的方程式为:NH3+Cl2—N2+HCl
①该反应中被氧化的元素是___ (填元素名称),氧化剂是__ (填化学式)。
②配平该方程式:____ NH3+ ____ Cl2—____ N2+____ HCl
③工业生产中常用喷洒氨水的方法来检查是否有Cl2泄漏,若Cl2有泄漏,可以观察到的现象是______ ,产生该现象的反应方程式为___ 。
(3)“地康法”制氯气的反应原理图示如下:
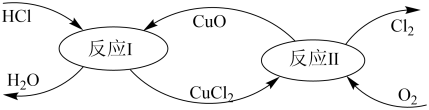
①反应I的化学方程式为____ 。
②若要制得标准状况下氯气11.2L,则整个反应中转移电子的物质的量为____ 。
(1)下列表述中没有氧化还原反应发生的是
a.滴水成冰 b.蜡炬成灰 c.百炼成钢
(2)NH3和Cl2反应的方程式为:NH3+Cl2—N2+HCl
①该反应中被氧化的元素是
②配平该方程式:
③工业生产中常用喷洒氨水的方法来检查是否有Cl2泄漏,若Cl2有泄漏,可以观察到的现象是
(3)“地康法”制氯气的反应原理图示如下:

①反应I的化学方程式为
②若要制得标准状况下氯气11.2L,则整个反应中转移电子的物质的量为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】Na2O2是重要的化工原料,具有多种用途。
(1)Na2O2可在呼吸面具和潜水艇中作为氧气的来源,请写出Na2O2与CO2反应的化学方程式________ 。
(2)查阅资料知:Na2O2在一定条件下可以转化为NaNO2,NaNO2易溶于水且溶解时吸热,有咸味,遇酸易放出气体,人误食会中毒。
请回答下列问题:
①已知NaNO2能发生如下反应:2NaNO2+4HI=2NO↑+I2+2NaI+2H2O。上述反应中氧化剂是________ ,氧化产物是________ ;HI在反应中体现了________ 性。
②某厂废液中含有3%—6%的NaNO2,直接排放会造成污染,下列试剂能使NaNO2转化为不引起二次污染的N2的是________ 。
A.浓硫酸 B.NH4Cl C.HNO3 D.KMnO4
(1)Na2O2可在呼吸面具和潜水艇中作为氧气的来源,请写出Na2O2与CO2反应的化学方程式
(2)查阅资料知:Na2O2在一定条件下可以转化为NaNO2,NaNO2易溶于水且溶解时吸热,有咸味,遇酸易放出气体,人误食会中毒。
请回答下列问题:
①已知NaNO2能发生如下反应:2NaNO2+4HI=2NO↑+I2+2NaI+2H2O。上述反应中氧化剂是
②某厂废液中含有3%—6%的NaNO2,直接排放会造成污染,下列试剂能使NaNO2转化为不引起二次污染的N2的是
A.浓硫酸 B.NH4Cl C.HNO3 D.KMnO4
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】回答下列问题:
(1)人体血红蛋白分子中含有Fe2+,正是这些Fe2+使血红蛋白分子具有载氧功能。亚硝酸钠(NaNO2)可将人体血红蛋白中的Fe2+转化为Fe3+,生成高铁血红蛋白而丧失与氧气的结合能力,反应过程中Fe2+发生___________ 反应,说明亚硝酸钠具有___________ 性;误食亚硝酸钠中毒,可服维生素C缓解,说明维生素C具有___________ 性。
(2)稀土氟化物是金属热还原法制取单一稀土金属的重要原料。微波法合成CeF3的化学方程式为6CeO2+18NH4F=6CeF3+16NH3↑+12H2O+N2↑,该反应中氧化剂是___________ ,还原剂是___________ ,反应中被氧化的氮原子与未被氧化的氮原子物质的量之比为___________ 。
(3)近年来,锂的含氢化合物作为氢源受到广泛关注。化合物LiNH2和LiH都是具有潜在应用价值的释氢材料。将LiNH2和LiH按一定比例混合,在催化剂作用下,所含氢全部以氢气形式放出同时生成Li3N,反应的化学方程式为___________ 。
(1)人体血红蛋白分子中含有Fe2+,正是这些Fe2+使血红蛋白分子具有载氧功能。亚硝酸钠(NaNO2)可将人体血红蛋白中的Fe2+转化为Fe3+,生成高铁血红蛋白而丧失与氧气的结合能力,反应过程中Fe2+发生
(2)稀土氟化物是金属热还原法制取单一稀土金属的重要原料。微波法合成CeF3的化学方程式为6CeO2+18NH4F=6CeF3+16NH3↑+12H2O+N2↑,该反应中氧化剂是
(3)近年来,锂的含氢化合物作为氢源受到广泛关注。化合物LiNH2和LiH都是具有潜在应用价值的释氢材料。将LiNH2和LiH按一定比例混合,在催化剂作用下,所含氢全部以氢气形式放出同时生成Li3N,反应的化学方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】为了达到下表的实验目的,请选择合适的试剂及实验方法,并将其标号填入对应的空格。
A.加热升华
B.向溶液中加入足量CO2气体
C.分别加入品红溶液中,观察现象
D.分别加入紫色石蕊试剂中,观察现象
E.加入硫酸铜固体观察现象
| 序号 | 实验目的 | 试剂及方法 |
| (1) | 鉴别CO2和SO2气体 | |
| (2) | 除去食盐中混有的少量碘 | |
| (3) | 检验无水乙醇中是否含有水 | |
| (4) | 除去NaHCO3溶液中混有的Na2CO3 |
B.向溶液中加入足量CO2气体
C.分别加入品红溶液中,观察现象
D.分别加入紫色石蕊试剂中,观察现象
E.加入硫酸铜固体观察现象
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】 是常见的主要大气污染物质。某学习小组利用如图探究
是常见的主要大气污染物质。某学习小组利用如图探究 的部分性质,进行以下系列实验。请回答下列问题:
的部分性质,进行以下系列实验。请回答下列问题: 的是
的是___________ (填序号)。
① 浴液与稀硝酸 ②
浴液与稀硝酸 ② 固体与浓硫酸 ③固体硫在氧气中燃烧
固体与浓硫酸 ③固体硫在氧气中燃烧
浓 与铜反应也可以制取
与铜反应也可以制取 ,写出反应的化学方程式
,写出反应的化学方程式___________ 。
(2)当足量的 进入装置A中后,品红溶液将
进入装置A中后,品红溶液将___________ (填“褪色”或“不褪色”),说明 具有
具有___________ (填“氧化性”或“漂白性”)。
(3)当 进入装置B中后,
进入装置B中后, 黄色溶液变浅绿色,说明
黄色溶液变浅绿色,说明 具有
具有___________ (填“氧化性”或“还原性”)。
(4)当 不断通入装置C中,含淀粉的碘水溶液由蓝色逐渐褪为无色,反应的化学方程式表示为
不断通入装置C中,含淀粉的碘水溶液由蓝色逐渐褪为无色,反应的化学方程式表示为___________ 。
(5)当 进入装置D中后,溶液中产生白色沉淀,其化学式为
进入装置D中后,溶液中产生白色沉淀,其化学式为___________ ,反应的离子方程式表示为___________ 。
 是常见的主要大气污染物质。某学习小组利用如图探究
是常见的主要大气污染物质。某学习小组利用如图探究 的部分性质,进行以下系列实验。请回答下列问题:
的部分性质,进行以下系列实验。请回答下列问题: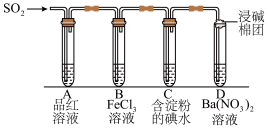
 的是
的是①
 浴液与稀硝酸 ②
浴液与稀硝酸 ② 固体与浓硫酸 ③固体硫在氧气中燃烧
固体与浓硫酸 ③固体硫在氧气中燃烧浓
 与铜反应也可以制取
与铜反应也可以制取 ,写出反应的化学方程式
,写出反应的化学方程式(2)当足量的
 进入装置A中后,品红溶液将
进入装置A中后,品红溶液将 具有
具有(3)当
 进入装置B中后,
进入装置B中后, 黄色溶液变浅绿色,说明
黄色溶液变浅绿色,说明 具有
具有(4)当
 不断通入装置C中,含淀粉的碘水溶液由蓝色逐渐褪为无色,反应的化学方程式表示为
不断通入装置C中,含淀粉的碘水溶液由蓝色逐渐褪为无色,反应的化学方程式表示为(5)当
 进入装置D中后,溶液中产生白色沉淀,其化学式为
进入装置D中后,溶液中产生白色沉淀,其化学式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】副产品Y主要含氢氧化铝,还含少量镁、铁的难溶化合物及可溶性杂质,精确分析Y中氢氧化铝含量的方法是称取n g样品,加入过量______ (填写试剂)、溶解、过滤、再通入足量______ (填写试剂)、……灼烧、冷却、称量,得干燥固体mg。计算样品中氢氧化铝的质量分数为_______ (用含m、n的代数式表示)。
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】在某无色溶液中缓慢地滴入NaOH溶液直至过量,产生沉淀的质量与加入的NaOH溶液体积的关系如图所示,由此确定

(1)原溶液中含有的阳离子是( )
A.Mg2+、Al3+、Fe2+ B.H+、Mg2+、Al3+
C.H+、Ba2+、Al3+ D.只有Mg2+、Al3+
(2)若原溶液的体积为100mL,生成沉淀的最大质量为10.7g,最终生成沉淀的质量为2.9g,则原溶液中Al3+的物质的量浓度为____ 。

(1)原溶液中含有的阳离子是
A.Mg2+、Al3+、Fe2+ B.H+、Mg2+、Al3+
C.H+、Ba2+、Al3+ D.只有Mg2+、Al3+
(2)若原溶液的体积为100mL,生成沉淀的最大质量为10.7g,最终生成沉淀的质量为2.9g,则原溶液中Al3+的物质的量浓度为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】将一定质量的镁铝混合物投入200 mL硫酸中,固体全部溶解后,向所得溶液中加入5 mol/L的NaOH溶液,生成沉淀的物质的量n与加入NaOH溶液的体积V的变化如图所示。
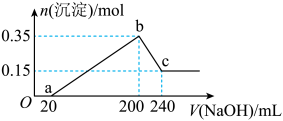
(1)写出Al与NaOH溶液反应的化学方程式___________________ ;
(2)镁和铝的总质量为________ g;
(3)b点溶液中的溶质为__________ ,硫酸的物质的量浓度为___________ mol/L;
(4)生成的氢气在标准状况下的体积为__________ L;
(5)c点溶液中通入足量的CO2的反应化学方程式为___________ 。

(1)写出Al与NaOH溶液反应的化学方程式
(2)镁和铝的总质量为
(3)b点溶液中的溶质为
(4)生成的氢气在标准状况下的体积为
(5)c点溶液中通入足量的CO2的反应化学方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】利用废旧镀锌铁皮制备磁性Fe3O4胶体粒子及副产物ZnO,制备流程图如下:
已知:Zn及其化合物的性质与Al及其化合物的性质相似。
(1)步骤Ⅰ中所用的试剂是______________ 。
(2)步骤Ⅲ中反应的离子方程式是_________________ 。
(3)步骤Ⅴ可选用的试剂是__________ (填序号)。
a.NaOH溶液 b.氨水 c.盐酸
(4)步骤Ⅵ的实验操作是_________________ 。

已知:Zn及其化合物的性质与Al及其化合物的性质相似。
(1)步骤Ⅰ中所用的试剂是
(2)步骤Ⅲ中反应的离子方程式是
(3)步骤Ⅴ可选用的试剂是
a.NaOH溶液 b.氨水 c.盐酸
(4)步骤Ⅵ的实验操作是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】一种反应物的两种或两种以上的组成离子,都能跟另一种反应物的组成离子反应,但因反应次序不同而跟用量有关,又可称为竞争型。
(1) 溶液与
溶液与 溶液的反应:
溶液的反应:
 不足:
不足:_______ ;
 过量:
过量:_______ 。
(2)向含有 的溶液中,逐滴加入
的溶液中,逐滴加入 溶液至过量,反应依次为:
溶液至过量,反应依次为:
_______ ;
_______ ;
_______ ;
_______ 。
(3)向含有 的溶液中,逐滴加入稀盐酸至过量,反应依次为:
的溶液中,逐滴加入稀盐酸至过量,反应依次为:
_______ ;
_______ ;
_______ ;
_______ 。
(4)向 溶液中通
溶液中通 :
:
 少量:
少量:_______ ;
 过量:
过量:_______ 。
(1)
 溶液与
溶液与 溶液的反应:
溶液的反应: 不足:
不足: 过量:
过量:(2)向含有
 的溶液中,逐滴加入
的溶液中,逐滴加入 溶液至过量,反应依次为:
溶液至过量,反应依次为:(3)向含有
 的溶液中,逐滴加入稀盐酸至过量,反应依次为:
的溶液中,逐滴加入稀盐酸至过量,反应依次为:(4)向
 溶液中通
溶液中通 :
: 少量:
少量: 过量:
过量:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】铁、铜单质及其化合物应用范围很广。现有含氯化亚铁杂质的氯化铜晶体( ),为制取纯净的
),为制取纯净的 ,某兴趣小组首先将其制成水溶液。
,某兴趣小组首先将其制成水溶液。
(1)通常将氢氧化钠溶液加入氯化亚铁溶液的实验现象是__________________________________ ,书写氢氧化亚铁在空气中转化为氢氧化铁的化学方程式________________________________ 。
(2)已知pH=1.9时,Fe3+就能开始沉淀,因此可首先加入氧化剂将Fe2+氧化后再除去,下列氧化剂最适合的是___________ 。
A. NaClO B. H2O2 C. KMnO4 D. 浓硫酸
(3)在所得的FeCl3、CuCl2混合溶液中加入镁粉,产生的气体是______ 。试解释原因:__________________________________________________ 。有同学提出加入CuO以除去Fe3+。你认为理由是___________________________________________________________________ 。
(4)能不能直接蒸发CuCl2溶液得到 晶体?
晶体?__________ (填“能”或“不能”)。若能,不用回答;若不能,说明理由______________________________________________________ 。经检测, 中含水28.6%,则
中含水28.6%,则 中
中 的值为
的值为___________ 。
 ),为制取纯净的
),为制取纯净的 ,某兴趣小组首先将其制成水溶液。
,某兴趣小组首先将其制成水溶液。(1)通常将氢氧化钠溶液加入氯化亚铁溶液的实验现象是
(2)已知pH=1.9时,Fe3+就能开始沉淀,因此可首先加入氧化剂将Fe2+氧化后再除去,下列氧化剂最适合的是
A. NaClO B. H2O2 C. KMnO4 D. 浓硫酸
(3)在所得的FeCl3、CuCl2混合溶液中加入镁粉,产生的气体是
(4)能不能直接蒸发CuCl2溶液得到
 晶体?
晶体? 中含水28.6%,则
中含水28.6%,则 中
中 的值为
的值为
您最近一年使用:0次

 )的黄铁矿(
)的黄铁矿( )样品,将其在氧气流中充分灼烧,反应完全后得0.78g残渣。
)样品,将其在氧气流中充分灼烧,反应完全后得0.78g残渣。

