苯与Br2发生取代反应时能量与反应进程如下图所示。下列说法正确的是
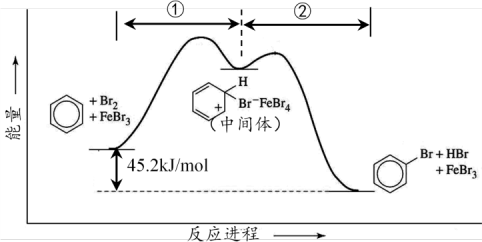

| A.①、②两步均放出能量 | B.FeBr3可以改变反应的焓变 |
| C.FeBr3不能改变反应的活化能 | D.FeBr3可以加快该反应速率 |
更新时间:2018-07-01 18:58:37
|
相似题推荐
【推荐1】中国学者在水煤气变换[CO(g)+H2O(g) CO2(g)+H2(g) △H]中攻克了低温下高转化率与高反应速率不能兼得的难题,该过程是基于双功能催化剂(能吸附不同粒子)催化实现的。反应过程示意图如下:
CO2(g)+H2(g) △H]中攻克了低温下高转化率与高反应速率不能兼得的难题,该过程是基于双功能催化剂(能吸附不同粒子)催化实现的。反应过程示意图如下:
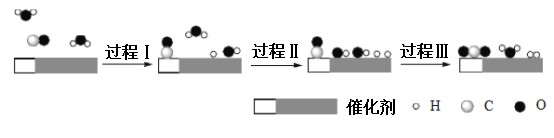
下列说法正确的是
 CO2(g)+H2(g) △H]中攻克了低温下高转化率与高反应速率不能兼得的难题,该过程是基于双功能催化剂(能吸附不同粒子)催化实现的。反应过程示意图如下:
CO2(g)+H2(g) △H]中攻克了低温下高转化率与高反应速率不能兼得的难题,该过程是基于双功能催化剂(能吸附不同粒子)催化实现的。反应过程示意图如下:
下列说法正确的是
| A.无催化剂时,该反应不会发生 |
| B.过程I、过程II、过程III均为放热过程 |
| C.使用催化剂可以提高CO的平衡转化率 |
| D.过程III既形成了极性共价键,也形成了非极性键 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】有关化学反应原理的说法正确的是
| A.对任何化学反应来说,反应速率越大,反应现象就越明显 |
| B.反应物的热效应与是否使用催化剂无关 |
C.已知中和热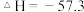  ,则1mol浓 ,则1mol浓 和1mol 和1mol  的反应热 的反应热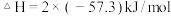 |
D.向 溶液中通入少量HCl气体,溶液的导电性明显增强 溶液中通入少量HCl气体,溶液的导电性明显增强 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】①101 kPa时,2C(s)+O2(g)===2CO(g)ΔH=-221 kJ·mol-1
②2H2(g)+O2=2H2O(l)ΔH=-572kJ·mol-1
③稀溶液中,H+(aq)+OH-(aq)===H2O(l)ΔH=-57.3 kJ·mol-1,下列结论正确的是
②2H2(g)+O2=2H2O(l)ΔH=-572kJ·mol-1
③稀溶液中,H+(aq)+OH-(aq)===H2O(l)ΔH=-57.3 kJ·mol-1,下列结论正确的是
| A.碳的燃烧热大于110.5 kJ·mol-1 | B.氢气的热值为143kJ·g-1 |
| C.浓硫酸与稀NaOH溶液反应的成1 mol水,放出57.3 kJ热量 | D.稀醋酸与稀NaOH溶液反应生成1 mol水,放出57.3 kJ热量 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】下列说法正确的是( )
| A.化学反应的热效应的大小与参加反应的物质的多少无关 |
| B.由H+(aq)+OH-(aq)=H2O(l) ΔH=-57.3 kJ·mol-1,则向含0.1 mol HCl的盐酸中加入4.0 gNaOH固体,放出热量等于5.73 kJ |
| C.同温同压下,反应H2(g)+Cl2(g)=2HCl(g)在光照和点燃条件下的△H不同 |
| D.反应物的总能量大于生成物的总能量的反应一定是放热反应 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】已知A转化为D和E分步进行:①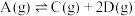 ,②
,②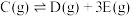 ,其反应过程能量变化如图所示,下列说法
,其反应过程能量变化如图所示,下列说法错误 的是

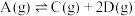 ,②
,②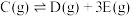 ,其反应过程能量变化如图所示,下列说法
,其反应过程能量变化如图所示,下列说法
A.整个反应的活化能为 |
| B.A转化为D和E的反应为吸热反应 |
| C.使用合适的催化剂可以降低反应的活化能,提高活化分子百分数 |
| D.第一步反应的速率小于第二步反应的速率 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】甲烷水蒸气重整制合成气[
 ]是利用甲烷资源的途径之一、其他条件相同时,在不同催化剂(
]是利用甲烷资源的途径之一、其他条件相同时,在不同催化剂( 、
、 、
、 )作用下,反应相同时间后,
)作用下,反应相同时间后, 的转化率随反应温度的变化如下图所示。下列说法错误的是
的转化率随反应温度的变化如下图所示。下列说法错误的是

 ]是利用甲烷资源的途径之一、其他条件相同时,在不同催化剂(
]是利用甲烷资源的途径之一、其他条件相同时,在不同催化剂( 、
、 、
、 )作用下,反应相同时间后,
)作用下,反应相同时间后, 的转化率随反应温度的变化如下图所示。下列说法错误的是
的转化率随反应温度的变化如下图所示。下列说法错误的是
A.该反应 | B.平衡常数: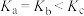 |
C.催化剂催化效率: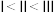 | D.增大压强, 增大倍数小于 增大倍数小于 增大倍数 增大倍数 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】根据实验目的,下列实验现象、结论都正确的是
| 选项 | 实验目的 | 实验过程 | 现象及结论 |
| A | 测定中和反应的反应热 | 测定浓度均为1.0  和 和 溶液初始温度 溶液初始温度 。快速将体积均为100 。快速将体积均为100 的 的 和 和 溶液倒入量热计中,盖好杯盖,轻轻搅拌,记录体系的最高温度 溶液倒入量热计中,盖好杯盖,轻轻搅拌,记录体系的最高温度 。 。 |  和 和 溶液密度近似为1 溶液密度近似为1 ,溶液的比热容4.18 ,溶液的比热容4.18 。中和反应的反应热: 。中和反应的反应热: 。 。 |
| B | 探究铁钉镀铜 | 直流电源正极、负极分别与铁钉、铜片连接,将铁钉和铜片插入 溶液中,接通电源。 溶液中,接通电源。 | 铜片逐渐溶解,铁钉表面有红色物质析出。 |
| C | 探究浓度对化学平衡的影响 | 向 溶液中缓慢滴加硫酸,溶液由黄色变为橙色。 溶液中缓慢滴加硫酸,溶液由黄色变为橙色。 | 增大 浓度,化学平衡向生成 浓度,化学平衡向生成 的方向移动。 的方向移动。 |
| D | 探究不同催化剂的催化效果 | 向两支试管中各加入2 10% 10% 溶液,再分别加入2滴1 溶液,再分别加入2滴1  溶液、2滴1 溶液、2滴1  溶液。 溶液。 | 滴加 溶液的试管产生气泡的速率快,说明 溶液的试管产生气泡的速率快,说明 的催化效果好。 的催化效果好。 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次

 在
在  中完全燃烧,生成
中完全燃烧,生成  比生成
比生成  放出的热量多
放出的热量多 在光照和点燃条件下的
在光照和点燃条件下的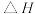 不同
不同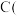 金刚石,
金刚石, 石墨,
石墨,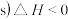
 CO2(g)+H2(g)
CO2(g)+H2(g)

