下列各物质或微粒性质的比较中正确的是
| A.粒子半径:K+>O2->Al3+>S2->Cl- | B.离子的还原性:S2->Cl->Br->I- |
| C.酸性:HClO>H2SO4>H3PO4>H2SiO3 | D.稳定性:H2O>NH3>PH3>SiH4 |
更新时间:2018-07-17 20:23:11
|
相似题推荐
单选题
|
较难
(0.4)
名校
【推荐1】电子级氢氟酸是微电子行业的关键性基础材料之一,由萤石粉(主要成分为 ,含有少量
,含有少量 和微量
和微量 等)制备工艺如下,下列有关说法
等)制备工艺如下,下列有关说法不正确 的是

 ,含有少量
,含有少量 和微量
和微量 等)制备工艺如下,下列有关说法
等)制备工艺如下,下列有关说法
A.“酸浸”时生成 的化学方程式为 的化学方程式为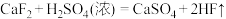 |
| B.工业生产时往往会适当加热,其目的是加快反应速率 |
| C.“精馏1”设备使用的材料可选用金或石英 |
D.已知 是一种配位酸,酸性与硝酸相近,可与 是一种配位酸,酸性与硝酸相近,可与 溶液反应制备极易溶于水的强酸 溶液反应制备极易溶于水的强酸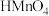 ,反应的离子方程式为 ,反应的离子方程式为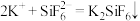 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】依据元素周期表判断,下列各组关系中正确的是
| A.稳定性:NH3>H2O>H2S |
| B.酸性:H3PO4>H2SO4>HClO4 |
| C.氧化性:Cl2>S>P |
| D.碱性:Mg(OH)2>Ca(OH)2>Ba(OH)2 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐1】下列递变规律正确的是
| A.LiOH、KOH、CsOH的碱性依次增强 | B.H2O、NH3、PH3的热稳定性依次增强 |
| C.HCl、BHr、HI的还原性依次减弱 | D.Na、Mg、Al的原子半径依次增大 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】如图是常温下部分短周期元素,最高价氧化物对应水化物的等物质的量浓度稀溶液的pH(pH=-lgc(H+) )与原子序数的关系图,其中H的氧化物是两性氧化物。下列说法正确的是
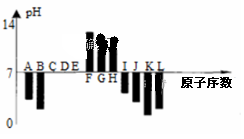

| A.元素B对应的氢化物比J对应的氢化物熔沸点更高,原因是B的氢化物中的键能比J中的大 |
| B.根据图形分析可知,K、L两种元素最高价氧化物对应的水化物的酸性,前者较强 |
| C.IC2熔化时克服的化学键和KL2与水反应时克服的化学键类型相同 |
| D.元素K、H、G分别形成的简单离子的半径逐渐减少 |
您最近一年使用:0次
单选题
|
较难
(0.4)
解题方法
【推荐3】短周期主族元素X、Y、Z、W的原子序数依次增大,K、L、M均是由这些元素组成的氧化物,甲、乙分别是元素Y、W的单质,甲是常见的固体,乙是常见的气体。K是红棕色气体,丙的浓溶液具有强氧化性,上述物质的转化关系如图所示。下列说法错误的是( )
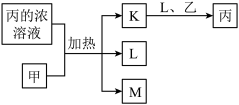

A.X、Y、Z三种元素的第一电离能: |
| B.X分别与Y、Z、W形成的分子中均可能含有非极性共价键 |
| C.Z元素的最高价含氧酸的酸性在同周期和同主族元素中均最强 |
D.若固体 是由直线形的 是由直线形的 和平面三角形的 和平面三角形的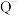 组成,则 组成,则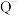 与丙溶液中的溶质阴离子相同 与丙溶液中的溶质阴离子相同 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐1】元素周期表隐含着许多信息和规律。以下所涉及的元素均为中学化学中常见的短周期元素,其原子半径及主要化合价列表如下,其中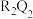 用于呼吸面具或潜水艇中作为氧气来源。
用于呼吸面具或潜水艇中作为氧气来源。
下列说法正确的是
 用于呼吸面具或潜水艇中作为氧气来源。
用于呼吸面具或潜水艇中作为氧气来源。元素代号 |
|
|
|
|
|
|
|
原子半径 | 0.037 | 0.186 | 0.074 | 0.102 | 0.150 | 0.160 | 0.099 |
主要化合价 |
|
|
|
|
|
|
|
A. 、 、 的最高价氧化物对应水化物的酸性 的最高价氧化物对应水化物的酸性 大于 大于 |
B. 、 、 、 、 的单质与同浓度酸反应最剧烈的是 的单质与同浓度酸反应最剧烈的是 |
C. 和 和 的最高价氧化物对应水化物能发生反应 的最高价氧化物对应水化物能发生反应 |
D. 、 、 、 、 都在第二周期 都在第二周期 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】依据元素周期表判断,下列各组关系中正确的是
| A.稳定性:NH3>H2O>H2S |
| B.酸性:H3PO4>H2SO4>HClO4 |
| C.氧化性:Cl2>S>P |
| D.碱性:Mg(OH)2>Ca(OH)2>Ba(OH)2 |
您最近一年使用:0次

 2溶液的pH比0.1mol/L Mg(NO3)2溶液小
2溶液的pH比0.1mol/L Mg(NO3)2溶液小 2溶液分别蒸干并灼烧,剩余固体成分相同
2溶液分别蒸干并灼烧,剩余固体成分相同


 、
、


 、
、
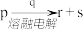 。下列说法正确的是(
。下列说法正确的是(

