下列关于Be、Mg及其化合物结构与性质的论述错误的是
| A.基态Mg原子有四种能量不同的电子 |
| B.Be(OH)2和Mg(OH)2均能溶于盐酸,均不溶于NaOH溶液 |
C.0.1 mol/L  2溶液的pH比0.1mol/L Mg(NO3)2溶液小 2溶液的pH比0.1mol/L Mg(NO3)2溶液小 |
D.MgCl2溶液与  2溶液分别蒸干并灼烧,剩余固体成分相同 2溶液分别蒸干并灼烧,剩余固体成分相同 |
更新时间:2024-04-29 10:29:43
|
相似题推荐
单选题
|
较难
(0.4)
名校
【推荐1】工业生产中,向Na2CO3溶液中通入SO2气体制备无水Na2SO3,水溶液中H2SO3、HSO3-、SO32-粒子的物质的量分数随pH的分布、Na2SO3的溶解度曲线如图所示:
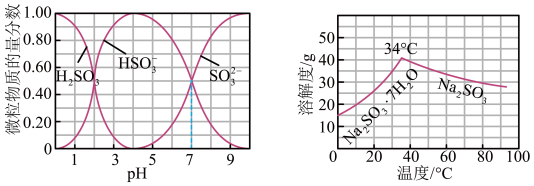
下列说法不正确 的是:

下列说法
| A.溶液pH=4时,溶质为NaHSO3 |
B.溶液pH=10时,c (Na+)+ c(H+)= c(OH–)+ c(SO32–)+ c(HSO3–) (Na+)+ c(H+)= c(OH–)+ c(SO32–)+ c(HSO3–) |
| C.溶液pH=7时, c(SO32–)= c(HSO3–) |
| D.溶液pH=10时,停止通入SO2,将溶液加热浓缩至有大量晶体析出,在高于34℃趁热过滤、洗涤、干燥得到无水Na2SO3 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】根据下列实验操作和现象所得到的结论正确的是
| 选项 | 结论 | 操作 |
| A | CO32-水解是吸热反应 | 在0.1 mol/LNa2CO3溶液中,滴加2滴酚酞显浅红色,微热,红色加深 |
| B | Ksp(BaSO4)>Ksp(BaCO3) | 常温下,用饱和Na2CO3溶液可将BaSO4全部转化为BaCO3 |
| C | 酸性A比B强 | 等体积、pH=3的两种酸HA和HB分别与足量的Zn反应,酸HA放出的氢气多 |
| D | 金属性:M>N | 由M、N与稀硫酸构成的原电池中,M上产生大量气泡 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐3】下面说法中,与盐类水解有关的有( )项
①NaHCO3做发酵粉时加入柠檬酸后效果更好
②FeCl2溶液中加入一定量的铁粉
③实验室配制AlCl3溶液,先把它溶解在浓盐酸中,而后加水稀释
④NH4F溶液不能保存在玻璃试剂瓶中
⑤实验室盛放Na2CO3、Na2SO3等溶液的试剂瓶应用橡皮塞
⑥在NH4Cl 或A1C13溶液中加入镁条会产生气泡
⑦Na2S溶液和A1C13溶液反应得不到Al2S3
⑧室温下NaHCO3饱和溶液pH约为8.4
⑨0.1mol/LA1C13溶液中c(A13+)<0.1mol/L
①NaHCO3做发酵粉时加入柠檬酸后效果更好
②FeCl2溶液中加入一定量的铁粉
③实验室配制AlCl3溶液,先把它溶解在浓盐酸中,而后加水稀释
④NH4F溶液不能保存在玻璃试剂瓶中
⑤实验室盛放Na2CO3、Na2SO3等溶液的试剂瓶应用橡皮塞
⑥在NH4Cl 或A1C13溶液中加入镁条会产生气泡
⑦Na2S溶液和A1C13溶液反应得不到Al2S3
⑧室温下NaHCO3饱和溶液pH约为8.4
⑨0.1mol/LA1C13溶液中c(A13+)<0.1mol/L
| A.5 | B.6 | C.7 | D.全有关 |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐1】X、Y、Z、W是原子序数依次增大的短周期主族元素。Y与W同主族,Z所在的族序数等于周期数,X、Y最外层电子数之和为7;X、Z原子的电子数总和与Y、W原子的电子数总和之比为7:12。下列说法正确的是( )
| A.原子半径:r(X)<r(Y)<r(Z)<r(W) |
| B.Y的简单气态氢化物的热稳定性比W的弱 |
| C.由X、Y组成的物质与由Y、W组成的物质化合,可能发生氧化还原反应 |
| D.常温下,Z的单质一定易溶于由X、Y、W三种元素组成的化合物的溶液 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】若已发现了116号元素则下列推断正确的是: 其钙盐的化学式为CaR;
其钙盐的化学式为CaR;  其最高价氧化物对应的水化物的酸性比硫酸弱;
其最高价氧化物对应的水化物的酸性比硫酸弱; 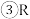 是金属元素;
是金属元素; 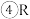 是非金属元素;
是非金属元素;  最外电子层有6个电子
最外电子层有6个电子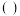
 其钙盐的化学式为CaR;
其钙盐的化学式为CaR;  其最高价氧化物对应的水化物的酸性比硫酸弱;
其最高价氧化物对应的水化物的酸性比硫酸弱;  是金属元素;
是金属元素;  是非金属元素;
是非金属元素;  最外电子层有6个电子
最外电子层有6个电子
| A.①②③ | B.①③⑤ | C.②④⑤ | D.②③⑤ |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐1】X、Y、Z、W是原子序数依次增大的前20号元素,常温下只有一种元素的单质为气态。基态X原子s轨道上的电子数是p轨道上的2倍,Y的简单氢化物与其最高价含氧酸反应会产生白烟,Z与X形成的某种化合物常温下为液体,基态W原子有1个未成对电子。下列说法错误的是
| A.氢化物的沸点:Y>Z>X |
| B.电负性:Y>Z>X>W |
| C.原子半径:W>Z>X>Y |
| D.上述元素形成的某种化合物的溶液可用于检测Fe3+ |
您最近一年使用:0次
单选题
|
较难
(0.4)
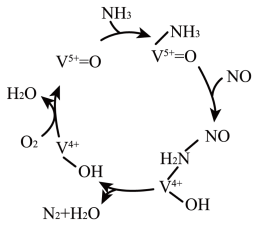
【推荐2】研究人员发现在某种含钒催化剂的作用下,NO可被 还原为
还原为 ,从而降低含氮气体造成的空气污染,反应机理如图所示,下列说法错误的是
,从而降低含氮气体造成的空气污染,反应机理如图所示,下列说法错误的是
 还原为
还原为 ,从而降低含氮气体造成的空气污染,反应机理如图所示,下列说法错误的是
,从而降低含氮气体造成的空气污染,反应机理如图所示,下列说法错误的是
A. 价电子排布式为 价电子排布式为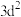 ,未成对电子数是2 ,未成对电子数是2 |
B. 和NO分子是极性分子, 和NO分子是极性分子, 为该反应的中间体 为该反应的中间体 |
| C.该转化过程中,氧化剂只有NO |
D.每生成标准状况下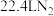 ,转移电子总数为 ,转移电子总数为 |
您最近一年使用:0次

 2CuO可推出同族的硫也有Cu+S
2CuO可推出同族的硫也有Cu+S 12KCN+Fe3C+2(CN)2↑+N2↑+C,下列关于该反应说法错误的是
12KCN+Fe3C+2(CN)2↑+N2↑+C,下列关于该反应说法错误的是

