科学家哈伯因为氨气的合成曾获1918年诺贝尔奖。
(1)写出实验室制取氨气的化学方程式_________ 。检验氨气已装满的方法是________ 。
(2)氨气可用如图装置进行喷泉实验,把氨气换成______ (填序号)也可形成喷泉实验。
A.二氧化碳 B.氧气 C.氯化氢气体 D.氢气
(3)完成氨催化氧化生成为NO的反应方程式,4NH3+____ O2===4NO+6_____ ,产物NO能在通常状况下被空气氧化为NO2,请完成下列反应生成硝酸的化学方程式:4NO+__ O2+2H2O===4HNO3,___ NO2+____ O2 +__ H2O===4HNO3
(4)12.8 g Cu与足量的浓硝酸反应生成的气体与一定量的O2混合,然后通入水中恰好完全反应无气体剩余,则该氧气的物质的量为_______ mol。
(1)写出实验室制取氨气的化学方程式
(2)氨气可用如图装置进行喷泉实验,把氨气换成
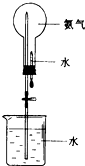
A.二氧化碳 B.氧气 C.氯化氢气体 D.氢气
(3)完成氨催化氧化生成为NO的反应方程式,4NH3+
(4)12.8 g Cu与足量的浓硝酸反应生成的气体与一定量的O2混合,然后通入水中恰好完全反应无气体剩余,则该氧气的物质的量为
17-18高一上·云南曲靖·期末 查看更多[3]
云南省沾益县第四中学2017-2018学年高一上学期期末考试化学试题(已下线)2018年12月5日——《每日一题》高一人教必修1-喷泉实验分析(已下线)2019年12月4日《每日一题》 人教版(必修1)——喷泉实验分析
更新时间:2018-09-03 14:54:09
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】研究氮及其化合物的性质,对生产、生活和有效改善人类的生存环境有重要的价值。如图是氮元素的“价—类”二维图,已知W中加入浓NaOH溶液,加热可生成X。据此回答下列问题:
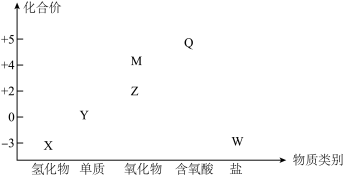
(1)写出物质的化学式:M_______ ,Q_______ 。
(2)实验室用装置甲制取X的化学方程式为_______ 。用装置乙收集X时,进气口为_______ (填“a”或“b”)。若观察到装置乙中的烧瓶内产生了红色喷泉,你认为引发喷泉的操作应是(止水夹a、b已关闭):_______ 。
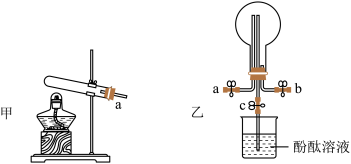
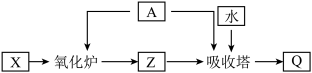
(3)某工厂用X制备Q的流程如图所示。物质A是_______ ,氧化炉中所发生反应的化学方程式为_______ 。
(4)汽车的“催化转换器”能使尾气中的Z与CO发生反应,生成Y和另一种无污染的气体,写出该反应的化学方程式_______ 。

(1)写出物质的化学式:M
(2)实验室用装置甲制取X的化学方程式为

(3)某工厂用X制备Q的流程如图所示。物质A是

(4)汽车的“催化转换器”能使尾气中的Z与CO发生反应,生成Y和另一种无污染的气体,写出该反应的化学方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】氮元素及其化合物应用广泛。
(1)如图是氮及其化合物的转化关系,X的化学式为____ 。图中①②③的转化步骤,不涉及氧化还原反应是____ (填序号)。

(2)①如图装置可用来实验室制取氨气,写出大试管中发生反应的化学方程式____ 。
②请在图装置方框内画出用试管收集NH3的装置图(需必要的标注)____ 。
(3)汽车排气管上装有催化转化器可减少尾气对环境的污染,使尾气中的有害气体CO与NO反应转化为无害气体,该反应的化学方程式为____ 。
(1)如图是氮及其化合物的转化关系,X的化学式为

(2)①如图装置可用来实验室制取氨气,写出大试管中发生反应的化学方程式
②请在图装置方框内画出用试管收集NH3的装置图(需必要的标注)

(3)汽车排气管上装有催化转化器可减少尾气对环境的污染,使尾气中的有害气体CO与NO反应转化为无害气体,该反应的化学方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】下列是中学化学常见气体:①二氧化硫②氨气③氯化氢④氯气,回答下列问题:
(1)上述气体属于非电解质有_______ (填序号)。
(2)上述气体的实验室制法中,属于固液加热型发生装置的有_______ (填序号),必须用防倒吸装置吸收尾气的有_______ (填序号)。
(3)上述气体中只能使紫色石蕊试液变红的有_______ (填序号)。
(4)将上述气体中能使品红溶液褪色的气体等体积混合后再通入品红溶液,观察到的现象是_______ ,其原因是_______ (用离子方程式表示)。
(5)大气固氮的反应条件为_______ 。该反应产物在一定条件下能与上述气体中的含氮化合物反应生成对环境友好的物质,写出该反应的化学方程式_______ 。
(1)上述气体属于非电解质有
(2)上述气体的实验室制法中,属于固液加热型发生装置的有
(3)上述气体中只能使紫色石蕊试液变红的有
(4)将上述气体中能使品红溶液褪色的气体等体积混合后再通入品红溶液,观察到的现象是
(5)大气固氮的反应条件为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】NaCl是一种基础化工原料,通过电解饱和食盐水可以制得NaOH、H2、Cl2。完成下列填空:
(1)写出电解饱和食盐水的化学方程式_______ 。开始时_______ 极(阴、阳)碱性增强。
(2)新冠疫情期间需要大量消毒液,工业上生产消毒液是将氯气与烧碱溶液反应,完成该反应方程式_______ 。
(3)氯气压缩成为液氯属于_______ 变化(选填“物理”“化学”)。常用浓氨水来检查输氯管道是否泄漏,泄漏处会观察到大量的白烟(NH4Cl),其中一步反应是:2NH3+3Cl2→N2+6HCl,该反应也表明氯和氮的非金属性_______ > _______ 。写出产生白烟的化学方程式:_______ 。该白烟的成分溶于水,溶液呈_______ 性。(酸、碱或中性),用离子方程式解释原因_______ 。
(4)pH=2的醋酸和盐酸两溶液中,水的电离_______。
(5)取25 mLpH=2的醋酸溶液,加入等体积pH=12的NaOH溶液,反应后溶液中c(Na+)、c(CH3COO-)的大小关系为c(Na+)_______ c(CH3COO-)。
(1)写出电解饱和食盐水的化学方程式
(2)新冠疫情期间需要大量消毒液,工业上生产消毒液是将氯气与烧碱溶液反应,完成该反应方程式
(3)氯气压缩成为液氯属于
(4)pH=2的醋酸和盐酸两溶液中,水的电离_______。
| A.都被促进 | B.都被抑制 |
| C.甲中被促进,乙中被抑制 | D.甲中被抑制,乙中被促进 |
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】氮氧化物、二氧化硫能引发酸雨、雾霾等。回答下列问题:
(1) 产生硝酸型酸雨的化学方程式为
产生硝酸型酸雨的化学方程式为_______ 。
(2)汽车尾气催化转化器可将尾气中的CO、NO均转化为无害气体,该反应的还原产物为_______ 。
(3)目前工业上烟气脱硫脱硝的工艺流程如下:

已知:烟气中含尘、 、NOx(
、NOx(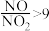 )。
)。
①“催化氧化”的目的是_______ 。
②图中产品中含硫成分为_______ (填化学式)。
(4)氨既是一种重要的化工产品,又是一种重要的化工原料。下图为合成氨以及氨氧化制硝酸的流程示意图。

分离器的作用是_______ ,写出氧化炉中的化学反应方程式:_______ 。
(1)
 产生硝酸型酸雨的化学方程式为
产生硝酸型酸雨的化学方程式为(2)汽车尾气催化转化器可将尾气中的CO、NO均转化为无害气体,该反应的还原产物为
(3)目前工业上烟气脱硫脱硝的工艺流程如下:

已知:烟气中含尘、
 、NOx(
、NOx(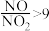 )。
)。①“催化氧化”的目的是
②图中产品中含硫成分为
(4)氨既是一种重要的化工产品,又是一种重要的化工原料。下图为合成氨以及氨氧化制硝酸的流程示意图。

分离器的作用是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】已知甲是短周期某主族元素的最简单氢化物,该物质有如下转化关系(反应条件部分省略)。
甲 乙
乙 丙
丙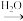 丁
丁
Ⅰ.若丙在常温常压为红棕色气体。
(1)写出实验室制取甲的化学方程式:__________ 。
(2)写出甲→乙的化学方程式:__________ 。
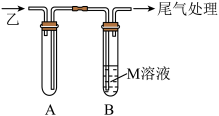
Ⅱ.若乙是具有刺激性气味的气体,丁为二元酸。某小组欲通过以下装置探究乙的部分性质。__________ 。
(4)试管A的作用为__________ 。
(5)若M是 溶液,试管B中观察到的现象为
溶液,试管B中观察到的现象为__________ ;为证明乙的氧化产物在溶液中的存在形式,某同学向试管B反应后的溶液中加入硝酸酸化的 溶液,判断是否出现白色沉淀。该做法
溶液,判断是否出现白色沉淀。该做法__________ (填“合理”或“不合理”),理由是__________ 。
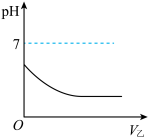
(6)将乙逐渐通入M溶液,测得溶液pH随通入乙气体体积的变化如图所示,则M溶液可能是__________ (填标号)。
甲
 乙
乙 丙
丙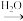 丁
丁Ⅰ.若丙在常温常压为红棕色气体。
(1)写出实验室制取甲的化学方程式:
(2)写出甲→乙的化学方程式:
Ⅱ.若乙是具有刺激性气味的气体,丁为二元酸。某小组欲通过以下装置探究乙的部分性质。
(4)试管A的作用为
(5)若M是
 溶液,试管B中观察到的现象为
溶液,试管B中观察到的现象为 溶液,判断是否出现白色沉淀。该做法
溶液,判断是否出现白色沉淀。该做法(6)将乙逐渐通入M溶液,测得溶液pH随通入乙气体体积的变化如图所示,则M溶液可能是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】实验室常用加热铵盐和碱的混合物的方法制取氨气。
(1)写出图中大试管中发生反应的化学方程式______________________________ 。

(2)收集氨气时,判断氨气是否收集满可采用的方法是_________________________ 。
(3)也可利用加热浓氨水的方法制取少量的氨气,此法利用了氨水的________ 性质。将收集满氨气的烧瓶组装成如图所示的装置。

当挤压胶头滴管,使少量的水进入烧瓶,打开弹簧夹可以观察到的现象是:_______________ 。
(1)写出图中大试管中发生反应的化学方程式

(2)收集氨气时,判断氨气是否收集满可采用的方法是
(3)也可利用加热浓氨水的方法制取少量的氨气,此法利用了氨水的

当挤压胶头滴管,使少量的水进入烧瓶,打开弹簧夹可以观察到的现象是:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】(1)硫酸在下列用途或反应中各表现的性质是(用字母填在横线上)
A.难挥发性 B.酸性 C.吸水性 D.脱水性 E.强氧化性 F.催化作用
①敞口放置浓硫酸时,质量增加_______ ,
②浓硫酸使润湿蓝色石蕊试纸先变红后又变黑___________ ,
③浓硫酸与铜反应_____________ ;
(2)氮氧化物也是造成酸雨的成分之一,治理汽车尾气中NO和CO的一种方法是:在汽车的排气管上装一个催化转换装置,使NO和CO反应,生成无毒气体,反应的化学方程式是_________________________________________ ;
(3)喷泉是一种常见的自然现象,其产生的原因是存在压强差;提供如图的装置,请说明引发喷泉的方法____________________________________ ;

(4)为了测定某铜银合金的成分,将17.2 g合金溶于40 mL 12.25 mol/L的浓硝酸中,待合金完全溶解后,收集到3.36 L(标准状况下)气体(气体为NO和NO2混合气体),并测得溶液中c(H+)=1mol/L,假设反应后溶液的体积仍为40 mL,则合金中铜的质量分数为_______________ ( 保留两位有效数字),收集到的混合气体中NO与NO2的体积之比为___________ 。
A.难挥发性 B.酸性 C.吸水性 D.脱水性 E.强氧化性 F.催化作用
①敞口放置浓硫酸时,质量增加
②浓硫酸使润湿蓝色石蕊试纸先变红后又变黑
③浓硫酸与铜反应
(2)氮氧化物也是造成酸雨的成分之一,治理汽车尾气中NO和CO的一种方法是:在汽车的排气管上装一个催化转换装置,使NO和CO反应,生成无毒气体,反应的化学方程式是
(3)喷泉是一种常见的自然现象,其产生的原因是存在压强差;提供如图的装置,请说明引发喷泉的方法

(4)为了测定某铜银合金的成分,将17.2 g合金溶于40 mL 12.25 mol/L的浓硝酸中,待合金完全溶解后,收集到3.36 L(标准状况下)气体(气体为NO和NO2混合气体),并测得溶液中c(H+)=1mol/L,假设反应后溶液的体积仍为40 mL,则合金中铜的质量分数为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】某同学采用如图装置进行实验,证明了铜与稀硝酸反应生成了NO。实验时,先向注射器内加入一定量的稀硝酸,排净注射器内的空气,迅速将带有铜丝的橡皮帽盖上,一段时间后,注射器内有无色气体产生。

(1)铜与稀硝酸反应的化学方程式为_________________ 。
(2)NO是大气污染物之一。目前有一种治理方法是在400℃左右、有催化剂存在的情况下,用氨气把NO还原为氮气和水。该反应的化学方程式为4NH3+6NO 5N2+6H2O,每有5 mol N2生成,氧化产物与还原产物的物质的量之比为
5N2+6H2O,每有5 mol N2生成,氧化产物与还原产物的物质的量之比为__________ 。
(3)若将上述稀硝酸换成浓硝酸,其生成的气体通入水中,该气体与水反应的化学方程式为______________________________________________ 。
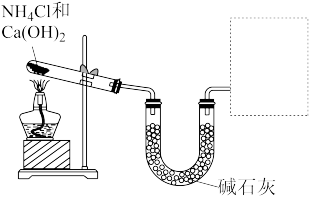
(4)①写出实验室由NH4Cl和Ca(OH)2加热制取氨气的化学方程式__________ 。
②进行喷泉实验,若在水中加入酚酞,得到红色喷泉。该实验体现了氨气的两个重要性质分别是________________________ 、___________________________ 。

(1)铜与稀硝酸反应的化学方程式为
(2)NO是大气污染物之一。目前有一种治理方法是在400℃左右、有催化剂存在的情况下,用氨气把NO还原为氮气和水。该反应的化学方程式为4NH3+6NO
 5N2+6H2O,每有5 mol N2生成,氧化产物与还原产物的物质的量之比为
5N2+6H2O,每有5 mol N2生成,氧化产物与还原产物的物质的量之比为(3)若将上述稀硝酸换成浓硝酸,其生成的气体通入水中,该气体与水反应的化学方程式为
(4)①写出实验室由NH4Cl和Ca(OH)2加热制取氨气的化学方程式
②进行喷泉实验,若在水中加入酚酞,得到红色喷泉。该实验体现了氨气的两个重要性质分别是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】SO2是主要大气污染物之一,其产生和治理是环境科学的主要研究方向。完成下列问题:
(1)SO2和O3是等电子体,有相似的结构质。以下关于O3的描述正确的是___________。(复选,填序号)
(2)SO2与CO2都属于酸性氧化物,以下关于两者比较正确的是___________。(复选,填序号)
(3)SO2能与稀硝酸反应生成NO,写出反应的化学方程式:___________ 。能否说明硝酸的酸性比硫酸强?说明理由___________ 。
(1)SO2和O3是等电子体,有相似的结构质。以下关于O3的描述正确的是___________。(复选,填序号)
| A.空间构型为直线形 | B.属于非电解质 |
| C.具有较强的氧化性 | D.属于极性分子 |
| A.都能使品红褪色 | B.都能使酸性KMnO4溶液褪色 |
| C.都能与Na2CO3反应 | D.都能与NaOH反应 |
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】按要求表达下列变化过程中的化学用语,其中⑴~⑶写化学方程式,⑷~⑸写离子方程式。
(1)金属镁在CO2中燃烧__________________________________________
(2)加热碳酸氢钠固体____________________________________________
(3)二氧化硫与氢氧化钠溶液反应__________________________________
(4)KCl溶液与AgNO3溶液反应_____________________________________
(5)铜与稀硝酸反应制取NO气体____________________________________
(1)金属镁在CO2中燃烧
(2)加热碳酸氢钠固体
(3)二氧化硫与氢氧化钠溶液反应
(4)KCl溶液与AgNO3溶液反应
(5)铜与稀硝酸反应制取NO气体
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】物质的量是高中化学常用的物理量,请完成第(1)-(4)小题的有关填空:
(1)0.6 mol 与0.4 mol
与0.4 mol  的质量之比为
的质量之比为_______ ,分子个数之比为_______ 。
(2)2 mol 与
与_______ mol  所含氧原子数相等。
所含氧原子数相等。
(3)已知铜在常温下能与稀 反应,化学方程式为
反应,化学方程式为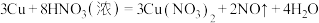 。
。
①请将上述反应改写成离子方程式:_______ 。
②在参加反应的硝酸中,起氧化作用的 与起酸性作用的
与起酸性作用的 的物质的量之比为
的物质的量之比为_______ 。
(4)某盐混合溶液中含有离子: 、
、 、
、 、
、 ,测得
,测得 、
、 和
和 的物质的量浓度依次为:
的物质的量浓度依次为: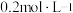 、
、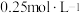 、
、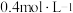 ,则
,则
_______ 。
(1)0.6 mol
 与0.4 mol
与0.4 mol  的质量之比为
的质量之比为(2)2 mol
 与
与 所含氧原子数相等。
所含氧原子数相等。(3)已知铜在常温下能与稀
 反应,化学方程式为
反应,化学方程式为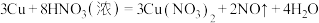 。
。①请将上述反应改写成离子方程式:
②在参加反应的硝酸中,起氧化作用的
 与起酸性作用的
与起酸性作用的 的物质的量之比为
的物质的量之比为(4)某盐混合溶液中含有离子:
 、
、 、
、 、
、 ,测得
,测得 、
、 和
和 的物质的量浓度依次为:
的物质的量浓度依次为: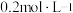 、
、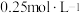 、
、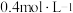 ,则
,则
您最近一年使用:0次



