味精的鲜味物质是谷氨酸钠,杂质主要是氯化钠。某学生欲测定味精中食盐的含量。
(1)下面是该学生所做的有关实验,请补写缺失的实验步骤②和④。
①称取某品牌的袋装味精样品5.0g,并溶于蒸馏水;
②___________________________________________________________________
③过滤;
④____________________________________________________________________
⑤将沉淀烘干、称量,测得固体质量为2.9g。
(2)根据上述实验步骤回答下列有关问题:
①过滤操作所需要的玻璃仪器有____________________________________________
②验沉淀是否洗净的方法是_____________________________________________
③若味精包装上标注“谷氨酸钠含量≥80%,NaCl含量≤20%”,问此样品是否符合产品标注的质量分数?________________ (填“符合”或“不符合”)。
(3)若有甲、乙两学生分别做了这个实验,甲学生认真地做了一次实验,就取得了实验数据,而乙学生认真地做了两次实验,取两次数据的平均值作为实验的测定数据,你认为_____ 学生的方法更合理(填“甲”或“乙”)。
(1)下面是该学生所做的有关实验,请补写缺失的实验步骤②和④。
①称取某品牌的袋装味精样品5.0g,并溶于蒸馏水;
②
③过滤;
④
⑤将沉淀烘干、称量,测得固体质量为2.9g。
(2)根据上述实验步骤回答下列有关问题:
①过滤操作所需要的玻璃仪器有
②验沉淀是否洗净的方法是
③若味精包装上标注“谷氨酸钠含量≥80%,NaCl含量≤20%”,问此样品是否符合产品标注的质量分数?
(3)若有甲、乙两学生分别做了这个实验,甲学生认真地做了一次实验,就取得了实验数据,而乙学生认真地做了两次实验,取两次数据的平均值作为实验的测定数据,你认为
更新时间:2018-09-16 18:59:38
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐1】葡萄糖酸钙是一种可促进骨骼生长的营养物质。葡萄糖酸钙可通过以下反应制得:
C6H12O6(葡萄糖)+Br2+H2O→C6H12O7(葡萄糖酸)+2HBr
2C6H12O7+CaCO3→Ca(C6H11O7)2(葡萄糖酸钙)+H2O+CO2↑
相关物质的溶解性见表:
实验流程如图:
C6H12O6溶液
 悬浊液
悬浊液 Ca(C6H11O7)2
Ca(C6H11O7)2
请回答下列问题:
(1)第①步中溴水氧化葡萄糖时,图中装置最适合的是_______ 。
A. B.
B.  C.
C. 
制备葡萄糖酸钙的过程中,葡萄糖的氧化也可用其它试剂,下列物质中最适合的是_______ 。
A.新制Cu(OH)2悬浊液 B.酸性KMnO4溶液
C.O2/葡萄糖氧化酶 D.[Ag(NH3)2]OH溶液
(2)第②步充分反应后CaCO3固体需有剩余,其目的是_______ ;本实验中不宜用CaCl2替代CaCO3,理由是_______ 。
(3)第③步需趁热过滤,其原因是_______ 。
(4)第④步加入乙醇的作用是_______ 。
(5)第⑥步中,下列洗涤剂最合适的是_______。
C6H12O6(葡萄糖)+Br2+H2O→C6H12O7(葡萄糖酸)+2HBr
2C6H12O7+CaCO3→Ca(C6H11O7)2(葡萄糖酸钙)+H2O+CO2↑
相关物质的溶解性见表:
| 物质名称 | 葡萄糖酸钙 | 葡萄糖酸 | 溴化钙 | 氯化钙 |
| 水中的溶解性 | 可溶于冷水 易溶于热水 | 可溶 | 易溶 | 易溶 |
| 乙醇中的溶解性 | 微溶 | 微溶 | 可溶 | 可溶 |
C6H12O6溶液

 悬浊液
悬浊液 Ca(C6H11O7)2
Ca(C6H11O7)2请回答下列问题:
(1)第①步中溴水氧化葡萄糖时,图中装置最适合的是
A.
 B.
B.  C.
C. 
制备葡萄糖酸钙的过程中,葡萄糖的氧化也可用其它试剂,下列物质中最适合的是
A.新制Cu(OH)2悬浊液 B.酸性KMnO4溶液
C.O2/葡萄糖氧化酶 D.[Ag(NH3)2]OH溶液
(2)第②步充分反应后CaCO3固体需有剩余,其目的是
(3)第③步需趁热过滤,其原因是
(4)第④步加入乙醇的作用是
(5)第⑥步中,下列洗涤剂最合适的是_______。
| A.冷水 | B.热水 | C.乙醇 | D.乙醇-水混合溶液 |
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】苯甲酸乙酯(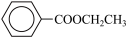 )是重要的精细化工试剂,常用于配制水果型食用香精。某化学兴趣小组通过酯化反应,以苯甲酸和乙醇为原料合成苯甲酸乙酯。
)是重要的精细化工试剂,常用于配制水果型食用香精。某化学兴趣小组通过酯化反应,以苯甲酸和乙醇为原料合成苯甲酸乙酯。
Ⅰ.试剂相关性质如表:
Ⅱ.实验装置如图(部分夹持装置以及加热装置已省去)
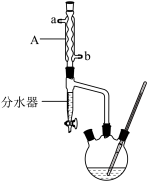
Ⅲ.实验步骤如下:
①加料:于100 mL三颈烧瓶中加入:9.8 g苯甲酸、15 mL(约0.25 mol)95%的乙醇和2 mL浓硫酸,摇匀,加沸石。
②加热:小心缓慢加热回流约2 h后,改为蒸馏装置。
③除杂:将瓶中残液倒入盛有20 mL冷水的烧杯中,在搅拌下分批加进 粉末,用pH试纸检验呈中性。
粉末,用pH试纸检验呈中性。
④分离萃取、干燥:分液,水层用10 mL乙醚萃取。合并有机层,加入物质X干燥。
⑤精馏:回收乙醚,加热蒸馏,收集211~213℃馏分,称量产物的质量为9.5 g。
回答下列问题:
(1)步骤①的装置如图所示(加热和夹持装置已略去),仪器A的名称为___________ ;冷却水从___________ (填“a”或“b”)口进入。
(2)写出该法制备苯甲酸乙酯的化学方程式___________ 。
(3)物质X应选择___________ (填选项字母)。
A.碱石灰 B.无水 C.
C.
(4)该反应装置中使用到了分水器,通过分水器不断分离除去反应生成的水,这样做的目的是___________ 。
(5)步骤④中分液操作叙述正确的是___________ (填选项字母)。
A.向盛有水层的分液漏斗中加入乙醚,盖好玻璃塞,将分液漏斗倒转,用力振荡
B.振荡几次后需打开分液漏斗的下口活塞放气
C.经几次振荡并放气后,手持分液漏斗静置待液体分层
D.液体分层后,将分液漏斗上的玻璃塞打开,或使塞上的凹槽对准漏斗上的小孔
E.分液操作时,分液漏斗中的下层液体由下口放出,然后再将上层液体由下口放出
(6)通过计算,本实验的产率是___________ (保留三位有效数字)。
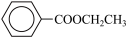 )是重要的精细化工试剂,常用于配制水果型食用香精。某化学兴趣小组通过酯化反应,以苯甲酸和乙醇为原料合成苯甲酸乙酯。
)是重要的精细化工试剂,常用于配制水果型食用香精。某化学兴趣小组通过酯化反应,以苯甲酸和乙醇为原料合成苯甲酸乙酯。Ⅰ.试剂相关性质如表:
| 苯甲酸 | 乙醇 | 苯甲酸乙酯 | |
| 常温性状 | 无色晶体 | 无色透明液体 | 无色透明液体 |
| 沸点/℃ | 249.0 | 78.0 | 212.6 |
| 相对分子量 | 122 | 46 | 150 |
| 溶解性 | 微溶于水,易溶于乙醇、乙醚等有机溶剂 | 与水任意比互溶 | 难溶于冷水,微溶于热水,易溶于乙醇和乙醚 |

Ⅲ.实验步骤如下:
①加料:于100 mL三颈烧瓶中加入:9.8 g苯甲酸、15 mL(约0.25 mol)95%的乙醇和2 mL浓硫酸,摇匀,加沸石。
②加热:小心缓慢加热回流约2 h后,改为蒸馏装置。
③除杂:将瓶中残液倒入盛有20 mL冷水的烧杯中,在搅拌下分批加进
 粉末,用pH试纸检验呈中性。
粉末,用pH试纸检验呈中性。④分离萃取、干燥:分液,水层用10 mL乙醚萃取。合并有机层,加入物质X干燥。
⑤精馏:回收乙醚,加热蒸馏,收集211~213℃馏分,称量产物的质量为9.5 g。
回答下列问题:
(1)步骤①的装置如图所示(加热和夹持装置已略去),仪器A的名称为
(2)写出该法制备苯甲酸乙酯的化学方程式
(3)物质X应选择
A.碱石灰 B.无水
 C.
C.
(4)该反应装置中使用到了分水器,通过分水器不断分离除去反应生成的水,这样做的目的是
(5)步骤④中分液操作叙述正确的是
A.向盛有水层的分液漏斗中加入乙醚,盖好玻璃塞,将分液漏斗倒转,用力振荡
B.振荡几次后需打开分液漏斗的下口活塞放气
C.经几次振荡并放气后,手持分液漏斗静置待液体分层
D.液体分层后,将分液漏斗上的玻璃塞打开,或使塞上的凹槽对准漏斗上的小孔
E.分液操作时,分液漏斗中的下层液体由下口放出,然后再将上层液体由下口放出
(6)通过计算,本实验的产率是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】氯化苦( )是一种无色或微黄色油状液体,可用于粮食害虫熏蒸,还可用于木材防腐、房屋和船舶消毒等。制备氯化苦的反应原理为
)是一种无色或微黄色油状液体,可用于粮食害虫熏蒸,还可用于木材防腐、房屋和船舶消毒等。制备氯化苦的反应原理为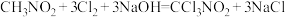
 。已知氯化苦、硝基甲烷(
。已知氯化苦、硝基甲烷( )的性质如下表所示:
)的性质如下表所示:
(一)氯化苦的制备

(1)仪器X的名称是______ 。
(2)装置A中发生反应的化学方程式为 ,将其改写成离子方程式:
,将其改写成离子方程式:______ 。
(3)装置B中饱和食盐水的作用是______ ,装置D的作用是______ 。
(二)氯化苦的提纯
(4)步骤1:将上述制得的氯化苦混合溶液在下图装置中进行分液,氯化苦应该从分液漏斗______ (填“上”或“下”)口倒出。

步骤2:将步骤1分离出的氯化苦混合溶液进行蒸馏,将温度控制在101.2~110℃范围内其目的是______ 。
 )是一种无色或微黄色油状液体,可用于粮食害虫熏蒸,还可用于木材防腐、房屋和船舶消毒等。制备氯化苦的反应原理为
)是一种无色或微黄色油状液体,可用于粮食害虫熏蒸,还可用于木材防腐、房屋和船舶消毒等。制备氯化苦的反应原理为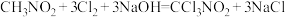
 。已知氯化苦、硝基甲烷(
。已知氯化苦、硝基甲烷( )的性质如下表所示:
)的性质如下表所示:| 名称 | 相对分子质量 | 密度/( ) ) | 熔点/℃ | 沸点/℃ | 溶解性 |
| 氯化苦 | 164.5 | 1.66 | -69.2 | 112 | 不溶于水,溶于乙醇 |
| 硝基甲烷 | 61 | 1.14 | -28.6 | 101.2 | 溶于水、乙醇 |

(1)仪器X的名称是
(2)装置A中发生反应的化学方程式为
 ,将其改写成离子方程式:
,将其改写成离子方程式:(3)装置B中饱和食盐水的作用是
(二)氯化苦的提纯
(4)步骤1:将上述制得的氯化苦混合溶液在下图装置中进行分液,氯化苦应该从分液漏斗

步骤2:将步骤1分离出的氯化苦混合溶液进行蒸馏,将温度控制在101.2~110℃范围内其目的是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】有一包粉末可能含有Na+、Fe3+、Al3+、Cl-、SO42-、CO32-中的若干种,现进行以下实验:
①取少量固体,加入稀硝酸搅拌,固体全部溶解,没有气体放出;
②向①溶液中加入一定量Ba(OH)2溶液,生成有色沉淀,过滤后,滤液呈中性,在滤液中滴入AgNO3溶液,有白色沉淀生成;
③取②中的有色沉淀加入足量的稀盐酸后,沉淀全部溶解;
④重新取少量固体加入适量蒸馏水搅拌后,固体全部溶解,得到澄清溶液;
⑤向④的溶液中加入氨水使溶液呈碱性,有沉淀生成,过滤.往得到的沉淀中加入过量的NaOH溶液,沉淀减少。
(1)根据上述实验,这包粉末中一定不含有的离子是________ ,肯定含有的离子是________ ,不能确定是否含有的离子是_________ 。
(2)写出⑤中生成有色沉淀反应的离子方程式:_______________________________ 。
(3)写出⑤中沉淀减少反应的离子方程式:___________________________________ 。
①取少量固体,加入稀硝酸搅拌,固体全部溶解,没有气体放出;
②向①溶液中加入一定量Ba(OH)2溶液,生成有色沉淀,过滤后,滤液呈中性,在滤液中滴入AgNO3溶液,有白色沉淀生成;
③取②中的有色沉淀加入足量的稀盐酸后,沉淀全部溶解;
④重新取少量固体加入适量蒸馏水搅拌后,固体全部溶解,得到澄清溶液;
⑤向④的溶液中加入氨水使溶液呈碱性,有沉淀生成,过滤.往得到的沉淀中加入过量的NaOH溶液,沉淀减少。
(1)根据上述实验,这包粉末中一定不含有的离子是
(2)写出⑤中生成有色沉淀反应的离子方程式:
(3)写出⑤中沉淀减少反应的离子方程式:
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐2】实验室用浓盐酸和 制
制 ,并以干燥的
,并以干燥的 为原料制备无水
为原料制备无水 。已知
。已知 易升华,易吸收水分而潮解。装置如下图所示。
易升华,易吸收水分而潮解。装置如下图所示。_______ 。
(2)装置B、C中应盛放的试剂名称分别为_______ 、_______ 。
(3)从A装置导出的气体若不经过B、C装置而直接进入D管,将对实验产生的不良后果是_______ 。
(4)实验时,先点燃A处的酒精灯,让 充满装置,再点燃D处酒精灯,写出D中反应的化学方程式:
充满装置,再点燃D处酒精灯,写出D中反应的化学方程式:_______ 。
(5)F装置所起的作用是_______ 和防止空气中的水蒸气进入E中。
(6)生产消毒液是将氯气通入NaOH溶液中,发生反应的化学方程式为_______ 。
(7)取少量消毒液滴加酸性 溶液,现象是出现白色沉淀,说明消毒液中有
溶液,现象是出现白色沉淀,说明消毒液中有_______ (填离子符号),消毒液稀释后喷洒在空气中,可以生成有漂白性的物质,请写出此过程的化学方程式:_______ 。
 制
制 ,并以干燥的
,并以干燥的 为原料制备无水
为原料制备无水 。已知
。已知 易升华,易吸收水分而潮解。装置如下图所示。
易升华,易吸收水分而潮解。装置如下图所示。
(2)装置B、C中应盛放的试剂名称分别为
(3)从A装置导出的气体若不经过B、C装置而直接进入D管,将对实验产生的不良后果是
(4)实验时,先点燃A处的酒精灯,让
 充满装置,再点燃D处酒精灯,写出D中反应的化学方程式:
充满装置,再点燃D处酒精灯,写出D中反应的化学方程式:(5)F装置所起的作用是
(6)生产消毒液是将氯气通入NaOH溶液中,发生反应的化学方程式为
(7)取少量消毒液滴加酸性
 溶液,现象是出现白色沉淀,说明消毒液中有
溶液,现象是出现白色沉淀,说明消毒液中有
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐3】某钠盐溶液可能含有阴离子 NO 、CO
、CO 、SO
、SO 、SO
、SO 、Cl-、Br-、I-。为鉴定这些离子,分别取少量溶液进行以下实验:
、Cl-、Br-、I-。为鉴定这些离子,分别取少量溶液进行以下实验:
①测得溶液呈碱性;
②加HCl后,生成无色、无味气体。该气体能使饱和石灰水溶液变浑浊;
③加CCl4,滴加少量氯水,振荡后,CCl4层未变色;
④加BaCl2溶液产生白色沉淀,分离,在沉淀中加入足量盐酸,沉淀不能完全溶解;
⑤加HNO3酸化后,再加过量AgNO3溶液,溶液中析出白色沉淀。
分析上述5个实验,写出每一实验鉴定离子的结论(用“一定有”或“可能有”或“一定没有”来描述,说明理由。)。
(1)实验①_____________________________ ;
(2)实验②______________________________ ;
(3)实验③____________________________ ;
(4)实验④____________________________ ;
(5)实验⑤____________________________ 。
 、CO
、CO 、SO
、SO 、SO
、SO 、Cl-、Br-、I-。为鉴定这些离子,分别取少量溶液进行以下实验:
、Cl-、Br-、I-。为鉴定这些离子,分别取少量溶液进行以下实验:①测得溶液呈碱性;
②加HCl后,生成无色、无味气体。该气体能使饱和石灰水溶液变浑浊;
③加CCl4,滴加少量氯水,振荡后,CCl4层未变色;
④加BaCl2溶液产生白色沉淀,分离,在沉淀中加入足量盐酸,沉淀不能完全溶解;
⑤加HNO3酸化后,再加过量AgNO3溶液,溶液中析出白色沉淀。
分析上述5个实验,写出每一实验鉴定离子的结论(用“一定有”或“可能有”或“一定没有”来描述,说明理由。)。
(1)实验①
(2)实验②
(3)实验③
(4)实验④
(5)实验⑤
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐1】某校化学趣小组设计了图示实验装置来测定某铁碳合金的质量分数。
完成下列填空:
(1)m g铁碳合金中加入过量浓硫酸,未点燃酒精灯前,A、B均无明显现象,其原因是:①常温下碳与浓硫酸不反应;②______________________________________ 。
(2)加热时A中碳与浓硫酸反应的化学方程式为____________ ,B中的现象是__________ ;C的作用是______________________________ 。
(3)待A中不再逸出气体时,停止加热,拆下E并称重,E称重b g。则铁碳合金中铁的质量分数的表达式为______________________________ (化简后的表达式)。
(4)甲同学认为利用此装置测得铁的质量分数偏大,可能的原因是__________________ 。
(5)乙同学提出,本套装置在设计上存在多处缺陷而导致实验结果不准确,其中会导致铁质量质量分数测量值偏低是___________ (回答一条即可)。

完成下列填空:
(1)m g铁碳合金中加入过量浓硫酸,未点燃酒精灯前,A、B均无明显现象,其原因是:①常温下碳与浓硫酸不反应;②
(2)加热时A中碳与浓硫酸反应的化学方程式为
(3)待A中不再逸出气体时,停止加热,拆下E并称重,E称重b g。则铁碳合金中铁的质量分数的表达式为
(4)甲同学认为利用此装置测得铁的质量分数偏大,可能的原因是
(5)乙同学提出,本套装置在设计上存在多处缺陷而导致实验结果不准确,其中会导致铁质量质量分数测量值偏低是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】冰晶石又名六氟铝酸钠(Na3AlF6),白色固体,微溶于水,常用作电解铝工业的助熔剂。工业上用萤石(主要成分是CaF2)、浓硫酸、氢氧化铝和碳酸钠溶液通过湿法制备冰晶石,某化学实验小组模拟工业上制取Na3AlF6的装置图如图(该装置均由聚四氟乙烯仪器组装而成)。
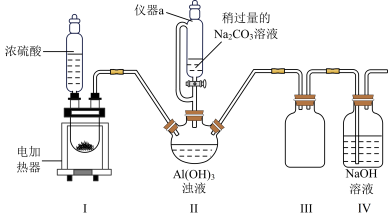
已知:CaF2+H2SO4 CaSO4+2HF↑
CaSO4+2HF↑
(1)装置Ⅲ的作用为__ 。
(2)在实验过程中,装置Ⅱ中有CO2气体逸出,同时观察到有白色固体析出,请写出该反应的离子方程式:__ 。
(3)在实验过程中,先向装置Ⅱ中通入HF气体,然后再滴加Na2CO3溶液,而不是先将Na2CO3和Al(OH)3混合后再通入HF气体,其原因是__ 。
(4)装置Ⅱ反应后的混合液经过过滤可得到Na3AlF6晶体,在过滤操作中确定沉淀已经洗涤干净的方法是__ 。
(5)萤石中含有少量的Fe2O3杂质,可用装置Ⅰ反应后的溶液来测定氟化钙的含量。具体操作如下:取8.0g萤石加入装置Ⅰ中,完全反应后,将混合液加水稀释,然后加入足量的KI固体,再以淀粉为指示剂,用0.1000mol·L-1 Na2S2O3标准溶液滴定,当出现__ 现象时,到达滴定终点,消耗Na2S2O3标准溶液40.00mL,则萤石中氟化钙的百分含量为__ 。(已知:I2+2 =
= +2I-)
+2I-)

已知:CaF2+H2SO4
 CaSO4+2HF↑
CaSO4+2HF↑(1)装置Ⅲ的作用为
(2)在实验过程中,装置Ⅱ中有CO2气体逸出,同时观察到有白色固体析出,请写出该反应的离子方程式:
(3)在实验过程中,先向装置Ⅱ中通入HF气体,然后再滴加Na2CO3溶液,而不是先将Na2CO3和Al(OH)3混合后再通入HF气体,其原因是
(4)装置Ⅱ反应后的混合液经过过滤可得到Na3AlF6晶体,在过滤操作中确定沉淀已经洗涤干净的方法是
(5)萤石中含有少量的Fe2O3杂质,可用装置Ⅰ反应后的溶液来测定氟化钙的含量。具体操作如下:取8.0g萤石加入装置Ⅰ中,完全反应后,将混合液加水稀释,然后加入足量的KI固体,再以淀粉为指示剂,用0.1000mol·L-1 Na2S2O3标准溶液滴定,当出现
 =
= +2I-)
+2I-)
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】某学习小组探究FeCl3溶液与Na2S溶液在某种条件下的反应。
实验Ⅰ
已知:FeS、Fe2S3均为黑色固体,难溶于水。
(1)用化学用语解释Na2S溶液呈碱性的原因___________ 。
(2)小组同学们试管b中黑色沉淀的提出猜想
猜想1::黑色沉淀是Fe2S3
猜想2::黑色沉淀是FeS
①针对猜想1,甲同学根据Na2S溶液呈碱性,推测试管b中黑色沉淀除Fe2S3外,还可能存在Fe(OH)3,补充实验II如下:
②甲同学继续查找数据:Ksp[Fe2S3]=1.0×10-88,Ksp[Fe(OH)3]=1.1×10-36,设计实验III:向Fe(OH)3中加入过量pH=12.5的0.1mol·L-1Na2S溶液,观察到的现象是沉淀颜色由___________ ,该现象对应的离子方程式为___________ 。
③针对猜想2,乙同学推测,若猜想2成立,应该还有S生成。写出该同学推测所依据的离子方程式___________ 。乙同学继续检验:进行实验并获取证据:取试管b中黑色沉淀,用水多次洗涤后,___________ ,确认黑色沉淀中无S单质,猜想2不成立。
(已知:Ksp(FeS)=1.59×10-19;H2S:Ka1=9.5×10-8,Ka2=1.3×10-14)
(3)丙同学利用电化学原理继续进行探究
丙同学依据实验IV得出结论:pH=1的0.1mol·L-1FeCl3溶液与pH=12.5的0.1mol·L-1Na2S溶液___________ (填“能”或“不能”)发生氧化还原反应。
(4)综合以上研究,从反应原理角度分析试管b中黑色沉淀是Fe2S3而不是FeS的原因:___________ 。
实验Ⅰ

已知:FeS、Fe2S3均为黑色固体,难溶于水。
(1)用化学用语解释Na2S溶液呈碱性的原因
(2)小组同学们试管b中黑色沉淀的提出猜想
猜想1::黑色沉淀是Fe2S3
猜想2::黑色沉淀是FeS
①针对猜想1,甲同学根据Na2S溶液呈碱性,推测试管b中黑色沉淀除Fe2S3外,还可能存在Fe(OH)3,补充实验II如下:
| 编号 | 操作或过程 | 现象和结论 |
| 实验Ⅱ | 向 | 有红褐色溶液生成。试管b中黑色的Fe2S3可能影响Fe(OH)3红褐色的观察。 |
③针对猜想2,乙同学推测,若猜想2成立,应该还有S生成。写出该同学推测所依据的离子方程式
(已知:Ksp(FeS)=1.59×10-19;H2S:Ka1=9.5×10-8,Ka2=1.3×10-14)
(3)丙同学利用电化学原理继续进行探究
| 编号 | 装置 | 操作及现象 |
| 实验IV |  | ①电流计指针有微弱偏转 ②2分钟后,取左侧烧杯溶液,滴加K3[Fe(CN)6]溶液,有少量蓝色沉淀;2小时后,右侧烧杯有黄色浑浊产生,再取左侧烧杯溶液,滴加K3[Fe(CN)6]溶液,有大量蓝色沉淀。 |
(4)综合以上研究,从反应原理角度分析试管b中黑色沉淀是Fe2S3而不是FeS的原因:
您最近一年使用:0次



