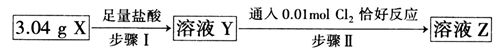
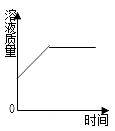
在托盘天平两端的烧杯中加入同浓度同体积的足量盐酸,当向两个烧杯中分别加入0.1mol两种金属充分反应后,而在某一端要再放一个0.2g砝码,天平才能平衡,则这两种金属是
| A.Mg和Al | B.Al和Fe | C.Fe和Cu | D.Na和Mg |
10-11高二下·辽宁大连·期末 查看更多[7]
(已下线)2010—2011学年辽宁大连23中高二下学期期末考试化学试卷(已下线)2011-2012学年浙江省杭州十四中高一上学期期末化学试卷河南省洛阳名校2017-2018学年高一上学期第二次联考化学试题【全国百强校】内蒙古自治区赤峰市第二中学2018-2019学年高一上学期第二次月考化学试题(已下线)【走进新高考】(人教版必修一)3.1.1金属的化学性质——金属与非金属、酸、水的反应 同步练习01(已下线)3.2.2 物质的量在化学方程式计算中的应用(精练)-2020-2021学年上学期高一化学同步精品课堂(人教版必修第一册)(已下线)衔接点13 钠的单质-2021年初升高化学无忧衔接
更新时间:2017-12-21 17:12:19
|
相似题推荐
单选题
|
较难
(0.4)
【推荐1】室温下,用0.100mol·L-1NaOH溶液分别滴定20.00mL0.100mol·L-1的盐酸和醋酸,滴定曲线如图。不考虑反应的热效应,下列说法正确的是
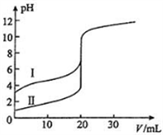
| A.曲线Ⅰ表示的是滴定盐酸的曲线 |
B.滴定醋酸过程中,溶液中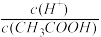 增大 增大 |
| C.V(NaOH)=10.00mL时,醋酸溶液中c(Na+)>c(CH3COO-)>c(H+)>c(OH-) |
| D.V(NaOH)=20.00mL时,两份溶液中c(Cl-)>c(CH3COO-) |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】25℃时,向20mL 0.lmol·L-1H2A溶液中滴加0.lmol·L-1NaOH溶液,有关粒子物质的量的变化如图所示。下列有关说法正确的是
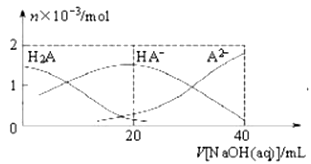

| A.H2A在水中的第一步电离的电离方程式为:H2A=HA-+H+ |
| B.c(HA-)/c(H2A)的比值随着V[NaOH(aq)]的增大而减小 |
| C.V[NaOH(aq)]=20mL 时,溶液中存在关系:c(HA-)+c(A2-)+c(H2A)=0.1 mol·L-1 |
| D.V[NaOH(aq)]=20mL 时,溶液中存在关系:c(Na+)>c(HA-)>c(H+)>c(A2-)>c(OH-) |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐3】下列有关说法正确 的是
| A.为了减小中和滴定的误差,锥形瓶必须洗净并烘干后才能使用 |
B.向 溶液中滴加过量的 溶液中滴加过量的 溶液得到浊液,过滤得到的滤液中不含 溶液得到浊液,过滤得到的滤液中不含 |
| C.离子交换膜在工业上应用广泛,如氯碱工业中使用阴离子交换膜 |
D.室温下, 的 的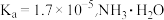 的 的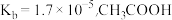 溶液中的 溶液中的 与 与 中的 中的 不一定相等 不一定相等 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐1】将1.60gCuSO4固体在高温下加热,得到0.72g红色固体(纯净物,不含S元素),同时有气体X生成,X可能是SO2、SO3、O2中的两种或三种。下列说法正确的是
| A.所得红色固体是铜 |
| B.将X通入氢氧化钡溶液,若溶液变浑浊,则X中含有SO3 |
| C.X的物质的量最少为0.01mol |
| D.将X缓慢通过足量NaOH溶液,若溶液增重0.72g,则X中含0.005molO2 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐2】某小组为探究K3[Fe(C2O4)3·3H2O(三草酸合铁酸钾晶体)的热分解产物,按如图所示装置进行实验。下列有关叙述错误的是
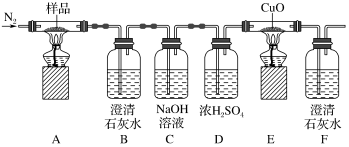

| A.通入氮气的目的有;隔绝空气、使反应产生的气体全部进入后续装置 |
| B.实验中观察到装置F中澄清石灰水变浑浊,装置E中固体变为红色,由此可判断热分解产物中一定含有CO2和CO |
| C.为防止倒吸,停止实验时应进行的操作是:先熄灭装置A、E的酒精灯,冷却后停止通入氮气 |
D.样品完全分解后,取少许装置A中残留物于试管中,加稀硫酸溶解,滴入1~2滴KSCN溶液,溶液变红色,可证明残留物中含有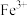 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐1】下列除去杂质的方法,正确的是
| A.除去碳酸氢钠固体中的少量碳酸钠:充入足量二氧化碳 |
| B.CuCl2溶液中含有FeCl3杂质:加入过量氧化铜粉末,过滤 |
| C.提取溴水中的溴:用乙醇萃取后分液 |
| D.CO2中含有HCl杂质:通入饱和Na2CO3溶液,洗气 |
您最近一年使用:0次
单选题
|
较难
(0.4)
解题方法
【推荐2】探究乙酸乙酯(沸点77.1℃)在不同温度、不同浓度NaOH溶液中的水解速率。取四支大小相同的试管,在试管外壁贴上体积刻度纸,按下表进行对照实验。在两种不同温度的水浴中加热相同时间后,记录酯层的体积来确定水解反应的速率。
下列说法中不正确的是( )
| 试管I(55℃) | 试管II(55℃) | 试管III(55℃) | 试管IV(75℃) | |
| 乙酸乙酯/mL | 1 | V1 | V2 | V3 |
| 1mol/L NaOH溶液/mL | V4 | 3 | 0 | V5 |
| 蒸馏水/mL | 0 | V6 | 5 | 2 |
| A.试管I、II、III叫探究乙酸乙酯在相同温度下在不同浓度NaOH溶液中的水解速率,则V2=1,V4=5 |
| B.探究乙酸乙酯在相同NaOH溶液中在不同温度下的水解速率的实验是试管II和IV,则V5=3 |
| C.试管外壁体积刻度纸读数的大小为:试管IV>试管I>试管II>试管III |
| D.试管IV比试管II中的酯层减少更快除温度高速率快外,还可能是水浴温度接近乙酸乙酯的沸点造成乙酸乙酯大量挥发 |
您最近一年使用:0次