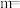(1)24.8 g Na2R含有Na+ 0.8 mol则R的摩尔质量为_________________ 。
(2)质量都为a g的镁和铝,物质的量之比为___________ ;将它们分别放入适量的盐酸溶液中恰好完全反应,则消耗的HCl的物质的量之比为___________ 。
(3)在标准状况下,CO和CO2混合气体的质量为36 g,体积为22.4 L,则其中CO2所占的体积为_________ ,CO所占的质量为_________ 。
(2)质量都为a g的镁和铝,物质的量之比为
(3)在标准状况下,CO和CO2混合气体的质量为36 g,体积为22.4 L,则其中CO2所占的体积为
更新时间:2018-10-27 07:40:29
|
相似题推荐
计算题
|
适中
(0.65)
解题方法
【推荐1】在标准状况下,18gCO与CO2的混合气体,体积为11.2L。则:
(1)混合气体的密度是________ ;
(2)混合气体的平均摩尔质量是_______ ;
(3)CO与CO2的体积之比是_________ ;
(4)CO与CO2的质量之比是__________ ;
(5)混合气体中所含碳原子的物质的量是________ 。
(1)混合气体的密度是
(2)混合气体的平均摩尔质量是
(3)CO与CO2的体积之比是
(4)CO与CO2的质量之比是
(5)混合气体中所含碳原子的物质的量是
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐2】(1)3.6gH2O的物质的量是____ mol,含有___ 个水分子,含有__ molH。
(2)标准状况下44.8LHCl气体的物质的量是____ mol,全部溶于水形成1L盐酸溶液,此盐酸的物质的量浓度是____ mol•L-1。
(3)3.01×1022个OH-的物质的量为___ mol,质量为___ g,含有质子的物质的量为___ mol,含有电子的物质的量为____ mol,这些OH-与____ molNH3的质量相同。
(4)用20gNaOH配成250mL溶液,它的物质的量浓度为___ mol•L-1。取出5mL该溶液,它的物质的量浓度为__ mol•L-1,再加水稀释至100mL,则稀释后溶液的物质的量浓度为___ mol•L-1。
(5)18.6gNa2R含0.6molNa+,则Na2R的摩尔质量为___ ,R的相对原子质量为___ 。
(2)标准状况下44.8LHCl气体的物质的量是
(3)3.01×1022个OH-的物质的量为
(4)用20gNaOH配成250mL溶液,它的物质的量浓度为
(5)18.6gNa2R含0.6molNa+,则Na2R的摩尔质量为
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐1】回答下列问题:
(1)纯净的过氧化钙(CaO2)是一种新型水产养殖增氧剂,常用于鲜活水产品的运输,可以起到杀菌、解酸(吸收二氧化碳)、防腐、供氧的作用。分别写出供氧、解酸(吸收二氧化碳)的化学方程式:_______ 、_______ 。
(2)现有某过氧化钙(CaO2)样品,带有结晶水,含有CaO杂质。
a. 称取5.42 g过氧化钙样品,灼烧时发生如下反应:2(CaO2·xH2O) 2CaO+O2↑+2xH2O,得到O2在标准状况下体积为672 mL,则该样品中CaO2的物质的量为
2CaO+O2↑+2xH2O,得到O2在标准状况下体积为672 mL,则该样品中CaO2的物质的量为_______ 。
b. 另取同一样品5.42 g,溶于适量的稀盐酸中,然后加入足量的Na2CO3溶液,将溶液中的Ca2+全部转化为CaCO3沉淀,得到干燥的CaCO3 7.0 g。
①样品中CaO的质量为_______ 。
②样品中CaO2·xH2O中的x为_______ 。
(1)纯净的过氧化钙(CaO2)是一种新型水产养殖增氧剂,常用于鲜活水产品的运输,可以起到杀菌、解酸(吸收二氧化碳)、防腐、供氧的作用。分别写出供氧、解酸(吸收二氧化碳)的化学方程式:
(2)现有某过氧化钙(CaO2)样品,带有结晶水,含有CaO杂质。
a. 称取5.42 g过氧化钙样品,灼烧时发生如下反应:2(CaO2·xH2O)
 2CaO+O2↑+2xH2O,得到O2在标准状况下体积为672 mL,则该样品中CaO2的物质的量为
2CaO+O2↑+2xH2O,得到O2在标准状况下体积为672 mL,则该样品中CaO2的物质的量为b. 另取同一样品5.42 g,溶于适量的稀盐酸中,然后加入足量的Na2CO3溶液,将溶液中的Ca2+全部转化为CaCO3沉淀,得到干燥的CaCO3 7.0 g。
①样品中CaO的质量为
②样品中CaO2·xH2O中的x为
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐2】工业上可以由N2和H2合成NH3,已知该反应为放热反应。
(1)写出该反应的化学方程式______________ 。已知:1molN2的共价键断裂吸收的能量为Q1kJ;1molH2的化学键断裂吸收的能量为Q2kJ;形成1molNH3中的化学键释放的能量为Q3kJ。则Q1+3Q2_____ 2Q3(填“>”、“<”或“=”)。
(2)写出加快合成氨反应速率的措施_______________ 。
(3)工业上也可通过电解的方法由N2制取NH3:2N2 +6H2O 4NH3 +3O2,若制得8.96L(标准状况下)NH3,转移电子
4NH3 +3O2,若制得8.96L(标准状况下)NH3,转移电子_____ mol。
(1)写出该反应的化学方程式
(2)写出加快合成氨反应速率的措施
(3)工业上也可通过电解的方法由N2制取NH3:2N2 +6H2O
 4NH3 +3O2,若制得8.96L(标准状况下)NH3,转移电子
4NH3 +3O2,若制得8.96L(标准状况下)NH3,转移电子
您最近一年使用:0次
【推荐3】为确定某铝热剂(含氧化铁和铝)的组成,分别进行下列实验。
(1) 若取a g样品,向其中加入足量的NaOH溶液,测得生成的气体(标准状况,下同)体积为b L。样品中铝的质量是_____________ g。
(2) 若取a g样品将其点燃,恰好完全反应,该反应的化学方程式是:________ ,氧化铁与铝的质量比是________ 。
(3) 待(2)中反应产物冷却后,加入足量盐酸,测得生成的气体体积为c L,该气体与(1)中所得气体的体积比c∶b=______________ 。
(1) 若取a g样品,向其中加入足量的NaOH溶液,测得生成的气体(标准状况,下同)体积为b L。样品中铝的质量是
(2) 若取a g样品将其点燃,恰好完全反应,该反应的化学方程式是:
(3) 待(2)中反应产物冷却后,加入足量盐酸,测得生成的气体体积为c L,该气体与(1)中所得气体的体积比c∶b=
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐1】合成氨原料可以由天然气制取。
其主要反应为:CH4(g)+H2O(g)→CO(g)+3H2(g)
(1)1m3(标准状况)CH4按上式完全反应,产生H2____________mol。
(计算结果保留整数)
(2)CH4和O2的反应为:2CH4(g)+O2(g)→2CO(g)+4H2(g)
设CH4同时和H2O(g)及O2(g)反应。1m3(标准状况)CH4按上述两式完全反应,产物气体的体积V(标准状况)为____________ m3。(填体积取值范围)
(3)CH4和H2O(g)及富氧空气(O2含量较高,不同富氧空气氧气含量不同)混合反应,产物气体组成如下表:
计算该富氧空气中O2和N2的体积比V(O2)/V(N2)=
其主要反应为:CH4(g)+H2O(g)→CO(g)+3H2(g)
(1)1m3(标准状况)CH4按上式完全反应,产生H2____________mol。
(计算结果保留整数)
(2)CH4和O2的反应为:2CH4(g)+O2(g)→2CO(g)+4H2(g)
设CH4同时和H2O(g)及O2(g)反应。1m3(标准状况)CH4按上述两式完全反应,产物气体的体积V(标准状况)为____________ m3。(填体积取值范围)
(3)CH4和H2O(g)及富氧空气(O2含量较高,不同富氧空气氧气含量不同)混合反应,产物气体组成如下表:
| 气体 | CO | H2 | N2 | O2 |
| 体积(L) | 25 | 60 | 15 | 2.5 |
计算该富氧空气中O2和N2的体积比V(O2)/V(N2)=
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】2021年11月初,世界气候峰会在英国举行,为减少环境污染,减少化石能源的使用,开发新型、清洁、可再生能源迫在眉睫。
(1)甲醇、乙醇来源丰富、燃烧热值高,可作为能源使用。其中一种可减少空气中CO2的甲醇合成方法为:CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g)。
①若将一定量的CO2和H2投入1.0L恒容密闭容器中合成甲醇,实验测得不同温度及压强下,平衡时甲醇的物质的量变化如图所示。则该反应的正反应为_______ (填“放热”或“吸热”)反应,在p2及512K时,图中N点处平衡向_______ (填“正向”或“逆向”)移动;

②若将物质的量之比为1:3的CO2和H2充入体积为1.0L的恒容密闭容器中反应,不同压强下CO2转化率随温度的变化关系如下图所示。
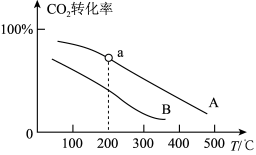
a.A、B两条曲线的压强分别为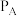 、
、 ,则
,则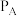
_______  (填“>”“<”或“=”);
(填“>”“<”或“=”);
b.若A曲线条件下,起始充入CO2和H2的物质的量分别为lmol、3mol,且a点时的K=300(L2/mol2),则a点对应CO2转化率为_______ 。
(2)在工业生产中也用反应CO(g)+H2O(g)=CO2(g)+H2(g) ΔH=-41.2kJ·mol-1制取H2,从而获得氢能源,该反应需要加入催化剂,若用[M]表示催化剂,则反应历程可表示为:
第一步:[M]+H2O(g)=[M]O+H2(g)
第二步:[M]O+CO(g)=[M]+CO2(g)
①第二步比第一步反应慢,则第二步反应的活化能比第一步_______ (填“大”或“小”)。反应过程中,中间产物[M]O的能量比产物的能量_______ (填“高”或“低”);
②研究表明,此反应的速率方程为 ,式中)
,式中)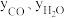 、
、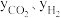 分别表示相应的物质的量分数,Kp为平衡常数,k为反应的速率常数,温度升高时k值增大。在气体组成和催化剂一定的情况下,反应速率随温度变化的曲线如图所示。温度升高时,该反应的Kp
分别表示相应的物质的量分数,Kp为平衡常数,k为反应的速率常数,温度升高时k值增大。在气体组成和催化剂一定的情况下,反应速率随温度变化的曲线如图所示。温度升高时,该反应的Kp_______ (填“增大”或“减小”)。根据速率方程分析,T>Tm时v逐渐减小的原因是_______ 。

(3)以甲醇为主要原料,电化学合成碳酸二甲酯的工作原理如图所示。阳极的电极反应式为____ ,若装置中消耗标准状态下O244.8L,理论上能制得碳酸二甲酯的质量____ g。

(1)甲醇、乙醇来源丰富、燃烧热值高,可作为能源使用。其中一种可减少空气中CO2的甲醇合成方法为:CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g)。
①若将一定量的CO2和H2投入1.0L恒容密闭容器中合成甲醇,实验测得不同温度及压强下,平衡时甲醇的物质的量变化如图所示。则该反应的正反应为

②若将物质的量之比为1:3的CO2和H2充入体积为1.0L的恒容密闭容器中反应,不同压强下CO2转化率随温度的变化关系如下图所示。

a.A、B两条曲线的压强分别为
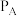 、
、 ,则
,则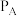
 (填“>”“<”或“=”);
(填“>”“<”或“=”);b.若A曲线条件下,起始充入CO2和H2的物质的量分别为lmol、3mol,且a点时的K=300(L2/mol2),则a点对应CO2转化率为
(2)在工业生产中也用反应CO(g)+H2O(g)=CO2(g)+H2(g) ΔH=-41.2kJ·mol-1制取H2,从而获得氢能源,该反应需要加入催化剂,若用[M]表示催化剂,则反应历程可表示为:
第一步:[M]+H2O(g)=[M]O+H2(g)
第二步:[M]O+CO(g)=[M]+CO2(g)
①第二步比第一步反应慢,则第二步反应的活化能比第一步
②研究表明,此反应的速率方程为
 ,式中)
,式中)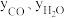 、
、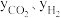 分别表示相应的物质的量分数,Kp为平衡常数,k为反应的速率常数,温度升高时k值增大。在气体组成和催化剂一定的情况下,反应速率随温度变化的曲线如图所示。温度升高时,该反应的Kp
分别表示相应的物质的量分数,Kp为平衡常数,k为反应的速率常数,温度升高时k值增大。在气体组成和催化剂一定的情况下,反应速率随温度变化的曲线如图所示。温度升高时,该反应的Kp
(3)以甲醇为主要原料,电化学合成碳酸二甲酯的工作原理如图所示。阳极的电极反应式为

您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐3】如图所示,若电解5 min时,测得铜电极的质量增加2.16 g。试回答:

(1)电源中X极是________ (填“正”或“负”)极。
(2)通电5 min时,B中共收集到224 mL(标准状况)气体,溶液体积为200 mL(电解前后溶液的体积变化忽略不计),则通电前c(CuSO4)=________ 。
(3)若A中KCl溶液的体积也是200 mL,电解后溶液中仍有Cl-,则电解后溶液的c(OH-)=________ 。
(4)二氧化碳是地球温室效应的罪魁祸首,目前人们处理二氧化碳的方法之一是使其与氢气合成为甲醇,甲醇是汽车燃料电池的重要燃料。已知氢气、甲醇燃烧的热化学方程式如下:
2H2(g)+O2(g)===2H2O(l) ΔH=-570 kJ·mol-1 ①
2CH3OH(l)+ 3O2(g)===2CO2(g)+4H2O(l) ΔH=-1452 kJ·mol-1 ②
写出二氧化碳与氢气合成甲醇液体的热化学方程式:_________________________________ 。

(1)电源中X极是
(2)通电5 min时,B中共收集到224 mL(标准状况)气体,溶液体积为200 mL(电解前后溶液的体积变化忽略不计),则通电前c(CuSO4)=
(3)若A中KCl溶液的体积也是200 mL,电解后溶液中仍有Cl-,则电解后溶液的c(OH-)=
(4)二氧化碳是地球温室效应的罪魁祸首,目前人们处理二氧化碳的方法之一是使其与氢气合成为甲醇,甲醇是汽车燃料电池的重要燃料。已知氢气、甲醇燃烧的热化学方程式如下:
2H2(g)+O2(g)===2H2O(l) ΔH=-570 kJ·mol-1 ①
2CH3OH(l)+ 3O2(g)===2CO2(g)+4H2O(l) ΔH=-1452 kJ·mol-1 ②
写出二氧化碳与氢气合成甲醇液体的热化学方程式:
您最近一年使用:0次
计算题
|
适中
(0.65)
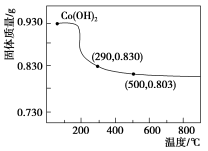
【推荐1】在空气中加热Co(OH)2,使其转化为钴的氧化物。加热过程中,固体质量与温度的关系如图所示。290~500℃,发生反应的化学方程式为___ 。

您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】为了测定某铜银合金的成分,将30.0g合金溶于80mL13.5mol·L-1的浓HNO3中,待合金完全溶解后,收集到气体6.72L(标准状况),并测得溶液中c(H+)=1mol·L-1。假设反应后溶液的体积仍为80mL,试计算:
①被还原的HNO3的物质的量是_______ ;(只写结果)
②合金中铜的质量分数为_______ 。(写出计算过程)
①被还原的HNO3的物质的量是
②合金中铜的质量分数为
您最近一年使用:0次

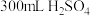 和
和 的混合溶液,将其分成三等份,向第一份中加入
的混合溶液,将其分成三等份,向第一份中加入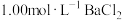 溶液,至恰好不再产生沉淀,消耗100mL,将沉淀过滤、洗涤、干燥,称其质量为m g;向第二份溶液中加入铁片,充分反应后,取出铁片,洗涤、烘干,称量其质量比原来减轻了0.56g;向第三份溶液加入
溶液,至恰好不再产生沉淀,消耗100mL,将沉淀过滤、洗涤、干燥,称其质量为m g;向第二份溶液中加入铁片,充分反应后,取出铁片,洗涤、烘干,称量其质量比原来减轻了0.56g;向第三份溶液加入 的NaOH溶液,当沉淀量达最大时,所加入NaOH溶液的体积为V mL。试计算:
的NaOH溶液,当沉淀量达最大时,所加入NaOH溶液的体积为V mL。试计算: