恒温恒容条件下,能说明反应A(s)+ 2B(g) C(g)+ D(g)一定处于化学平衡状态的是
C(g)+ D(g)一定处于化学平衡状态的是
 C(g)+ D(g)一定处于化学平衡状态的是
C(g)+ D(g)一定处于化学平衡状态的是| A.混合气体的密度不再改变 | B.容器内的压强保持不变 |
| C.C与D的物质的量相等 | D.消耗1 mol B的同时生成 0.5 mol D |
更新时间:2018-10-27 17:02:43
|
【知识点】 化学平衡状态的判断方法解读
相似题推荐
单选题
|
适中
(0.65)
解题方法
【推荐1】在一定条件下,将3 molA和 1 molB混合于固定容积为2 L的密闭容器中,发生如下反应:3A(g)+B(g) xCg)+2D(g)。2 min末该反应达到平衡,生成0.8 molD,得C的浓度为0.2mol/L,下列判断错误的是
xCg)+2D(g)。2 min末该反应达到平衡,生成0.8 molD,得C的浓度为0.2mol/L,下列判断错误的是
 xCg)+2D(g)。2 min末该反应达到平衡,生成0.8 molD,得C的浓度为0.2mol/L,下列判断错误的是
xCg)+2D(g)。2 min末该反应达到平衡,生成0.8 molD,得C的浓度为0.2mol/L,下列判断错误的是| A.x=1 |
| B.0~2min内A的平均反应速率为0.1mol/(L·min) |
| C.A的转化率为40% |
| D.若混合气体的平均相对分子质量不变,则表明该反应达到平衡状态 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】对于反应 N2O4(g)⇌2NO2(g) ΔH=+57 kJ·mol-1,下列有关说法正确的是
| A.升高体系温度正反应速率增大,逆反应速率减小 |
| B.若容器体积不变,密度不变时说明该反应建立化学平衡 |
C.其它条件不变,向平衡后的容器中再加入少量N2O4,新平衡后 的值不变 的值不变 |
| D.增大体系的压强能提高 N2O4的反应速率和平衡转化率 |
您最近一年使用:0次

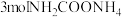 ,发生反应:
,发生反应: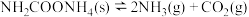 。10min时达平衡,此时
。10min时达平衡,此时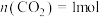 ,下列说法正确的是
,下列说法正确的是
 ,平衡向正反应方向移动
,平衡向正反应方向移动

