已知化合物X由3种元素组成,某学习小组进行了如下实验:
①取适量X,加水完全溶解,无气体产生,溶液呈碱性;进行焰色反应,透过蓝色钴玻璃观察到火焰呈紫色;
②取1.685gX溶于水,加入含HCl 0.02000mol的盐酸恰好中和;中和后的溶液与硝酸酸化的过量AgNO3溶液反应,得到4.305g白色沉淀。
请回答:
(1)X中3种元素是___________ (用元素符号表示);
(2)X与水反应的化学方程式是___________ ;
(3)X中一种元素对应的单质,可与足量的Na2CO3溶液反应得到Cl2O,写出该反应的化学方程式:___________ 。
①取适量X,加水完全溶解,无气体产生,溶液呈碱性;进行焰色反应,透过蓝色钴玻璃观察到火焰呈紫色;
②取1.685gX溶于水,加入含HCl 0.02000mol的盐酸恰好中和;中和后的溶液与硝酸酸化的过量AgNO3溶液反应,得到4.305g白色沉淀。
请回答:
(1)X中3种元素是
(2)X与水反应的化学方程式是
(3)X中一种元素对应的单质,可与足量的Na2CO3溶液反应得到Cl2O,写出该反应的化学方程式:
2019·浙江·高考真题 查看更多[6]
2018年11月浙江省普通高校招生选考科目考试化学试题浙江省2019届高三11月选考科目考试化学试卷高一必修第一册(苏教2019版)专题3 C 高考挑战区 过模拟 2年模拟精编精练(已下线)【浙江新东方】8(已下线)【浙江新东方】高中化学20210513-030【2021】【高一下】(已下线)专题19.无机综合推断-十年(2012-2021)高考化学真题分项汇编(浙江专用)
更新时间:2018-11-07 22:38:52
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】产自我国西北某盐湖的“块碱”是一种Na2CO3和NaCl的混合物。可通过以下方法对块碱样品的组成和含量进行分析测定。
Ⅰ.定性测定NaCl的存在:
(1)取样品少许溶于水,加入足量稀硝酸充分反应后再滴加_________________ 溶液,能观察到有_______________________ 产生,说明块碱中含有NaCl。
Ⅱ.定量测定Na2CO3的含量:
准确称量w g样品置于如下装置中,向其中加入足量稀硫酸,通过测定生成气体的体积来求算Na2CO3的含量。请回答下列相关问题:

(2)测定装置中,导管a的作用是___________________________________________ 。
(3)为提高测定的准确度,溶液b最宜选用___________________________________ 。
①饱和食盐水 ②饱和NaHCO3溶液 ③澄清石灰水 ④酸性KMnO4溶液
(4)若根据所取样品的质量估计反应时产生的气体体积最多在30mL左右,则产生气体前对量气装置读数时,装置内的装液量和液面调节最为合理的是_______________________ (填虚线框中对应这的字母编号)。
(5)用你以上所选出的最为合理的读数为起点,若终点读数为17.60mL,则反应所产生的气体的测定体积为_____________ mL。若实验温度下的气体摩尔体积为VmL.mol-1,由此可得出样品中Na2CO3的含量表达式为: __________________ 。
Ⅰ.定性测定NaCl的存在:
(1)取样品少许溶于水,加入足量稀硝酸充分反应后再滴加
Ⅱ.定量测定Na2CO3的含量:
准确称量w g样品置于如下装置中,向其中加入足量稀硫酸,通过测定生成气体的体积来求算Na2CO3的含量。请回答下列相关问题:

(2)测定装置中,导管a的作用是
(3)为提高测定的准确度,溶液b最宜选用
①饱和食盐水 ②饱和NaHCO3溶液 ③澄清石灰水 ④酸性KMnO4溶液
(4)若根据所取样品的质量估计反应时产生的气体体积最多在30mL左右,则产生气体前对量气装置读数时,装置内的装液量和液面调节最为合理的是
(5)用你以上所选出的最为合理的读数为起点,若终点读数为17.60mL,则反应所产生的气体的测定体积为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐2】某无色透明溶液中可能大量存在Ag+、Ca2+、Cu2+、Fe3+、Na+中的几种,请填写下列空白:
(1)不做任何实验就可以肯定原溶液中不存在的离子是_______ 。
(2)取少量原溶液,加入过量稀盐酸,有白色沉淀生成再加入过量的稀硝酸,沉淀不消失,说明原溶液中肯定存在的离子是_______ 。
(3)取(2)中的滤液,加入过量的碳酸钠溶液,出现白色沉淀,说明原溶液中肯定有_______ ,写出生成该白色沉淀的离子方程式为_______ 。
(4)原溶液可能大量共存的阴离子是_______(填字母)。
(1)不做任何实验就可以肯定原溶液中不存在的离子是
(2)取少量原溶液,加入过量稀盐酸,有白色沉淀生成再加入过量的稀硝酸,沉淀不消失,说明原溶液中肯定存在的离子是
(3)取(2)中的滤液,加入过量的碳酸钠溶液,出现白色沉淀,说明原溶液中肯定有
(4)原溶液可能大量共存的阴离子是_______(填字母)。
| A.OH— | B. | C. | D.Cl— |
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】实验室欲用碳酸钠晶体( )配制500
)配制500 0.5
0.5 的
的 溶液,据此回答下列问题:
溶液,据此回答下列问题:
(1)需称量碳酸钠晶体___________ g。(精确到小数点后一位)
(2)在配制的过程中一定不需要用到的仪器是___________ (填字母),还缺少的仪器有___________ 。
A.烧杯 B.药匙 C.玻璃棒 D.托盘天平 E.锥形瓶 F.胶头滴管 G.量筒
(3)配制过程中,如果不小心加水超过刻度线,应该怎么办?___________ 。
(4)下列的实验操作可能导致配制的溶液浓度偏高的是___________(填字母)。
(5)若碳酸钠晶体中混有少量的 ,简述检验其中
,简述检验其中 的实验操作与现象:
的实验操作与现象:___________ 。
 )配制500
)配制500 0.5
0.5 的
的 溶液,据此回答下列问题:
溶液,据此回答下列问题:(1)需称量碳酸钠晶体
(2)在配制的过程中一定不需要用到的仪器是
A.烧杯 B.药匙 C.玻璃棒 D.托盘天平 E.锥形瓶 F.胶头滴管 G.量筒
(3)配制过程中,如果不小心加水超过刻度线,应该怎么办?
(4)下列的实验操作可能导致配制的溶液浓度偏高的是___________(填字母)。
| A.容量瓶内原来存有少量的水 |
| B.定容时液面超过刻度线,用胶头滴管吸出 |
| C.碳酸钠晶体久置已部分失去结晶水 |
| D.定容时俯视刻度线 |
 ,简述检验其中
,简述检验其中 的实验操作与现象:
的实验操作与现象:
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
【推荐1】NaCl是重要的化工原料。回答下列问题:
(1)元素Na的焰色呈_______ 色。价层电子被激发到相邻高能级后形成的激发态Na且原子,其价层电子轨道表示式为_______ 。
(2)KBr具有NaCl型的晶体结构,但其熔点比NaCl低,原因是_______ 。
(3)在适当的条件下,电解NaCl水溶液可制得 其中
其中 离子的几何构型为
离子的几何构型为_______ ,中心原子的杂化方式为_______ 。
(4)NaCl晶体在50~300 GPa的高压下和 反应,可以形成一种晶体,其立方晶胞如图所示(白球为Cl,黑球为Na)。
反应,可以形成一种晶体,其立方晶胞如图所示(白球为Cl,黑球为Na)。

已知晶胞参数为a pm。阿伏加德罗常数的值为 ,则该晶体的密度为
,则该晶体的密度为_______  (列出计算式)。
(列出计算式)。
(1)元素Na的焰色呈
(2)KBr具有NaCl型的晶体结构,但其熔点比NaCl低,原因是
(3)在适当的条件下,电解NaCl水溶液可制得
 其中
其中 离子的几何构型为
离子的几何构型为(4)NaCl晶体在50~300 GPa的高压下和
 反应,可以形成一种晶体,其立方晶胞如图所示(白球为Cl,黑球为Na)。
反应,可以形成一种晶体,其立方晶胞如图所示(白球为Cl,黑球为Na)。
已知晶胞参数为a pm。阿伏加德罗常数的值为
 ,则该晶体的密度为
,则该晶体的密度为 (列出计算式)。
(列出计算式)。
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐2】现有金属单质A、B和气体甲、乙、丙以及物质C、D、E、F,它们之间能发生图中反应。(图中有些反应的产物和反应条件没有标出)
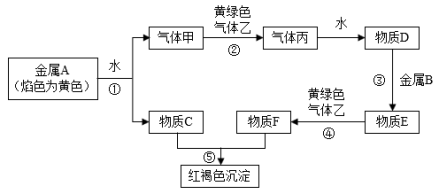
(1)金属A的化学式为_______ ,金属B的化学式为_______ ,乙的化学式为_______ ,丙的化学式为_______ 。
(2)写出下列反应的离子方程式:
③_______ ;
④_______ ;
⑤_______ 。

(1)金属A的化学式为
(2)写出下列反应的离子方程式:
③
④
⑤
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐3】短周期元素的单质及其化合物应用广泛。回答下列问题:
(1)红磷和白磷属于_______ (填“同素异形体”或“同位素”)。
(2)人们通过焰色试验制造了绚丽多彩的烟花,下列焰色为黄色的是_______ (填“ ”或“
”或“ ”)。
”)。
(3) 在元素周期表中的位置是
在元素周期表中的位置是______________ 。
(4)化合物 遇水反应生成氨气
遇水反应生成氨气 和一种强碱,该反应的化学方程式为
和一种强碱,该反应的化学方程式为______________ 。
(5)C1、S、P的最简单氢化物的热稳定性由大到小的顺序为______________ (用“>”将其氢化物连接起来)。请设计验证 的非金属性大于S的方法:
的非金属性大于S的方法:______________ (任写一种即可)。
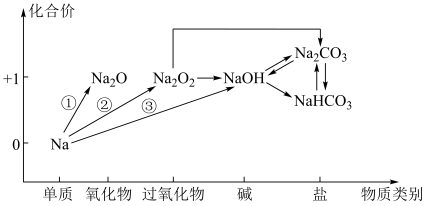
(6)已知钠及其化合物的“价-类”二维图如下。反应①②③转化的共同特征是均加入了_______ (填“氧化剂”或“还原剂”)。反应③的离子方程式为______________ 。
(1)红磷和白磷属于
(2)人们通过焰色试验制造了绚丽多彩的烟花,下列焰色为黄色的是
 ”或“
”或“ ”)。
”)。(3)
 在元素周期表中的位置是
在元素周期表中的位置是(4)化合物
 遇水反应生成氨气
遇水反应生成氨气 和一种强碱,该反应的化学方程式为
和一种强碱,该反应的化学方程式为(5)C1、S、P的最简单氢化物的热稳定性由大到小的顺序为
 的非金属性大于S的方法:
的非金属性大于S的方法:(6)已知钠及其化合物的“价-类”二维图如下。反应①②③转化的共同特征是均加入了
您最近一年使用:0次
【推荐1】某澄清溶液,可能含有 、Na+、K+、Cl-、
、Na+、K+、Cl-、 、
、 中的一种或几种,现做如下实验:
中的一种或几种,现做如下实验:
①取少量该溶液加入BaCl2溶液有白色沉淀生成,再加入足量盐酸后,沉淀部分溶解,并有气体生成。
②用铂丝蘸取少量该溶液置于无色酒精灯火焰中灼烧,火焰呈黄色,透过蓝色钴玻璃观察,未见紫色火焰。
③另取少量该溶液加入NaOH溶液并加热,将湿润的红色石蕊试纸靠近试管口无颜色变化。
(1)第①步可以检验出的离子是____________ 。
(2)第②③步说明一定含有的离子是__________ 。
(3)从以上操作中,不能判断是否存在的离子是____ ,为了检验该离子是否存在,请你写出进一步检验的操作步骤和实验现象:___________ 。
 、Na+、K+、Cl-、
、Na+、K+、Cl-、 、
、 中的一种或几种,现做如下实验:
中的一种或几种,现做如下实验:①取少量该溶液加入BaCl2溶液有白色沉淀生成,再加入足量盐酸后,沉淀部分溶解,并有气体生成。
②用铂丝蘸取少量该溶液置于无色酒精灯火焰中灼烧,火焰呈黄色,透过蓝色钴玻璃观察,未见紫色火焰。
③另取少量该溶液加入NaOH溶液并加热,将湿润的红色石蕊试纸靠近试管口无颜色变化。
(1)第①步可以检验出的离子是
(2)第②③步说明一定含有的离子是
(3)从以上操作中,不能判断是否存在的离子是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐2】有一包白色固体粉末,其中可能含有KMnO4、NaNO3、BaCl2、Na2SO4、Na2CO3中的一种或几种,现做以下实验:
①将部分粉末加入水中,振荡,有白色沉淀生成,过滤后溶液呈无色;
②向①的沉淀物中加入足量稀硝酸,固体部分溶解,并有气泡产生;
③取少量②的溶液,滴入稀硫酸,有白色沉淀产生;
④另取①中过滤后的溶液于试管中,向该试管中加入足量硝酸银溶液产生白色沉淀。
试根据上述实验事实,回答下列问题:
(1)原白色粉末中一定不含有的物质是__________ (填化学式,下同),一定含有的物质是_____________ ,可能含有的物质是______________ 。
(2)写出下列步骤中发生的离子方程式:
①________
②________
④_______
①将部分粉末加入水中,振荡,有白色沉淀生成,过滤后溶液呈无色;
②向①的沉淀物中加入足量稀硝酸,固体部分溶解,并有气泡产生;
③取少量②的溶液,滴入稀硫酸,有白色沉淀产生;
④另取①中过滤后的溶液于试管中,向该试管中加入足量硝酸银溶液产生白色沉淀。
试根据上述实验事实,回答下列问题:
(1)原白色粉末中一定不含有的物质是
(2)写出下列步骤中发生的离子方程式:
①
②
④
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】(NH4)2Fe(SO4)2·6H2O(M=392g/mol)又称摩尔盐,简称FAS,它是浅蓝色绿色晶体,可溶于水,难溶于水乙醇。某小组利用工业废铁屑进行下列实验。请按要求回答下列问题:
Ⅰ. FAS的制取。流程如下:
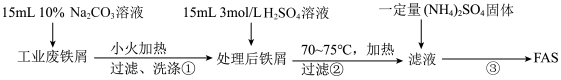
(1)步骤①加热的目的是_________________________ 。
(2)步骤②必须在剩余少量铁屑时进行过滤,其原因是(用离子方程式表示):______________ 。
Ⅱ.NH4+含量的测定。装置如图所示:
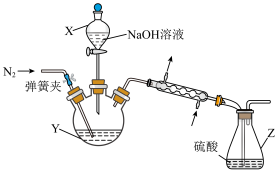
实验步骤:①称取FAS样品a g,加水溶解后,将溶液注入Y中
②量取b mL c1 mol/LH2SO4溶液于Z中
③向Y加入足量NaOH浓溶液,充分反应后通入气体N2,加热(假设氨完全蒸出),蒸氨结束后取下Z。
④用c2mol/LNaOH标准溶液滴定Z中过量的硫酸,滴定终点时消耗d mLNaOH标准溶液。
(3)仪器X的名称______________ ;N2的电子式为______________ 。
(4)步骤③蒸氨结束后,为了减少实验误差,还需要对直形冷凝管进行处理的操作是__________________ ;NH4+质量百分含量为(用代数式表示)__________________ 。
Ⅲ. FAS纯度的测定。称取FAS m g样品配制成500 mL待测溶液。分别取20.00mL待测溶液,进行如下方案实验:
(5)方案一:用0.01000mol/L的酸性KMnO4溶液进行滴定。滴定过程中需用到的仪器中(填图中序号)_________ 。滴定中反应的离子方程式为____________________ 。
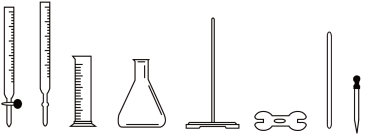
① ② ③ ④ ⑤ ⑥ ⑦ ⑧
(6)方案二: 待测液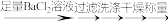 固体n g ;则FAS的质量百分含量为(用代数式表示)
固体n g ;则FAS的质量百分含量为(用代数式表示)_____________________________ 。
(7)方案一、二实验操作均正确,却发现方案一测定结果总是小于方案二的,其可能的原因是_______________ ;为验证该猜测正确,设计后续实验操作为_________________ ,现象为______________ 。
Ⅰ. FAS的制取。流程如下:

(1)步骤①加热的目的是
(2)步骤②必须在剩余少量铁屑时进行过滤,其原因是(用离子方程式表示):
Ⅱ.NH4+含量的测定。装置如图所示:

实验步骤:①称取FAS样品a g,加水溶解后,将溶液注入Y中
②量取b mL c1 mol/LH2SO4溶液于Z中
③向Y加入足量NaOH浓溶液,充分反应后通入气体N2,加热(假设氨完全蒸出),蒸氨结束后取下Z。
④用c2mol/LNaOH标准溶液滴定Z中过量的硫酸,滴定终点时消耗d mLNaOH标准溶液。
(3)仪器X的名称
(4)步骤③蒸氨结束后,为了减少实验误差,还需要对直形冷凝管进行处理的操作是
Ⅲ. FAS纯度的测定。称取FAS m g样品配制成500 mL待测溶液。分别取20.00mL待测溶液,进行如下方案实验:
(5)方案一:用0.01000mol/L的酸性KMnO4溶液进行滴定。滴定过程中需用到的仪器中(填图中序号)

① ② ③ ④ ⑤ ⑥ ⑦ ⑧
(6)方案二: 待测液
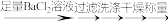 固体n g ;则FAS的质量百分含量为(用代数式表示)
固体n g ;则FAS的质量百分含量为(用代数式表示)(7)方案一、二实验操作均正确,却发现方案一测定结果总是小于方案二的,其可能的原因是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】用MnO2与浓盐酸反应制取Cl2,再用铜粉和Cl2反应制取少量CuCl2,实验流程如图:

(1)装置A中的化学反应方程式为_______ ;
(2)装置A选择图中的_______

(3)判断已有CuCl2生成的现象是_______ ;将产物溶于水后,证明溶液中含有氯离子所用的试剂为_______
(4)E中常用_______ 吸收尾气,发生反应的化学方程式为_______ 。

(1)装置A中的化学反应方程式为
(2)装置A选择图中的

(3)判断已有CuCl2生成的现象是
(4)E中常用
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】(1)选择下列实验方法分离物质,将分离方法的序号填在横线上。
A 萃取 B 升华 C 结晶 D 分液 E 蒸馏 F 过滤
①分离饱和食盐水与沙子的混合物。_________
②从硝酸钾和氯化钠的混合液中获得硝酸钾晶体。_____
③分离CCl4(沸点为76.75°C)和甲苯(沸点为110.6°C)的互溶混合物。________
④已知丙酮(C3H6O)通常是无色液体,不溶于水,密度小于1g/mL,沸点约为55°C。要从水与丙酮的混合液里将丙酮分离出来。____
⑤分离NaCl固体和单质碘固体的混合物。____
(2)某溶液中含有较大量的Cl—、CO32—、OH—等三种阴离子,如果只取一次该溶液就能分别将三种阴离子依次检验出来,下列实验操作顺序正确的是。________
①滴加Ba(NO3)2溶液 ②过滤 ③滴加AgNO3溶液 ④滴加Mg(NO3)2
A.①②③②④ B.④②③②① C.①②④②③ D.④②①②③
A 萃取 B 升华 C 结晶 D 分液 E 蒸馏 F 过滤
①分离饱和食盐水与沙子的混合物。
②从硝酸钾和氯化钠的混合液中获得硝酸钾晶体。
③分离CCl4(沸点为76.75°C)和甲苯(沸点为110.6°C)的互溶混合物。
④已知丙酮(C3H6O)通常是无色液体,不溶于水,密度小于1g/mL,沸点约为55°C。要从水与丙酮的混合液里将丙酮分离出来。
⑤分离NaCl固体和单质碘固体的混合物。
(2)某溶液中含有较大量的Cl—、CO32—、OH—等三种阴离子,如果只取一次该溶液就能分别将三种阴离子依次检验出来,下列实验操作顺序正确的是。
①滴加Ba(NO3)2溶液 ②过滤 ③滴加AgNO3溶液 ④滴加Mg(NO3)2
A.①②③②④ B.④②③②① C.①②④②③ D.④②①②③
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】在某澄清溶液中,可能存在下列几种离子:H+、K+、Ba2+、SO42-、Cl-、SiO32-。取该溶液进行下列实验:
①用pH试纸检验该溶液呈强酸性;
②另取部分溶液逐滴加入NaOH溶液,当溶液呈碱性时,再加入Na2CO3溶液,有白色沉淀生成。
回答下列问题:
(1)根据上述实验现象,推断原溶液中肯定存在的离子是___ ,肯定不存在的离子是___ ,可能存在的离子是___ 。要检验可能存在的离子,可采用的实验方法是___ 。
(2)写出实验②中发生反应的离子方程式:___ 、___ 。
①用pH试纸检验该溶液呈强酸性;
②另取部分溶液逐滴加入NaOH溶液,当溶液呈碱性时,再加入Na2CO3溶液,有白色沉淀生成。
回答下列问题:
(1)根据上述实验现象,推断原溶液中肯定存在的离子是
(2)写出实验②中发生反应的离子方程式:
您最近一年使用:0次



