某化工厂分析人员从生产车间取过氧化氢样品1.00mL于锥形瓶中,加入适量蒸馏水稀释,再用稀硫酸酸化后,逐滴加入0.10 mol·L-1的KMnO4溶液,当反应完全时,消耗KMnO4溶液25.00 mL,相关反应的化学方的程式为:2KMnO4+5H2O2+3H2SO4=K2SO4+2MnSO4+5O2↑+8H2O
(1)已知过氧化氢不稳定,试写出过氧化氢发生分解反应的化学方程式,并用双线桥标出电子转移的方向和数目_____________________________________________________ 。
(2)通过计算确定该过氧化氢样品的物质的量浓度(写出计算过程)______________ 。
(1)已知过氧化氢不稳定,试写出过氧化氢发生分解反应的化学方程式,并用双线桥标出电子转移的方向和数目
(2)通过计算确定该过氧化氢样品的物质的量浓度(写出计算过程)
更新时间:2018-11-25 11:39:17
|
相似题推荐
计算题
|
适中
(0.65)
名校
解题方法
【推荐1】完成下列小题
(1) 溶液含中,含
溶液含中,含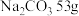 ,则该溶液中
,则该溶液中 的物质的量浓度
的物质的量浓度_____  。
。
(2)对于反应: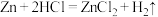 ,现有
,现有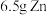 放入
放入 的
的 溶液中充分反应后,溶液中存在的溶质有
溶液中充分反应后,溶液中存在的溶质有_____ 。
(3)对于反应: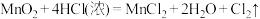 。
。
①用双线桥法表示上述反应电子转移的方向和数目_____ 。
②上述反应中还原剂是_____ ,若该反应有中有 电子转移,实际参加反应的
电子转移,实际参加反应的 质量
质量_____ g,生成氯在气在STP时体积是_____ L。
③若使用浓盐酸的质量分数0.365、密度 ,该浓盐酸物质的量浓度是
,该浓盐酸物质的量浓度是_____  。
。
(1)
 溶液含中,含
溶液含中,含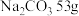 ,则该溶液中
,则该溶液中 的物质的量浓度
的物质的量浓度 。
。(2)对于反应:
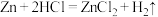 ,现有
,现有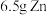 放入
放入 的
的 溶液中充分反应后,溶液中存在的溶质有
溶液中充分反应后,溶液中存在的溶质有(3)对于反应:
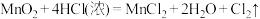 。
。①用双线桥法表示上述反应电子转移的方向和数目
②上述反应中还原剂是
 电子转移,实际参加反应的
电子转移,实际参加反应的 质量
质量③若使用浓盐酸的质量分数0.365、密度
 ,该浓盐酸物质的量浓度是
,该浓盐酸物质的量浓度是 。
。
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】(1)若要配制100mL 0.1mol·L的Na2SO4溶液,需称量Na2SO4的质量为_____ ;
(2)将2240mL(标准状况)氨完全溶于水配成100mL溶液,求氨水中NH3的物质的量浓度为______________ (不考虑NH3与H2O的反应)
(3)在上一题的研究性学习中,若需要制取2240mL(标准状况)氨,求至少需要氯化铵的质量________ 。
(2)将2240mL(标准状况)氨完全溶于水配成100mL溶液,求氨水中NH3的物质的量浓度为
(3)在上一题的研究性学习中,若需要制取2240mL(标准状况)氨,求至少需要氯化铵的质量
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐3】化学计量在化学中占有重要地位。回答下列问题:
(1)相同质量SO2和SO3所含的原子个数比是___________ 。
(2)同温同压下,等体积的N2和O2的质量之比为___________ 。
(3)溶质质量为29.4 g的硫酸溶液中含有___________ mol SO 。
。
(4)标准状况下6.72 L NH3分子中所含原子数与___________ g H2O所含原子数相等。
(5)0.5 L 1 mol·L-1 FeCl3溶液与0.2 L 1 mol· L-1 KCl 溶液中的Cl-的数目之比为___________ 。
(6)用MnO2和浓盐酸制取氯气,当4 mol氯化氢被氧化时,生成的氯气的体积(标况)是___________ 。
(1)相同质量SO2和SO3所含的原子个数比是
(2)同温同压下,等体积的N2和O2的质量之比为
(3)溶质质量为29.4 g的硫酸溶液中含有
 。
。(4)标准状况下6.72 L NH3分子中所含原子数与
(5)0.5 L 1 mol·L-1 FeCl3溶液与0.2 L 1 mol· L-1 KCl 溶液中的Cl-的数目之比为
(6)用MnO2和浓盐酸制取氯气,当4 mol氯化氢被氧化时,生成的氯气的体积(标况)是
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐1】钢铁是最重要、用量最大的金属材料之一。完成下列计算:
51.生产1吨含铁96%的生铁,至少需要氧化铁含量70%的赤铁矿(杂质不含铁)_____ 吨。(计算结果保留2位小数)
52.工业炼铁用一氧化碳还原氧化铁时会发生如下一系列反应:
3Fe2O3+CO=2Fe3O4+CO2
Fe3O4+CO=3FeO+CO2
FeO+CO=Fe+CO2
某次实验中,用CO还原4.80 g氧化铁,当固体质量变成4.56 g时,测得此固体中只存在2种氧化物。通过计算确定此固体可能的成分和它们的物质的量之比_____ 。
53.为了测定某碳素钢(假设只含铁和碳)的含碳量,将10.000 g钢样完全溶解于过量的热浓硝酸中,产生了0.300 mol气体(假设气体全部逸出,N2O4已折算为NO2)。气体用50.00 mL 12.00 mol/L的NaOH溶液完全吸收后,只生成两种盐,溶液蒸干后得到不含结晶水的固体32.664 g。计算:
(1)钢样的含碳量_____ 。
(2)参加反应的硝酸的物质的量_____ 。
51.生产1吨含铁96%的生铁,至少需要氧化铁含量70%的赤铁矿(杂质不含铁)
52.工业炼铁用一氧化碳还原氧化铁时会发生如下一系列反应:
3Fe2O3+CO=2Fe3O4+CO2
Fe3O4+CO=3FeO+CO2
FeO+CO=Fe+CO2
某次实验中,用CO还原4.80 g氧化铁,当固体质量变成4.56 g时,测得此固体中只存在2种氧化物。通过计算确定此固体可能的成分和它们的物质的量之比
53.为了测定某碳素钢(假设只含铁和碳)的含碳量,将10.000 g钢样完全溶解于过量的热浓硝酸中,产生了0.300 mol气体(假设气体全部逸出,N2O4已折算为NO2)。气体用50.00 mL 12.00 mol/L的NaOH溶液完全吸收后,只生成两种盐,溶液蒸干后得到不含结晶水的固体32.664 g。计算:
(1)钢样的含碳量
(2)参加反应的硝酸的物质的量
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】标准状况下,某气态烃A的密度是1.25g·L-1,取x L的A在足量的氧气中充分燃烧,生成的混合气体通入到50mLNaOH溶液,随后取此溶液25mL将其稀释至100mL,并向此稀释后的溶液中逐滴加入0.1mol·L-1的HCl溶液,产生的CO2气体体积与所加入的盐酸的体积之间的关系如图所示:

(1)A的摩尔质量为________________ 。
(2)请计算x的值(写出具体计算过程 )。________________

(1)A的摩尔质量为
(2)请计算x的值(
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐1】完成下列小题
(1) 溶液含中,含
溶液含中,含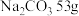 ,则该溶液中
,则该溶液中 的物质的量浓度
的物质的量浓度_____  。
。
(2)对于反应: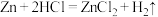 ,现有
,现有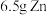 放入
放入 的
的 溶液中充分反应后,溶液中存在的溶质有
溶液中充分反应后,溶液中存在的溶质有_____ 。
(3)对于反应: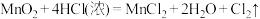 。
。
①用双线桥法表示上述反应电子转移的方向和数目_____ 。
②上述反应中还原剂是_____ ,若该反应有中有 电子转移,实际参加反应的
电子转移,实际参加反应的 质量
质量_____ g,生成氯在气在STP时体积是_____ L。
③若使用浓盐酸的质量分数0.365、密度 ,该浓盐酸物质的量浓度是
,该浓盐酸物质的量浓度是_____  。
。
(1)
 溶液含中,含
溶液含中,含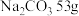 ,则该溶液中
,则该溶液中 的物质的量浓度
的物质的量浓度 。
。(2)对于反应:
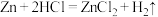 ,现有
,现有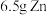 放入
放入 的
的 溶液中充分反应后,溶液中存在的溶质有
溶液中充分反应后,溶液中存在的溶质有(3)对于反应:
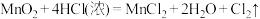 。
。①用双线桥法表示上述反应电子转移的方向和数目
②上述反应中还原剂是
 电子转移,实际参加反应的
电子转移,实际参加反应的 质量
质量③若使用浓盐酸的质量分数0.365、密度
 ,该浓盐酸物质的量浓度是
,该浓盐酸物质的量浓度是 。
。
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】在反应:3BrF3+5H2O= HBrO3+Br2+9HF十O2中(F为-1价)
(1)此反应中被氧化的元素是_________ 、被还原的元素是_____________ 。
(2)当有5mol水参加反应时,被氧化的水的物质的量为________ ,被还原的BrF3的物质的量为_________ 。
(1)此反应中被氧化的元素是
(2)当有5mol水参加反应时,被氧化的水的物质的量为
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐3】(1)写出NaHSO4在水中的电离方程式________ 。
(2)粗盐中含可溶性CaCl2、MgCl2及一些硫酸盐,要除去这些杂质,可选用以下试剂:①Na2CO3、②NaOH、③BaCl2、④HCl ,则试剂加入的先后顺序是__________ (填序号)。
(3)2KMnO4+16HCl(浓) =2KCl+2MnCl2+5Cl2↑+8H2O,用双线桥法标出该反应电子转移的方向和数目_______ ;若有0.1mol电子转移时生成Cl2的体积为__________ (标准状况),被氧化的HCl的物质的量为______________ 。
(4)某无色透明溶液可能含有K+、Cu2+、Ca2+、SO42-、CO32-、Cl﹣中的几种,现进行如下实验:
①滴加BaCl2溶液,有白色沉淀产生,将沉淀滤出。
②向上述沉淀中加入足量的稀硝酸,有部分沉淀溶解。
③向滤液加入AgNO3溶液,有白色沉淀生成,该沉淀不溶于稀HNO3。
试判断:该溶液中肯定有__________ ,肯定没有_________ ,可能有_________ (填离子符号)。
(2)粗盐中含可溶性CaCl2、MgCl2及一些硫酸盐,要除去这些杂质,可选用以下试剂:①Na2CO3、②NaOH、③BaCl2、④HCl ,则试剂加入的先后顺序是
(3)2KMnO4+16HCl(浓) =2KCl+2MnCl2+5Cl2↑+8H2O,用双线桥法标出该反应电子转移的方向和数目
(4)某无色透明溶液可能含有K+、Cu2+、Ca2+、SO42-、CO32-、Cl﹣中的几种,现进行如下实验:
①滴加BaCl2溶液,有白色沉淀产生,将沉淀滤出。
②向上述沉淀中加入足量的稀硝酸,有部分沉淀溶解。
③向滤液加入AgNO3溶液,有白色沉淀生成,该沉淀不溶于稀HNO3。
试判断:该溶液中肯定有
您最近一年使用:0次

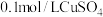 溶液
溶液 ,应用托盘天平称取
,应用托盘天平称取 的质量为
的质量为

