实验室可用MnO2和浓盐酸反应制取氯气:MnO2+4HCl(浓) MnCl2+Cl2↑+2H2O。
MnCl2+Cl2↑+2H2O。
(1)用单线桥标出电子转移的方向和数目________________________ 。
(2)将上述化学方程式改写为离子方程式________________________ 。
(3)浓盐酸在反应中显示出来的性质是____________ (填序号) 。
①只有还原性 ②还原性和酸性 ③只有氧化性 ④氧化性和酸性
(4)若产生2mol Cl2,则被氧化的HCl_____ mol,转移的电子的数目为________ 。
 MnCl2+Cl2↑+2H2O。
MnCl2+Cl2↑+2H2O。(1)用单线桥标出电子转移的方向和数目
(2)将上述化学方程式改写为离子方程式
(3)浓盐酸在反应中显示出来的性质是
①只有还原性 ②还原性和酸性 ③只有氧化性 ④氧化性和酸性
(4)若产生2mol Cl2,则被氧化的HCl
更新时间:2018-12-17 22:08:55
|
相似题推荐
填空题
|
较易
(0.85)
【推荐1】硅是无机非金属材料的主角,硅的氧化物和硅酸盐占地壳质量的90%以上。
(1)保存NaOH溶液的试剂瓶不能用玻璃磨口塞,用离子方程式表示其原因___________ ,工艺师常用___________ (填物质名称)来雕刻玻璃。
(2)绿柱石(绿宝石矿藏的主要化学成分为BenAl2Si6O18,可用氧化物形式表示为nBeO•Al2O3•6SiO2,其n值为___________ 。
(3)用Na2SiO3水溶液浸泡过的棉花不易燃烧,说明Na2SiO3可用作___________ 。Na2SiO3可通过SiO2与纯碱混合高温熔融反应制得,高温熔融纯碱时下列坩埚可选用的是___________ (填字母)。
A.普通玻璃坩埚 B.石英玻璃坩埚 C.铁坩埚
(1)保存NaOH溶液的试剂瓶不能用玻璃磨口塞,用离子方程式表示其原因
(2)绿柱石(绿宝石矿藏的主要化学成分为BenAl2Si6O18,可用氧化物形式表示为nBeO•Al2O3•6SiO2,其n值为
(3)用Na2SiO3水溶液浸泡过的棉花不易燃烧,说明Na2SiO3可用作
A.普通玻璃坩埚 B.石英玻璃坩埚 C.铁坩埚
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】分类是认识和研究物质及其变化的一种常用的科学方法。回答下列问题:
(1)如图所示为树状分类法对物质进行的分类。
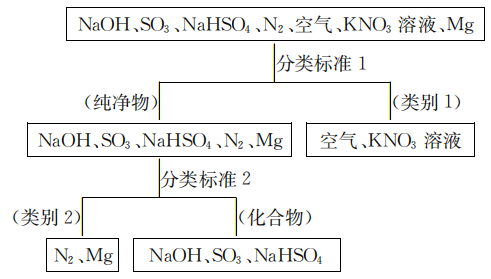
①分类标准1是___________ ,类别2是___________ 。
②上述物质中属于电解质的是___________ (填化学式,下同),属于非电解质的是___________ 。
③向NaHSO4溶液中加Mg可产生气体,反应的离子方程式是___________ 。
④将NaHSO4溶液和NaOH溶液混合,恰好呈中性,对应的离子方程式为___________ 。
(2)请对以下过程形成的分散系进行分类:
①碘和酒精的混合物;
②面粉加入水中后充分搅拌;
③氢氧化钡溶液中通入过量的CO2;
④向蒸馏水中加入氯化铵至恰好饱和;
⑤饱和氯化铁溶液中加入氢氧化钾溶液;
⑥用滤纸过滤氢氧化铁胶体后得到的滤液;
⑦将纳米材料分散在塑料中制备复合材料。
属于浊液的是___________ (填序号,下同);属于胶体的是___________ 。
(1)如图所示为树状分类法对物质进行的分类。

①分类标准1是
②上述物质中属于电解质的是
③向NaHSO4溶液中加Mg可产生气体,反应的离子方程式是
④将NaHSO4溶液和NaOH溶液混合,恰好呈中性,对应的离子方程式为
(2)请对以下过程形成的分散系进行分类:
①碘和酒精的混合物;
②面粉加入水中后充分搅拌;
③氢氧化钡溶液中通入过量的CO2;
④向蒸馏水中加入氯化铵至恰好饱和;
⑤饱和氯化铁溶液中加入氢氧化钾溶液;
⑥用滤纸过滤氢氧化铁胶体后得到的滤液;
⑦将纳米材料分散在塑料中制备复合材料。
属于浊液的是
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】回答下列问题
(1)1.5mol CH4约含有___________ 个CH4分子,质量为___________ g,标准状况下体积为___________ 升。49 gH2SO4溶于水得到0.5升溶液其物质的量浓度为___________ mol/L。
(2)碳酸钙是___________ (填电解质或非电解质),写出硫酸铝的电离方程式___________ 。
(3)实验室用碳酸钙与盐酸反应制取CO2气体,反应的离子方程式为___________ ;用澄清石灰水检验CO2气体的离子方程式是___________ 。
(4)标明下列氧化还原反应MnO2 + 4HCl(浓) MnCl2+Cl2↑+ 2H2O电子转移的方向和数目
MnCl2+Cl2↑+ 2H2O电子转移的方向和数目___________ (标在方程式上),其中MnO2为___________ (填还原剂或氧化剂)。
(1)1.5mol CH4约含有
(2)碳酸钙是
(3)实验室用碳酸钙与盐酸反应制取CO2气体,反应的离子方程式为
(4)标明下列氧化还原反应MnO2 + 4HCl(浓)
 MnCl2+Cl2↑+ 2H2O电子转移的方向和数目
MnCl2+Cl2↑+ 2H2O电子转移的方向和数目
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】ClO2(其中氧元素为-2价)是一种消毒杀菌效率高、二次污染小的水处理剂。实验室中可通过以下反应制得ClO2:2KClO3+H2C2O4+H2SO4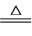 2ClO2↑+K2SO4+2CO2↑+2H2O。
2ClO2↑+K2SO4+2CO2↑+2H2O。
(1)该反应中氧化剂是__________ 。
(2)当收集到标况下气体22.4L时,求参加反应的H2C2O4质量和物质的量__________ 。
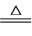 2ClO2↑+K2SO4+2CO2↑+2H2O。
2ClO2↑+K2SO4+2CO2↑+2H2O。(1)该反应中氧化剂是
(2)当收集到标况下气体22.4L时,求参加反应的H2C2O4质量和物质的量
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】回答下列问题:
(1)火药是中国古代“四大发明”之一。黑火药爆炸时发生如下反应: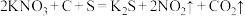 。其中被氧化的元素是
。其中被氧化的元素是_______ 。当生成22g 时,电子转移
时,电子转移_______ mol。
(2)阅读下列材料,回答有关问题:一个体重50kg的健康人,体内约含有2g铁,这2g铁在人体内不是以单质的形式存在,而是以 和
和 的形式存在。正二价铁离子易被吸收,给贫血者补充铁时,应给予含
的形式存在。正二价铁离子易被吸收,给贫血者补充铁时,应给予含 的亚铁盐,如硫酸亚铁。服用维生素C,可使食物中的
的亚铁盐,如硫酸亚铁。服用维生素C,可使食物中的 转变成
转变成 ,有利于人体吸收。
,有利于人体吸收。
①在人体中进行 和
和 的转化时,其中的
的转化时,其中的 作
作_______ 剂(填“氧化”或“还原”)。
②“服用维生素C,可使食物中的 转变成
转变成 ”这句话指出,维生素C在这一反应中具有
”这句话指出,维生素C在这一反应中具有_______ 性。(填“氧化”或“还原”)
(1)火药是中国古代“四大发明”之一。黑火药爆炸时发生如下反应:
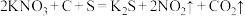 。其中被氧化的元素是
。其中被氧化的元素是 时,电子转移
时,电子转移(2)阅读下列材料,回答有关问题:一个体重50kg的健康人,体内约含有2g铁,这2g铁在人体内不是以单质的形式存在,而是以
 和
和 的形式存在。正二价铁离子易被吸收,给贫血者补充铁时,应给予含
的形式存在。正二价铁离子易被吸收,给贫血者补充铁时,应给予含 的亚铁盐,如硫酸亚铁。服用维生素C,可使食物中的
的亚铁盐,如硫酸亚铁。服用维生素C,可使食物中的 转变成
转变成 ,有利于人体吸收。
,有利于人体吸收。①在人体中进行
 和
和 的转化时,其中的
的转化时,其中的 作
作②“服用维生素C,可使食物中的
 转变成
转变成 ”这句话指出,维生素C在这一反应中具有
”这句话指出,维生素C在这一反应中具有
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐1】H2O2是一种重要的氧化剂,亦具有还原性。下列① ~ ④个涉及H2O2的反应(未配平、条件略)。①Na2O2+ HCl→NaCl + H2O2 ②H2O2 →H2O + O2③Ag2O + H2O2 →Ag + O2 + H2O ④H2O2 + Cr2(SO4)3+KOH→K2CrO4+K2SO4+H2O。
据此,填写下列空白:(1)[ ]H2O2 +[ ]Cr2(SO4)3+[ ]KOH→[ ]K2CrO4+[ ]K2SO4+[ ]H2O;配平上述反应④______________ ;并用单线桥标出电子转移方向与数目_________ ;当0.1mol氧化剂参加反应时,转移电子______ 个。
(2)H2O2仅体现还原性的反应是_____ (填代号),此反应中的氧化产物为___________ 。
(3)H2O2体现弱酸性的反应是______ (填代号),其理由为_______________ 。
据此,填写下列空白:(1)[ ]H2O2 +[ ]Cr2(SO4)3+[ ]KOH→[ ]K2CrO4+[ ]K2SO4+[ ]H2O;配平上述反应④
(2)H2O2仅体现还原性的反应是
(3)H2O2体现弱酸性的反应是
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】氧化还原反应在日常生产生活和科技创新发展等方面都具有广泛用途。
(1)为治理汽车尾气中的NO和CO对环境的污染,可在汽车排气管上安装催化转化器。汽车尾气中的NO和CO在催化剂作用下发生反应只生成 大气中两种常见的无公害气体。请写出上述反应的化学方程式:___________ 。
(2)吸入人体内的氧有2%转化为氧化性极强的“活性氧”,它能加速人体衰老,被称为“生命杀手”,服用含硒元素的化合物亚硒酸钠(Na2SeO3),能消除人体内的活性氧。说明NaSeO3具有___________ 性。
(3)储氢碳纳米管的研究成功体现了科技的进步。但用电弧法合成的碳纳米管常伴有大量的碳纳米颗粒杂质。这种碳纳米颗粒可用氧化气化法进行提纯:
①完成上述提纯反应的化学反应方程式,并单线桥标明电子转移方向和数目:__________
___C+___K2Cr2O7+____H2SO4=____CO2↑+____K2SO4+____Cr2(SO4)3+_____。
②该反应中还原剂是___________ (填化学式),被还原的元素是___________ (填元素符号)。
③该反应中,K2Cr2O7表现出___________ (填氧化性或者还原性)。
④每生成2分子水,转移___________ 个电子。
(1)为治理汽车尾气中的NO和CO对环境的污染,可在汽车排气管上安装催化转化器。汽车尾气中的NO和CO在催化剂作用下发生反应
(2)吸入人体内的氧有2%转化为氧化性极强的“活性氧”,它能加速人体衰老,被称为“生命杀手”,服用含硒元素的化合物亚硒酸钠(Na2SeO3),能消除人体内的活性氧。说明NaSeO3具有
(3)储氢碳纳米管的研究成功体现了科技的进步。但用电弧法合成的碳纳米管常伴有大量的碳纳米颗粒杂质。这种碳纳米颗粒可用氧化气化法进行提纯:
①完成上述提纯反应的化学反应方程式,并单线桥标明电子转移方向和数目:
___C+___K2Cr2O7+____H2SO4=____CO2↑+____K2SO4+____Cr2(SO4)3+_____。
②该反应中还原剂是
③该反应中,K2Cr2O7表现出
④每生成2分子水,转移
您最近一年使用:0次
【推荐3】已知下列反应:
①Cl2+2NaBr=2NaCl+Br2;
②2KI+Br2=2KBr+I2;
③Na2S+I2=2NaI+S↓。
(1)Cl-、Br-、I-、S2-四种离子的还原性由强到弱的顺序是__ 。
(2)判断Cl2与Na2S能否反应?__ (填“否”或书写离子反应方程式)。
(3)判断I2与NaBr能否反应?__ (填“否”或书写离子反应方程式)。
(4)已知NH3和Cl2可以发生氧化还原反应,配平该方程式并用单线桥表示电子转移的数目和方向:__NH3+__Cl2=__N2+__HCl。__
(5)在硫酸溶液中,NaClO3和Na2SO3能按粒子个数比1:2完全反应,生成一种棕黄色气体X,同时Na2SO3被氧化为Na2SO4,则X为__ 。
A.Cl2O7 B.ClO2 C.Cl2O D.Cl2
①Cl2+2NaBr=2NaCl+Br2;
②2KI+Br2=2KBr+I2;
③Na2S+I2=2NaI+S↓。
(1)Cl-、Br-、I-、S2-四种离子的还原性由强到弱的顺序是
(2)判断Cl2与Na2S能否反应?
(3)判断I2与NaBr能否反应?
(4)已知NH3和Cl2可以发生氧化还原反应,配平该方程式并用单线桥表示电子转移的数目和方向:__NH3+__Cl2=__N2+__HCl。
(5)在硫酸溶液中,NaClO3和Na2SO3能按粒子个数比1:2完全反应,生成一种棕黄色气体X,同时Na2SO3被氧化为Na2SO4,则X为
A.Cl2O7 B.ClO2 C.Cl2O D.Cl2
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐1】回答下列问题:
(1)H2O2水溶液称双氧水,医疗上利用它有杀菌消毒作用来清洗伤口,对下列两个涉及H2O2的反应,填写下列空白:
A.
B.
① H2O2仅体现氧化性的反应是_______ (填代号,下同);
② H2O2仅体现还原性的是_______ 。
(2)在一定条件下,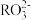 与Cl2反应如下:
与Cl2反应如下: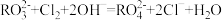 由以上反应可知上述过程中
由以上反应可知上述过程中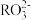 被
被_______ (填“氧化”或“还原”),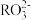 中元素R的化合价是
中元素R的化合价是_______ 。
(3)已知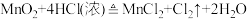
①当产生标准状况下11.2L的氯气时,被氧化的HCl的物质的量是_______ ;转移电子的数目是_______ 。
②浓盐酸所表现出的性质是_______ 。
a. 还原性 b. 酸性 c. 氧化性
(1)H2O2水溶液称双氧水,医疗上利用它有杀菌消毒作用来清洗伤口,对下列两个涉及H2O2的反应,填写下列空白:
A.

B.

① H2O2仅体现氧化性的反应是
② H2O2仅体现还原性的是
(2)在一定条件下,
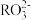 与Cl2反应如下:
与Cl2反应如下: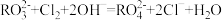 由以上反应可知上述过程中
由以上反应可知上述过程中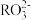 被
被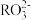 中元素R的化合价是
中元素R的化合价是(3)已知
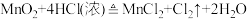
①当产生标准状况下11.2L的氯气时,被氧化的HCl的物质的量是
②浓盐酸所表现出的性质是
a. 还原性 b. 酸性 c. 氧化性
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】实验室用MnO2和浓盐酸制氯气的反应为MnO2+4HCl(浓) MnCl2+2H2O+Cl2↑。回答下列问题:
MnCl2+2H2O+Cl2↑。回答下列问题:
(1)用双线桥标出该反应的电子转移的方向和数目:________________________________________________________ 。
(2)如果反应中,如果有17.4 g纯MnO2被还原,那么被氧化的氯化氢的质量为______________ 。
 MnCl2+2H2O+Cl2↑。回答下列问题:
MnCl2+2H2O+Cl2↑。回答下列问题:(1)用双线桥标出该反应的电子转移的方向和数目:
(2)如果反应中,如果有17.4 g纯MnO2被还原,那么被氧化的氯化氢的质量为
您最近一年使用:0次

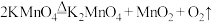 ,其中被氧化的元素是
,其中被氧化的元素是 共热,发生反应
共热,发生反应 ,该反应中氧化剂与还原剂的个数之比为
,该反应中氧化剂与还原剂的个数之比为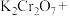


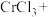

 ,若反应中发生氧化反应的
,若反应中发生氧化反应的 个数为12,则反应中转移的电子数为
个数为12,则反应中转移的电子数为

