高铁酸钾(K2FeO4)是一种高效多功能水处理剂。实验室模拟工业生产K2FeO4的流程如下:

(1) K2FeO4既能杀菌消毒,又能沉降水中悬浮物,其原因是:_________________________________________ 。
(2)无隔膜法电解饱和NaCl溶液制备NaClO总反应的离子方程式为:__________________ 。
(3)“氧化”时发生反应的化学方程式为:_________________________________________ 。Na2FeO4、FeCl3、NaClO氧化性由强到弱的顺序为_________________________________ 。
(4)“过滤”所得滤液中,除OH-外,一定存在的阴离子为_____________________ (填离子符号)。
(5) 试从沉淀溶解平衡的角度解释“转化”得以顺利实现的原因___________________________ 。

(1) K2FeO4既能杀菌消毒,又能沉降水中悬浮物,其原因是:
(2)无隔膜法电解饱和NaCl溶液制备NaClO总反应的离子方程式为:
(3)“氧化”时发生反应的化学方程式为:
(4)“过滤”所得滤液中,除OH-外,一定存在的阴离子为
(5) 试从沉淀溶解平衡的角度解释“转化”得以顺利实现的原因
更新时间:2018-12-20 12:36:25
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】氧化还原反应原理在生产、生活中应用广泛。
(1)下列反应中不涉及氧化还原反应的是___________ (填序号)。
a.蜡炬成灰 b.水滴石穿 c.食物腐败
(2)某同学写出以下化学反应方程式(未配平):① ,②
,② ,③
,③ ,在3个反应中一定不可能实现的是
,在3个反应中一定不可能实现的是___________ (填序号)。
(3) 可用于污水的杀菌和饮用水的净化。
可用于污水的杀菌和饮用水的净化。 与
与 在强酸性溶液中反应可制得
在强酸性溶液中反应可制得 ,
, 被氧化为
被氧化为 ,此反应的离子方程式为
,此反应的离子方程式为___________ 。
(4)亚硝酸钠( )是一种用途广泛的工业盐,因其外观和食盐相似容易误食中毒,误食
)是一种用途广泛的工业盐,因其外观和食盐相似容易误食中毒,误食 会导致人体血红蛋白中的
会导致人体血红蛋白中的 转化为
转化为 而中毒,该过程中
而中毒,该过程中 表现出的性质与下列(填序号)反应中
表现出的性质与下列(填序号)反应中 表现出的性质相同___________(填序号)。
表现出的性质相同___________(填序号)。
(5)已知亚硝酸钠( )可以与氯化铵(
)可以与氯化铵( )反应生成氮气、氯化钠及其它产物,写出该反应的化学反应方程式
)反应生成氮气、氯化钠及其它产物,写出该反应的化学反应方程式___________ 。
(6)一定条件下,当溶液中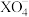 与
与 物质的量比恰好为2∶5时,溶液中
物质的量比恰好为2∶5时,溶液中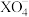 离子被还原为较低价态,则X元素的化合价变为
离子被还原为较低价态,则X元素的化合价变为___________ 。
(1)下列反应中不涉及氧化还原反应的是
a.蜡炬成灰 b.水滴石穿 c.食物腐败
(2)某同学写出以下化学反应方程式(未配平):①
 ,②
,② ,③
,③ ,在3个反应中一定不可能实现的是
,在3个反应中一定不可能实现的是(3)
 可用于污水的杀菌和饮用水的净化。
可用于污水的杀菌和饮用水的净化。 与
与 在强酸性溶液中反应可制得
在强酸性溶液中反应可制得 ,
, 被氧化为
被氧化为 ,此反应的离子方程式为
,此反应的离子方程式为(4)亚硝酸钠(
 )是一种用途广泛的工业盐,因其外观和食盐相似容易误食中毒,误食
)是一种用途广泛的工业盐,因其外观和食盐相似容易误食中毒,误食 会导致人体血红蛋白中的
会导致人体血红蛋白中的 转化为
转化为 而中毒,该过程中
而中毒,该过程中 表现出的性质与下列(填序号)反应中
表现出的性质与下列(填序号)反应中 表现出的性质相同___________(填序号)。
表现出的性质相同___________(填序号)。A. |
B. |
C. |
D. |
 )可以与氯化铵(
)可以与氯化铵( )反应生成氮气、氯化钠及其它产物,写出该反应的化学反应方程式
)反应生成氮气、氯化钠及其它产物,写出该反应的化学反应方程式(6)一定条件下,当溶液中
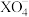 与
与 物质的量比恰好为2∶5时,溶液中
物质的量比恰好为2∶5时,溶液中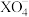 离子被还原为较低价态,则X元素的化合价变为
离子被还原为较低价态,则X元素的化合价变为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】已知:废液中含+6 价铬的化合物毒性较大污染性强,常用 NaHSO3 将废液中的Cr2O72-还原成 Cr3+。请配平该反应的离子方程式:_____ Cr2O72-+_____ HSO3-+____ H+ = ____ Cr3++_____ SO42-+_____ H2O
并用双线桥标出电子转移的方向和数目____________________ 。
并用双线桥标出电子转移的方向和数目
您最近一年使用:0次
【推荐3】氧化还原反应在高中化学中是一类重要的反应类型。 、
、 、
、 、
、 是中学化学中常用的氧化剂。回答下列问题:
是中学化学中常用的氧化剂。回答下列问题:
(1)下列基本反应类型中一定属于氧化还原反应的是_______(填字母)。
(2)实验室迅速制备少量氯气可利用如下反应: (未配平)。
(未配平)。 与
与 反应生成
反应生成 ,反应后
,反应后 转化为
转化为_______ , 发生反应
发生反应_______ (填“氧化”或“还原”)。
(3) 溶液能与Cu反应制作印刷电路板,其制作原理可用
溶液能与Cu反应制作印刷电路板,其制作原理可用 表示。
表示。
①上式中X的化学式为_______ 。
②若有32g铜参与反应,则参与反应的 的质量为
的质量为_______ g。
③该反应的离子方程式为_______ 。
(4)已知方程式: 。用双线桥法标出电子转移的方向和数目
。用双线桥法标出电子转移的方向和数目_______ 。
(5)某反应的反应物与生成物有 、KCl、
、KCl、 、
、 、HCl、
、HCl、 ,已知氧化性:
,已知氧化性: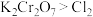 ,写出并配平该化学方程式:
,写出并配平该化学方程式:_______ 。
 、
、 、
、 、
、 是中学化学中常用的氧化剂。回答下列问题:
是中学化学中常用的氧化剂。回答下列问题:(1)下列基本反应类型中一定属于氧化还原反应的是_______(填字母)。
| A.化合反应 | B.分解反应 | C.置换反应 | D.复分解反应 |
 (未配平)。
(未配平)。 与
与 反应生成
反应生成 ,反应后
,反应后 转化为
转化为 发生反应
发生反应(3)
 溶液能与Cu反应制作印刷电路板,其制作原理可用
溶液能与Cu反应制作印刷电路板,其制作原理可用 表示。
表示。①上式中X的化学式为
②若有32g铜参与反应,则参与反应的
 的质量为
的质量为③该反应的离子方程式为
(4)已知方程式:
 。用双线桥法标出电子转移的方向和数目
。用双线桥法标出电子转移的方向和数目(5)某反应的反应物与生成物有
 、KCl、
、KCl、 、
、 、HCl、
、HCl、 ,已知氧化性:
,已知氧化性: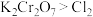 ,写出并配平该化学方程式:
,写出并配平该化学方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】高铁酸盐( )具有优异的氧化漂白、优良的杀菌消毒作用。
)具有优异的氧化漂白、优良的杀菌消毒作用。
(1)已知铁是26号元素,则1mol 中含有电子的物质的量为
中含有电子的物质的量为_______ mol,Na2FeO4是否具有还原性?_______ (填“有”或“没有”),原因是:________________________ 。
(2)制备高铁酸钠可以将Fe(OH)3在碱性条件下与NaClO溶液反应,该反应离子方程式为:________________________________ 。
(3)Na2FeO4作为高效的净水剂和杀菌消毒剂,在净水过程中 可变为Fe(OH)3胶体而吸附杂质,Fe(OH)3胶体粒子的直径大小范围是
可变为Fe(OH)3胶体而吸附杂质,Fe(OH)3胶体粒子的直径大小范围是_______ 。
(4)向1L 0.3mol/L的Na2FeO4溶液中加入足量稀H2SO4酸化,可以产生O2和Fe3+,该反应的离子方程式为____________________________ 。向酸化后的溶液中加入一定量的金属铜,使Fe3+和Cu2+浓度相等,则加入铜的质量为__________________ 。
 )具有优异的氧化漂白、优良的杀菌消毒作用。
)具有优异的氧化漂白、优良的杀菌消毒作用。(1)已知铁是26号元素,则1mol
 中含有电子的物质的量为
中含有电子的物质的量为(2)制备高铁酸钠可以将Fe(OH)3在碱性条件下与NaClO溶液反应,该反应离子方程式为:
(3)Na2FeO4作为高效的净水剂和杀菌消毒剂,在净水过程中
 可变为Fe(OH)3胶体而吸附杂质,Fe(OH)3胶体粒子的直径大小范围是
可变为Fe(OH)3胶体而吸附杂质,Fe(OH)3胶体粒子的直径大小范围是(4)向1L 0.3mol/L的Na2FeO4溶液中加入足量稀H2SO4酸化,可以产生O2和Fe3+,该反应的离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】查资料得:HNO2是一种弱酸且不稳定,易分解生成NO和NO2;它能被常见的强氧化剂氧化;在酸性溶液中它也是一种氧化剂,如能把Fe2+氧化成Fe3+。AgNO2是一种难溶于水、易溶于酸的化合物。
试回答下列问题:
(1)下列方法中,不能用来区分NaNO2和NaCl的是________ (填序号)。
A.测定这两种溶液的pH
B.分别在两种溶液中滴加甲基橙
C.在酸性条件下加入KI—淀粉溶液来区别
D.用AgNO3和HNO3两种试剂来区别
(2)Fe与过量稀硫酸反应可以制取FeSO4。若用反应所得的酸性溶液,将Fe2+转化为Fe3+,要求产物纯净,可选用的最佳试剂是________ (填序号)。
A.Cl2 B.Fe C.H2O2 D.HNO3
(3)某同学把酸性高锰酸钾溶液滴入NaNO2溶液中,观察到紫色褪去,同时生成NO3-和Mn2+,请写出反应的离子方程式:_________________ 。
(4)已知FeSO4在一定条件下可转变为高铁酸钾(K2FeO4),高铁酸钾是一种新型、高效的绿色水处理剂,在水中发生反应生成氢氧化铁胶体。高铁酸钾作为水处理剂发挥的作用是____________ 。
试回答下列问题:
(1)下列方法中,不能用来区分NaNO2和NaCl的是
A.测定这两种溶液的pH
B.分别在两种溶液中滴加甲基橙
C.在酸性条件下加入KI—淀粉溶液来区别
D.用AgNO3和HNO3两种试剂来区别
(2)Fe与过量稀硫酸反应可以制取FeSO4。若用反应所得的酸性溶液,将Fe2+转化为Fe3+,要求产物纯净,可选用的最佳试剂是
A.Cl2 B.Fe C.H2O2 D.HNO3
(3)某同学把酸性高锰酸钾溶液滴入NaNO2溶液中,观察到紫色褪去,同时生成NO3-和Mn2+,请写出反应的离子方程式:
(4)已知FeSO4在一定条件下可转变为高铁酸钾(K2FeO4),高铁酸钾是一种新型、高效的绿色水处理剂,在水中发生反应生成氢氧化铁胶体。高铁酸钾作为水处理剂发挥的作用是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】高铁酸钾(K2FeO4)是一种新型绿色消毒剂,其在消毒(发生氧化还原反应)后可形成Fe(OH)3胶体,常用于处理饮用水。工业上有干法与湿法两种制备高铁酸钾的方法。
(1)干法制备高铁酸钾时,先制备得到Na2FeO4,反应为:2FeSO4+6Na2O2=2Na2FeO4+2Na2O+2Na2SO4+O2↑
①该反应中,氧化剂是________ ,氧化产物是________ 。
②每生成1 mol Na2FeO4,转移________ mol电子。
(2)配平湿法制备高铁酸钾反应的离子方程式:______ Fe(OH)3+______ ClO-+______ OH-=______ FeO42-+______ Cl-+______ H2O
(3)取少量K2FeO4溶液,滴加盐酸,有Cl2产生,该反应表明氧化性:K2FeO4______ (填“>”或“<”)Cl2。
(4)Fe(OH)3胶体可使水中悬浮物沉降下来,用作净水剂。实验室用饱和氯化铁溶液制取Fe(OH)3胶体的化学方程式是_____________________ 。
(1)干法制备高铁酸钾时,先制备得到Na2FeO4,反应为:2FeSO4+6Na2O2=2Na2FeO4+2Na2O+2Na2SO4+O2↑
①该反应中,氧化剂是
②每生成1 mol Na2FeO4,转移
(2)配平湿法制备高铁酸钾反应的离子方程式:
(3)取少量K2FeO4溶液,滴加盐酸,有Cl2产生,该反应表明氧化性:K2FeO4
(4)Fe(OH)3胶体可使水中悬浮物沉降下来,用作净水剂。实验室用饱和氯化铁溶液制取Fe(OH)3胶体的化学方程式是
您最近一年使用:0次
【推荐1】完成下列填空
| 序号 | 实验 | 现象 | 解释与结论 | 正误 |
| 1 | 用洁净铂丝蘸取溶液进行焰色反应 | 火焰呈黄色 | 原溶液中有 无 无 | |
| 2 | 滴加几滴稀 溶液,将湿润红色石蕊试纸置于试管口 溶液,将湿润红色石蕊试纸置于试管口 | 试纸不变蓝 | 原溶液中无 | |
| 3 | 用坩埚钳夹住一小块用砂纸仔细打磨过的铝箔在酒精灯上加热 | 熔化后的液态铝滴落下来 | 金属铝的熔点较低 | |
| 4 | 硝酸银溶液中加入足量 溶液,再加入 溶液,再加入 溶液 溶液 | 先出现白色沉淀,后变为黄色沉淀 | 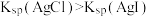 | |
| 5 |  溶液中加4~6滴 溶液中加4~6滴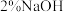 溶液,振荡后加入 溶液,振荡后加入 溶液,加热煮沸 溶液,加热煮沸 | 未出现红色沉淀 | X不含有醛基 | |
| 6 | 等体积 的 的 和 和 两种酸分别与足量的锌反应 两种酸分别与足量的锌反应 | 相同时间内, 收集到的氢气多 收集到的氢气多 |  是强酸 是强酸 | |
| 7 | 将铝片和镁条作为电极,插入 的 的 溶液中 溶液中 | 电流表指针偏向镁片 | 金属铝比镁活泼 | |
| 8 | 向 的 的 溶液中滴加2滴甲基橙 溶液中滴加2滴甲基橙 | 溶液呈黄色 |  溶液呈碱性 溶液呈碱性 | |
| 9 | 向 溶液中加入氯水,再加入淀粉 溶液中加入氯水,再加入淀粉 溶液 溶液 | 溶液变蓝 | 氧化性: | |
| 10 | 将浓硫酸滴到蔗糖表面 | 固体变黑膨胀 | 浓硫酸有脱水性和强氧化性 | |
| 11 | 配制 溶液 溶液 | 将 固体溶解于适量硫酸溶液 固体溶解于适量硫酸溶液 |  抑制 抑制 水解 水解 | |
| 12 | 常温下,相同的铝片分别投入足量的稀、浓硫酸中 | 浓硫酸中铝片先溶解完 | 反应物浓度越大,反应速率越快 | |
| 13 | 向 溶液中通入 溶液中通入 体 体 | 有黑色沉淀 |  不溶于稀硫酸 不溶于稀硫酸 | |
| 14 | 在 溶液中加入 溶液中加入 溶液,再加入苯,振荡 溶液,再加入苯,振荡 | 有白色沉淀生成,苯层呈紫色 | 白色沉淀可能为 | |
| 15 | 向硝酸亚铁溶液中滴入稀硫酸 | 无明显现象 | 硝酸亚铁与硫酸不反应 | |
| 16 | 常温下,用 试纸测定一定浓度的 试纸测定一定浓度的 溶液的 溶液的 | 比对后,测得 |  的水解程度小于其电离程度 的水解程度小于其电离程度 | |
| 17 | 向一定量的浓硫酸中加入过量的锌粒,微热至反应结束 | 产生气泡 | 该气体成分仅为 | |
| 18 | 将澄清石灰水滴入可能混有 的 的 溶液中 溶液中 | 有白色沉淀产生 | 该溶液中一定含有 | |
| 19 | 表面变黑的银器浸泡到盛有食盐水的铝制容器中,银器与铝接触 | 银器变得光亮如新 | 构成原电池,铝作负极,硫化银得电子被还原成单质银 | |
| 20 | 向足量的浓硝酸中加入铁片,一段时间后加入铜粉 | 有气体生成,溶液呈蓝绿色 | 浓硝酸将 氧化成 氧化成 ,生成 ,生成 , , 与 与 反应生成 反应生成 |
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】天然水加热时产生水垢.天然水中含 与
与 ,
, 热分解产物有
热分解产物有 、
、 。回答下列问题:
。回答下列问题:
(1)加热 的化学方程式为
的化学方程式为_______ ;持续加热, 沉淀可转换为
沉淀可转换为 ,说明
,说明_______ 更难溶。
(2)浓缩海水得粗盐水中主要含有 、
、 、
、 等离子.粗盐水精制食盐过程中,按除杂顺序写出除杂试剂的化学式为
等离子.粗盐水精制食盐过程中,按除杂顺序写出除杂试剂的化学式为_______ 、_______ 、_______ ,过滤取滤液,加过量盐酸酸化后,蒸发结晶纯化。
(3)工业上通常用 除去天然水中
除去天然水中 ,已知某天然水中
,已知某天然水中 开始沉淀的
开始沉淀的 为9.6,则溶液中
为9.6,则溶液中 的初始浓度是
的初始浓度是_______ 。
(4)工业上制备轻质氧化镁流程如下.轻质氧化镁相比重质氧化镁质量更轻,更加疏松多孔。

①水解过程加热的作用是_______ ;
②不用重质 而用轻质
而用轻质 酸溶制备
酸溶制备 的原因是
的原因是_______ 。
 与
与 ,
, 热分解产物有
热分解产物有 、
、 。回答下列问题:
。回答下列问题:(1)加热
 的化学方程式为
的化学方程式为 沉淀可转换为
沉淀可转换为 ,说明
,说明(2)浓缩海水得粗盐水中主要含有
 、
、 、
、 等离子.粗盐水精制食盐过程中,按除杂顺序写出除杂试剂的化学式为
等离子.粗盐水精制食盐过程中,按除杂顺序写出除杂试剂的化学式为(3)工业上通常用
 除去天然水中
除去天然水中 ,已知某天然水中
,已知某天然水中 开始沉淀的
开始沉淀的 为9.6,则溶液中
为9.6,则溶液中 的初始浓度是
的初始浓度是
(4)工业上制备轻质氧化镁流程如下.轻质氧化镁相比重质氧化镁质量更轻,更加疏松多孔。

①水解过程加热的作用是
②不用重质
 而用轻质
而用轻质 酸溶制备
酸溶制备 的原因是
的原因是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】电解质在水溶液中可能存在电离平衡、水解平衡、溶解平衡等。
(1)已知部分弱酸的电离常数如下表:
①室温下,一定浓度的HCOONa溶液 ,用离子方程式表示溶液呈碱性的原因
,用离子方程式表示溶液呈碱性的原因___________ 。
②0.1 mol·L-1 NaCN溶液和0.1 mol·L-1 溶液中,
溶液中,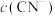
___________  (填“>”、“<”或“=”)。
(填“>”、“<”或“=”)。
③将 通入NaCN溶液,反应的离子方程式是
通入NaCN溶液,反应的离子方程式是___________ 。
(2)常温时,向20 mL 0.1 mol/L 水溶液中逐滴滴加0.1 mol/L NaOH溶液,混合溶液中
水溶液中逐滴滴加0.1 mol/L NaOH溶液,混合溶液中 、
、 和
和 的物质的量分数(δ)随pH变化的关系如图所示。
的物质的量分数(δ)随pH变化的关系如图所示。

则曲线Ⅱ表示___________ 微粒,弱酸 的
的
___________
(3)已知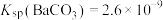 ,
,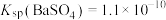 。
。
①将浓度为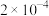 mol⋅L-1
mol⋅L-1  溶液与
溶液与 溶液
溶液等体积混合 ,则生成 沉淀所需
沉淀所需 溶液的最小浓度为
溶液的最小浓度为___________ mol⋅L-1。
②向含有 固体的溶液中滴加
固体的溶液中滴加 溶液,当有
溶液,当有 沉淀生成时,溶液中,写出沉淀转化的离子方程式
沉淀生成时,溶液中,写出沉淀转化的离子方程式___________ ,求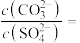
___________ (保留三位有效数字)。
(1)已知部分弱酸的电离常数如下表:
| 弱酸 | HCOOH | HCN |  |
| 电离常数(25℃) | 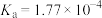 | 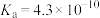 | 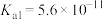 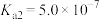 |
 ,用离子方程式表示溶液呈碱性的原因
,用离子方程式表示溶液呈碱性的原因②0.1 mol·L-1 NaCN溶液和0.1 mol·L-1
 溶液中,
溶液中,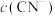
 (填“>”、“<”或“=”)。
(填“>”、“<”或“=”)。③将
 通入NaCN溶液,反应的离子方程式是
通入NaCN溶液,反应的离子方程式是(2)常温时,向20 mL 0.1 mol/L
 水溶液中逐滴滴加0.1 mol/L NaOH溶液,混合溶液中
水溶液中逐滴滴加0.1 mol/L NaOH溶液,混合溶液中 、
、 和
和 的物质的量分数(δ)随pH变化的关系如图所示。
的物质的量分数(δ)随pH变化的关系如图所示。
则曲线Ⅱ表示
 的
的
(3)已知
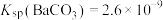 ,
,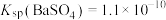 。
。①将浓度为
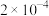 mol⋅L-1
mol⋅L-1  溶液与
溶液与 溶液
溶液 沉淀所需
沉淀所需 溶液的最小浓度为
溶液的最小浓度为②向含有
 固体的溶液中滴加
固体的溶液中滴加 溶液,当有
溶液,当有 沉淀生成时,溶液中,写出沉淀转化的离子方程式
沉淀生成时,溶液中,写出沉淀转化的离子方程式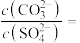
您最近一年使用:0次



