下图是一些常见的单质、化合物之间的转化关系图,有些反应中的部分物质被略去。常温常压下,A为无色有毒气体,B为红棕色粉末,C、E为金属单质。反应①②均为工业上的重要反应。
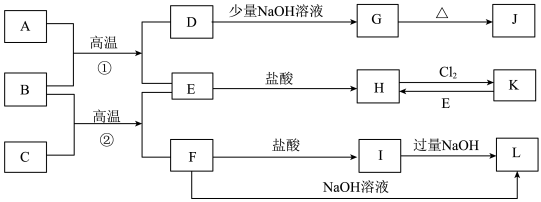
请回答下列问题:
(1)写出下列物质的化学式:D___________ ;K____________ ;L______________ 。
(2)写出B与C高温反应生成E和F的化学方程式:_______________________ 。
(3)写出D与J的稀溶液反应生成G的离子方程式:______________________ 。
(4)写出H转化为K的离子方程式:______________________ 。

请回答下列问题:
(1)写出下列物质的化学式:D
(2)写出B与C高温反应生成E和F的化学方程式:
(3)写出D与J的稀溶液反应生成G的离子方程式:
(4)写出H转化为K的离子方程式:
更新时间:2018-12-27 15:18:48
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】氯化亚铜(CuCl)是一种应用较广的催化剂,有关物质的转化关系如下图所示(除B、E外,均为对应物质的溶液参加反应,部分生成物和反应条件已略去)。其中B 为气体,能使品红溶液褪色; C 为正盐,D 为重要的调味剂,E 为一种红色的金属氧化物,M 的摩尔质量为34g•mol-1,它的水溶液常作医用消毒液。
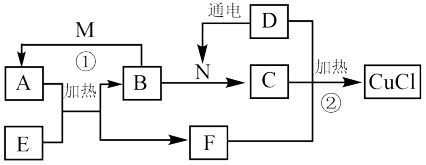
(1)E的化学式________________________ 。
(2)N的电子式为________________________ 。
(3)写出反应①的化学方程式:_________________________________________ 。
(4)写出反应②的离子方程式:_________________________________________ 。

(1)E的化学式
(2)N的电子式为
(3)写出反应①的化学方程式:
(4)写出反应②的离子方程式:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐2】A、B、C、D、E、X是中学常见的无机物,存在如图转化关系(部分生成物和反应条件略去)。
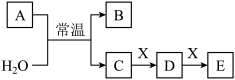
(1)若A为常见的金属单质,焰色反应呈黄色,X能使品红溶液褪色,写出C和E反应的离子方程式:________ 。证明D已经氧化变质的方法是:取少量D固体溶于水中,_______ 。
(2)若A为短周期元素组成单质,该元素的最高价氧化物的水化物酸性最强,则X可能为______ (填代号)。
a.NaHCO3 b.Na2CO3 c.Fe(OH)3 d.NaAlO2
(3)若A为淡黄色粉末,则A的电子式为______ 。若X为一种最常见的造成温室效应的气体。若鉴别等浓度的D、E两种溶液,可选择的试剂为_____ (填代号)。
a.盐酸 b.BaCl2溶液 c.NaOH溶液 d.Ca(OH)2溶液
(4)若A为氧化物,X是Fe,溶液D中加入KSCN溶液变红。则A与H2O反应的化学反应方程式为_____ ,E是_____ (填化学式)。

(1)若A为常见的金属单质,焰色反应呈黄色,X能使品红溶液褪色,写出C和E反应的离子方程式:
(2)若A为短周期元素组成单质,该元素的最高价氧化物的水化物酸性最强,则X可能为
a.NaHCO3 b.Na2CO3 c.Fe(OH)3 d.NaAlO2
(3)若A为淡黄色粉末,则A的电子式为
a.盐酸 b.BaCl2溶液 c.NaOH溶液 d.Ca(OH)2溶液
(4)若A为氧化物,X是Fe,溶液D中加入KSCN溶液变红。则A与H2O反应的化学反应方程式为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐1】用下图所示实验(部分装置)收集氯气并验证氯气的性质:
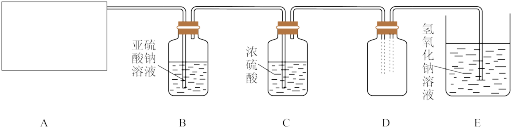
(1)A为Cl2的发生装置。实验室通常制取氯气的化学方程式为_______ ,且与之对应的A装置是_______ (从下面a、b、c序号中选择回答)。
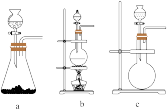
(2)利用D中的广口瓶收集氯气,试在装置图中完善D装置(将虚线表示的一根或两根导管改为实线,也可都不改)_______ (用文字回答)
(3)写出装置E中反应的离子方程式_______
(4)利用D中收集的氯气进行铁与氯气的反应实验:用坩埚钳夹持一束细铁丝,_______ ,然后伸入盛有氯气的集气瓶中。
(5)通入氯气一段时间后,洗气瓶B溶液中有一部分SO 氧化成SO
氧化成SO ,反应的离子方程式为
,反应的离子方程式为_______ 。设计实验检验洗气瓶B溶液中最终有Cl- 和SO 存在,将选择的试剂的序号填写在下表空格中
存在,将选择的试剂的序号填写在下表空格中
①稀盐酸 ②稀硝酸(有强氧化性) ③BaCl2溶液 Ba(NO3)2溶液 ⑤AgNO3溶液 ⑥澄清石灰水
若上述实验需要100mL、2mol/L的盐酸溶液,配制时应用量筒量取36.5%、密度1.19g/mL的浓盐酸_______ mL。

(1)A为Cl2的发生装置。实验室通常制取氯气的化学方程式为

(2)利用D中的广口瓶收集氯气,试在装置图中完善D装置(将虚线表示的一根或两根导管改为实线,也可都不改)
(3)写出装置E中反应的离子方程式
(4)利用D中收集的氯气进行铁与氯气的反应实验:用坩埚钳夹持一束细铁丝,
(5)通入氯气一段时间后,洗气瓶B溶液中有一部分SO
 氧化成SO
氧化成SO ,反应的离子方程式为
,反应的离子方程式为 存在,将选择的试剂的序号填写在下表空格中
存在,将选择的试剂的序号填写在下表空格中①稀盐酸 ②稀硝酸(有强氧化性) ③BaCl2溶液 Ba(NO3)2溶液 ⑤AgNO3溶液 ⑥澄清石灰水
| 实 验 步 骤 | 预 期 现 象 和 结 论 |
| 步骤1:取适量洗气瓶B中溶液于试管Ⅰ中,滴加 | 若产生的白色沉淀,则洗气瓶B溶液中存在SO 。 。 |
| 步骤2:另取适量洗气瓶B中溶液于试管Ⅱ中,滴加过量Ba(NO3)2溶液振荡,静置。 | 产生白色沉淀。 |
| 步骤3:取步骤2后试管Ⅱ中的上层清液于试管Ⅲ中,滴加 | 若产生白色沉淀,则洗气瓶B溶液中存在Cl- |
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐2】“84消毒液”是生活中常用的消毒剂,可与硫酸溶液反应制取氯气,反应原理为:NaClO+NaCl+H2SO4 Na2SO4 + Cl2↑ + H2O;为探究氯气的性质,某同学利用此原理制氯气并设计了如下所示的实验装置:
Na2SO4 + Cl2↑ + H2O;为探究氯气的性质,某同学利用此原理制氯气并设计了如下所示的实验装置:

(1)从①、②、③装置中选择合适的制氯气装置(A 处)_____________ (填写序号)。

(2)装置 B、C 中依次放的是干燥的红色布条和湿润的红色布条,实验过程中该同学发现装置 B 中的布条也褪色,其原因可能是____________________________________ ;说明该装置存在明显的缺陷,为解决上述问题,请提出合理的改进的方法 _________________________________________________________ 。
(3)氯气通到FeCl2 溶液中发生反应的离子方程式:_________________ 。
(4)氯气通到饱和NaHCO3溶液能产生无色气体,已知酸性:盐酸 > 碳酸 > 次氯酸, 该实验证明氯气与水反应的生成物中含有_______________ (填“盐酸”或“次氯酸”)。
(5)该同学运用了哪些方法探究氯气的性质______________ 。
A.分类法 B.观察法 C.对比法 D.定量研究法 E.实验探究法
 Na2SO4 + Cl2↑ + H2O;为探究氯气的性质,某同学利用此原理制氯气并设计了如下所示的实验装置:
Na2SO4 + Cl2↑ + H2O;为探究氯气的性质,某同学利用此原理制氯气并设计了如下所示的实验装置:
(1)从①、②、③装置中选择合适的制氯气装置(A 处)

(2)装置 B、C 中依次放的是干燥的红色布条和湿润的红色布条,实验过程中该同学发现装置 B 中的布条也褪色,其原因可能是
(3)氯气通到FeCl2 溶液中发生反应的离子方程式:
(4)氯气通到饱和NaHCO3溶液能产生无色气体,已知酸性:盐酸 > 碳酸 > 次氯酸, 该实验证明氯气与水反应的生成物中含有
(5)该同学运用了哪些方法探究氯气的性质
A.分类法 B.观察法 C.对比法 D.定量研究法 E.实验探究法
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐1】我国化学家侯德榜发明的“联合制碱法”为世界制碱工业做出了巨大贡献。
Ⅰ.如图为联合制碱法的主要过程(部分物质已略去):
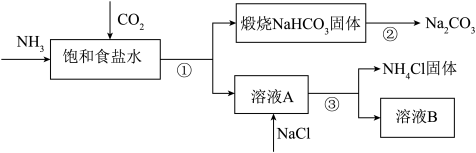
(1)①~③的涉及的操作方法中,包含过滤的是_______ (填序号)。
(2)根据上述流程图,将化学方程式补充完整:_______ 。NH3+CO2+______+______=NaHCO3+NH4Cl。
(3)煅烧NaHCO3固体的化学方程式是_______ 。
(4)上述联合制碱法流程可以循环使用的中一种物质是______ (填化学式)。
Ⅱ.某小组利用下列装置对Na2CO3和NaHCO3的性质进行探究,(夹持装置已略去,气密性已检查)。

(5)方框中为洗气装置,请将该装置图补充完整_____________ 。
(6)试剂a为饱和NaHCO3溶液,其作用是_____________ 。
(7)实验持续-段时间后,观察到饱和Na2CO3溶液中有细小晶体析出,用化学方程式表示产生细小晶体的原因_________________ 。
Ⅰ.如图为联合制碱法的主要过程(部分物质已略去):

(1)①~③的涉及的操作方法中,包含过滤的是
(2)根据上述流程图,将化学方程式补充完整:
(3)煅烧NaHCO3固体的化学方程式是
(4)上述联合制碱法流程可以循环使用的中一种物质是
Ⅱ.某小组利用下列装置对Na2CO3和NaHCO3的性质进行探究,(夹持装置已略去,气密性已检查)。

(5)方框中为洗气装置,请将该装置图补充完整
(6)试剂a为饱和NaHCO3溶液,其作用是
(7)实验持续-段时间后,观察到饱和Na2CO3溶液中有细小晶体析出,用化学方程式表示产生细小晶体的原因
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐2】下列各物质中只有A、B、C三种单质,A的焰色反应为黄色,主要以G形式存在于海水中,F是一种淡黄色的固体,H是一种常见的无色液体,I是造成温室效应的“元凶”,各物质间的转化关系图如下:

请按要求书写:
(1)反应①的离子方程式:____________________________________ ;
(2)物质K与物质L等物质的量离子方程式:___________________________ ;
(3)物质F转化为D的离子方程式:___________________________________ ;
(4)物质G向物质J转化的化学方程式:_______________________________ ;

请按要求书写:
(1)反应①的离子方程式:
(2)物质K与物质L等物质的量离子方程式:
(3)物质F转化为D的离子方程式:
(4)物质G向物质J转化的化学方程式:
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】有些挂面在压制过程中会加入少量叫食用碱的碳酸钠。
(一)工业上常采用侯氏制碱法制取碳酸钠,实验装置如图所示(夹持装置省略)。回答:

(1)实验时,先从__________ 管通入__________ 。
(2)有同学建议在b管下端连接多孔球泡装置,理由是__________ 。
(二)碳酸钠样品中往往含有少量的 ,某学习小组设计质量差分析法测定样品中
,某学习小组设计质量差分析法测定样品中 的质量分数。
的质量分数。
(3)将一定质量的样品与足量的稀硫酸反应,采用如下图所示装置,通过称量反应前后盛有碱石灰的干燥管C的质量,利用其质量差计算样品的纯度。

①按照实验顺序排列下列操作步骤__________ gdfch。(某些步骤可以重复)
a.检查装置的气密性 b.打开止水夹 c.缓慢鼓入空气数分钟
d.干燥管C内碱石灰质量为 g e.取
g e.取 g样品装入广口瓶中
g样品装入广口瓶中
f.缓慢加入稀硫酸至不再产生气体为止 g.关闭止水夹
h.称量干燥管C质量为 g(
g( )
)
②在操作h前,要缓慢鼓入空气数分钟,鼓入空气的作用是_________ ,装置A的作用是_________ 。
③若去掉装置D,对实验结果的影响是________ (读“偏大”,“偏小”或“无影响”),样品中 的质量分数
的质量分数_______
(一)工业上常采用侯氏制碱法制取碳酸钠,实验装置如图所示(夹持装置省略)。回答:

(1)实验时,先从
(2)有同学建议在b管下端连接多孔球泡装置,理由是
(二)碳酸钠样品中往往含有少量的
 ,某学习小组设计质量差分析法测定样品中
,某学习小组设计质量差分析法测定样品中 的质量分数。
的质量分数。(3)将一定质量的样品与足量的稀硫酸反应,采用如下图所示装置,通过称量反应前后盛有碱石灰的干燥管C的质量,利用其质量差计算样品的纯度。

①按照实验顺序排列下列操作步骤
a.检查装置的气密性 b.打开止水夹 c.缓慢鼓入空气数分钟
d.干燥管C内碱石灰质量为
 g e.取
g e.取 g样品装入广口瓶中
g样品装入广口瓶中f.缓慢加入稀硫酸至不再产生气体为止 g.关闭止水夹
h.称量干燥管C质量为
 g(
g( )
)②在操作h前,要缓慢鼓入空气数分钟,鼓入空气的作用是
③若去掉装置D,对实验结果的影响是
 的质量分数
的质量分数
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】A~I分别表示中学化学中常见的一种物质,它们之间的相互关系如图所示(部分反应物、生成物没有列出)。已知H为两性氧化物,F是红褐色难溶于水的沉淀,且A、B、C、D、E、F六种物质中均合同一种元素。

请填写下列空白:
(1)六种物质A、B、C、D、E、F中所含的同一种元素的名称是____________ 。
(2)写出C、H的化学式:C___ ,H______ 。
(3)写出反应①、⑦的化学方程式:反应①_______________ ,反应⑦________________ 。
(4)反应⑥过程中出现的现象是_______________ 。

请填写下列空白:
(1)六种物质A、B、C、D、E、F中所含的同一种元素的名称是
(2)写出C、H的化学式:C
(3)写出反应①、⑦的化学方程式:反应①
(4)反应⑥过程中出现的现象是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】I.天宫二号空间实验室已于2016年9月15日22时04分在酒泉卫星发射中心发射成功。请回答下列问题:
(1)耐辐照石英玻璃是航天器姿态控制系统的核心元件。石英玻璃的成分是___________ (填化学式),该物质的类别属于_______ (填“碱性氧化物”或“酸性氧化物”),实验室中不能用玻璃塞的试剂瓶盛放KOH溶液,原因是___________________ (用离子方程式表示)。
(2)太阳能电池帆板是“天宫二号”空间运行的动力。其性能直接影响到“天宫二号”的运行寿命和可靠性。天宫二号使用的光太阳能电池,该电池的核心材料是_______ ,其能量转化方式为____________________ 。
II.铝和氢氧化钾都是重要的工业产品。
请回答:
(1)铝与氢氧化钾溶液反应的离子方程式是____________________ 。
(2)用铝粉和Fe2O3做铝热反应实验,需要的试剂还有____________ (填序号)。
a.KCl b.KClO3 c.MnO2 d.Mg
取少量铝热反应所得到的固体混合物,将其溶于足量稀H2SO4,滴加KSCN溶液无明显现象,________ (填“能”或“不能”)说明固体混合物中无Fe2O3,若能,则不用填写理由,若不能,理由是(用离子方程式说明)___________________ 。
(1)耐辐照石英玻璃是航天器姿态控制系统的核心元件。石英玻璃的成分是
(2)太阳能电池帆板是“天宫二号”空间运行的动力。其性能直接影响到“天宫二号”的运行寿命和可靠性。天宫二号使用的光太阳能电池,该电池的核心材料是
II.铝和氢氧化钾都是重要的工业产品。
请回答:
(1)铝与氢氧化钾溶液反应的离子方程式是
(2)用铝粉和Fe2O3做铝热反应实验,需要的试剂还有
a.KCl b.KClO3 c.MnO2 d.Mg
取少量铝热反应所得到的固体混合物,将其溶于足量稀H2SO4,滴加KSCN溶液无明显现象,
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】已知A-F是中学化学常见的物质,其中A、C、E为气体,B、D为液体,D是一种不挥发性酸,其浓溶液有强氧化性,F的溶液与X共热通常用于实验室制备单质C,X是一种黑色粉末,B分子中有18个电子,实验室常用B和X制备单质E。反应中部分生成物已略去。试回答下列问题:

(1)写出B的电子式_______ ,化学键类型_______ 。
(2)根据图中信息,B.C.X氧化性从强到弱的顺序是_______ 。
(3)X与铝高温下反应的方程式为_______ 。
(4)写出反应②的化学方程式_______ 。
(5)反应①的离子方程式_______ 。

(1)写出B的电子式
(2)根据图中信息,B.C.X氧化性从强到弱的顺序是
(3)X与铝高温下反应的方程式为
(4)写出反应②的化学方程式
(5)反应①的离子方程式
您最近一年使用:0次





