一定温度下,在1L恒容密闭容器中加入lmol的N2(g)和3molH2(g)发生反应:N2(g)+3H2(g)  2NH3(g) △H<0, NH3的物质的量与时间的关系如下表所示,下列说法
2NH3(g) △H<0, NH3的物质的量与时间的关系如下表所示,下列说法不正确 的是
 2NH3(g) △H<0, NH3的物质的量与时间的关系如下表所示,下列说法
2NH3(g) △H<0, NH3的物质的量与时间的关系如下表所示,下列说法| 时间(min) | 0 | t1 | t2 | t3 |
| NH3物质的量(mol) | 0 | 0.2 | 0.3 | 0.3 |
| A.0~t1min,v(NH3)=0.2/t1mol·L-1·min-1 |
| B.t3时再加入1mol的N2(g)和3molH2(g),反应达新平衡时,c(N2)>0.85mol·L-1 |
C.N2(g)+3H2(g)  2NH3(g)的活化能小于2NH3(g) 2NH3(g)的活化能小于2NH3(g)  N2(g)+3H2(g)的活化能 N2(g)+3H2(g)的活化能 |
| D.升高温度,可使正反应速率减小,逆反应速率增大,故平衡逆移 |
2018·福建泉州·一模 查看更多[7]
更新时间:2019-01-02 08:55:56
|
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】汽车尾气系统中的催化转化器,可有效降低尾气中 、
、 等大气污染物的排放量,发生反应为
等大气污染物的排放量,发生反应为 。
。 时,向
时,向 含有固体催化剂的恒容密闭容器中充入
含有固体催化剂的恒容密闭容器中充入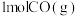 和
和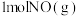 ,
, 后,测得容器中
后,测得容器中 的浓度为
的浓度为 。下列说法错误的是
。下列说法错误的是
 、
、 等大气污染物的排放量,发生反应为
等大气污染物的排放量,发生反应为 。
。 时,向
时,向 含有固体催化剂的恒容密闭容器中充入
含有固体催化剂的恒容密闭容器中充入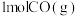 和
和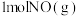 ,
, 后,测得容器中
后,测得容器中 的浓度为
的浓度为 。下列说法错误的是
。下列说法错误的是A. 内, 内,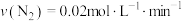 |
B.反应达到平衡状态时,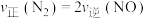 |
| C.升高温度,可以加快反应速率 |
D.反应达到平衡状态时,容器中 、 、 的浓度之比为 的浓度之比为 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】已知某条件下,合成氨反应的数据如下表。
N2+3H2 2NH3
2NH3
下列说法中错误的是
| N2 | H2 | NH3 | |
| 起始浓度/mol·L-1 | 1.0 | 3.0 | 0.2 |
| 2s末浓度/mol·L-1 | 0.6 | 1.8 | 1.0 |
| 4s末浓度/mol·L-1 | 0.4 | 1.2 | 1.4 |
 2NH3
2NH3下列说法中错误的是
| A.前4s时间内氮气的平均反应速率为0.15mol·L-1·s-1 |
| B.前2s时间内氢气的平均反应速率为0.6mol·L-1·s-1 |
| C.2s末氨气的反应速率为0.4mol·L-1·s-1 |
| D.2~4s时间内氨气的平均反应速率为0.2mol·L-1·s-1 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】合金ThNi5可催化反应CO(g)+3H2(g)=CH4(g)+H2O(g),在一定温度下,反应过程中有无催化剂的能量变化如图。下列叙述正确的是
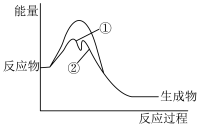

| A.使用催化剂时反应的速率主要决定于第②步 |
| B.缩小体积可加快该反应速率,是因为增大了活化分子百分数 |
| C.使用催化剂降低反应的焓变,降低温度有利于产物的生成 |
| D.升高温度,平衡常数减小 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】下列说法正确的有( )
①活化分子间的碰撞不一定能发生化学反应
②普通分子间的碰撞有时也能发生化学反应
③增大反应物的浓度,可增大单位体积内活化分子数,从而使有效碰撞次数增多
④有气体参加的化学反应,若增大压强(即缩小反应容器的容积),可增大活化分子百分数,从而使反应速率增大
⑤化学反应的实质是旧化学键断裂和新化学键形成的过程
①活化分子间的碰撞不一定能发生化学反应
②普通分子间的碰撞有时也能发生化学反应
③增大反应物的浓度,可增大单位体积内活化分子数,从而使有效碰撞次数增多
④有气体参加的化学反应,若增大压强(即缩小反应容器的容积),可增大活化分子百分数,从而使反应速率增大
⑤化学反应的实质是旧化学键断裂和新化学键形成的过程
| A.1个 | B.2个 | C.3个 | D.4个 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】为了说明影响化学反应快慢的因素,甲、乙、丙、丁四位学生分别设计了如下A~D四个实验,你认为结论不正确的是
| A.在相同条件下,等质量的大理石块和大理石粉与相同的盐酸反应,大理石粉反应快 |
| B.将大小、形状相同的镁条和铝条与相同浓度的盐酸反应时,两者速率一样大 |
| C.向两支试管中分别加入2mL5%H2O2溶液和2mL10%的H2O2溶液,再向其中各加入相同质量的二氧化锰,产生氧气的快慢不同 |
| D.两支试管中分别加入2mL0.1mol/LNa2S2O3溶液与2mL0.1mol/L稀硫酸的混合溶液,其中一支试管放入冷水中,另一支试管放入热水中,产生浑浊的快慢不同 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】在一定条件下的密闭容器中,进行反应:2SO2 (g) + O2(g)  2SO3 (g)。下列有关说法正确的是
2SO3 (g)。下列有关说法正确的是
 2SO3 (g)。下列有关说法正确的是
2SO3 (g)。下列有关说法正确的是| A.催化剂的使用可实现SO2的转化率为100% |
| B.其他条件不变,升高温度,不能增大反应的速率 |
| C.达到化学平衡时,各物质的浓度不再改变 |
| D.其他条件不变,降低SO3的浓度,可以增大反应的速率 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】一定温度下在恒容密闭容器中,进行反应:A(s)+2B(g) 2C(g) ΔH<0。下列说法正确的是
2C(g) ΔH<0。下列说法正确的是
 2C(g) ΔH<0。下列说法正确的是
2C(g) ΔH<0。下列说法正确的是| A.达到平衡后,从容器中移走部分反应物A,则正反应速率将下降 |
| B.当混合气体的密度不再发生变化时,说明反应达到平衡状态 |
| C.改变反应前A与B的投料比,ΔH将发生相应的改变 |
| D.向反应体系中继续通入足量B气体,A有可能反应完全 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】下列说法正确的是( )
| A.同温同压下H2(g)+Cl2(g)===2HCl(g)在光照和点燃条件的ΔH都相同 |
| B.已知2H2(g)+O2(g)===2H2O(g) ΔH=-483.6 kJ/mol,则氢气的燃烧热为-241.8kJ/mol |
| C.在稀溶液中H+(aq)+OH-(aq)===H2O(l) ΔH=-57.3 kJ·mol-1,若将含0.5 molH2SO4的浓硫酸与含1 molNaOH的稀溶液混合,放出的热量为57.3 kJ |
D.由N2O4(g)  2NO2(g) △H=+56.9 kJ·mol-1,可知将1mol N2O4(g)置于密闭容器中充分反应后吸收热量为56.9kJ 2NO2(g) △H=+56.9 kJ·mol-1,可知将1mol N2O4(g)置于密闭容器中充分反应后吸收热量为56.9kJ |
您最近一年使用:0次

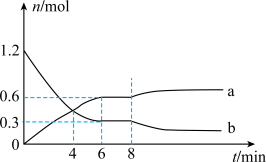
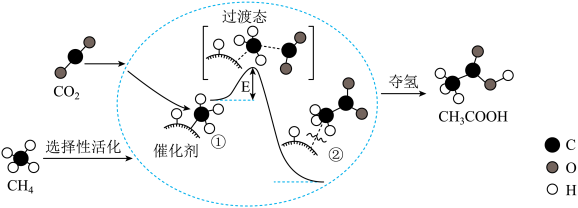
 ②吸收能量并形成了C-C键
②吸收能量并形成了C-C键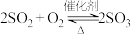 。下列有关该反应的说法不正确的是
。下列有关该反应的说法不正确的是 和
和 不可能全部转化为
不可能全部转化为


