下列叙述或书写正确的是
| A.H2(g)+F2 (g)===2HF(g) △H=-270 kJ·mol -1,则相同条件下,2mol HF气体的能量大于1mol氢气和1mol氟气的能量之和 |
| B.2H2(g)+O2(g)===2H2O(g) △H=-483.6kJ·mol-1,则氢气的燃烧热大于241.8kJ.mol-1 |
| C.含20.0gNaOH的稀溶液与稀盐酸完全中和,放出28.7kJ的热量,则表示该中和反应的热化学方程式为NaOH+HCl===NaCl+H2O △H =-57.4kJ·mol-1 |
D.500℃、30MPa时,发生反应N2(g)+3H2(g)  2NH3(g) △H =-38.6kJ·mol-1在此条件下将1.5molH2和过量N2充分反应,放出热量19.3kJ 2NH3(g) △H =-38.6kJ·mol-1在此条件下将1.5molH2和过量N2充分反应,放出热量19.3kJ |
更新时间:2019-01-05 11:23:27
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】下列关于热能的说法正确的是
| A.已知2H2(g)+O2(g)=2H2O(g) ΔH=-571.6 kJ/mol,则氢气的燃烧热为-285.8 kJ/mol |
| B.已知2C(s)+2O2(g)=2CO2(g) ΔH1;2C(s)+O2(g)=2CO(g) ΔH2,则ΔH1>ΔH2 |
| C.盐酸和NaOH溶液反应的中和热ΔH =-57.3kJ/mol,则NaOH溶液和醋酸溶液反应的中和热ΔH<-57.3kJ/mol |
| D.同温同压下,H2(g)+Cl2(g)═2HCl(g)在光照和点燃条件下的ΔH相同 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】根据下列表述,相关热化学方程式的书写和叙述,正确的是
| A.已知C(石墨,s)=C(金刚石,s) △H>0,则金刚石比石墨稳定 |
B.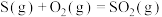  ; ;  ,则 ,则 |
C.已知12.8g硫粉与11.2g铁粉混合加热生成17.6gFeS时放出19.12kJ热量,则  |
D.在稀溶液中: 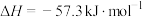 ,若将0.5 ,若将0.5 的稀 的稀 与1 与1 的NaOH的溶液等体积混合,放出的热量等于57.3kJ 的NaOH的溶液等体积混合,放出的热量等于57.3kJ |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】下列叙述正确的是:
①热稳定性:H2O>HF>H2S
②熔点:Al>Na>K
③IA、IIA族元素的阳离子与同周期稀有气体元素的原子具有相同的核外电子排布
④结合质子(H+)能力:CO32﹣>HCO3﹣>SO42﹣
⑤同一主族的元素的氢化物,相对分子质量越大,它的沸点一定越高
⑥已知2H2(g)+O2(g)=2H2O(1);△H=﹣571.6kJ•mol﹣1,则氢气的燃烧热为285.8kJ•mol﹣1,
⑦因为常温下白磷可自燃,而氮气须在放电时才与氧气反应,所以非金属性:P>N( )
①热稳定性:H2O>HF>H2S
②熔点:Al>Na>K
③IA、IIA族元素的阳离子与同周期稀有气体元素的原子具有相同的核外电子排布
④结合质子(H+)能力:CO32﹣>HCO3﹣>SO42﹣
⑤同一主族的元素的氢化物,相对分子质量越大,它的沸点一定越高
⑥已知2H2(g)+O2(g)=2H2O(1);△H=﹣571.6kJ•mol﹣1,则氢气的燃烧热为285.8kJ•mol﹣1,
⑦因为常温下白磷可自燃,而氮气须在放电时才与氧气反应,所以非金属性:P>N( )
| A.②③④ | B.①⑥⑦ | C.②④⑥ | D.③⑤⑦ |
您最近半年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】氢气、甲烷、乙烷、一氧化碳燃烧热分别为 、
、 、
、 、
、 ,相同质量上述四种物质分别燃烧放出热量最多的是
,相同质量上述四种物质分别燃烧放出热量最多的是
 、
、 、
、 、
、 ,相同质量上述四种物质分别燃烧放出热量最多的是
,相同质量上述四种物质分别燃烧放出热量最多的是
| A.氢气 | B.甲烷 | C.乙烷 | D.一氧化碳 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】沼气是一种能源,它的主要成分是CH4,标准状况下,0.5 mol CH4完全燃烧生成CO2和H2O时,放出445 kJ的热量,则表示CH4燃烧热的热化学方程式正确的是
A. CH4(g)+O2(g)= CH4(g)+O2(g)= CO2(g)+H2O(l) ΔH =−445 kJ/mol CO2(g)+H2O(l) ΔH =−445 kJ/mol |
| B.CH4+2O2=CO2+2H2O ΔH=−890 kJ/mol |
| C.CH4(g)+2O2(g)=CO2(g)+2 H2O(g) ΔH =−890 kJ/mol |
| D.CH4(g)+2O2(g)=CO2(g)+2H2O(l) ΔH = −890 kJ/mol |
您最近半年使用:0次
单选题
|
适中
(0.65)
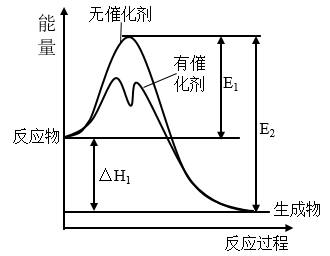
【推荐1】2SO2(g)+O2(g) 2SO3(g) △H1,反应过程中的能量变化如图所示。下列有关叙述
2SO3(g) △H1,反应过程中的能量变化如图所示。下列有关叙述错误 的是
 2SO3(g) △H1,反应过程中的能量变化如图所示。下列有关叙述
2SO3(g) △H1,反应过程中的能量变化如图所示。下列有关叙述
A.SO2(g)+ O2(g) O2(g) SO3(g) △H2= SO3(g) △H2= △H1 △H1 |
| B.温度升高,逆反应速率加快幅度大于正反应加快幅度 |
| C.该反应的正反应为放热反应,△H1=(E1-E2)kJ·mol-1 |
| D.使用催化剂可降低活化能,提高活化分子百分数 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】如图示与对应的叙述符合的是
A.如图可知实线、虚线分别表示某可逆反应未使用催化剂和使用催化剂的正、逆反应速率随时间的变化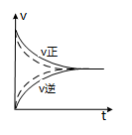 |
B.如图可知,反应C(金刚石,s) ══ C(石墨,s)的焓变ΔH ══ ΔH1-ΔH2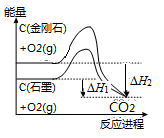 |
C.如图可知表示除去氧化膜的镁条放入盐酸中生成氢气速率随时间的变化,起初反应速率加快的原因可能是该反应为放热反应 |
D.如图可知表示25℃时用0.1000 mol·L-1醋酸滴定40.00 mL 0.1000 mol·L-1NaOH溶液得到的滴定曲线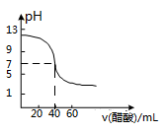 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
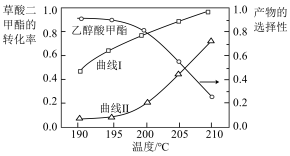
【推荐3】用草酸二甲酯(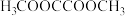 )和氢气为原料制备乙二醇的反应原理如下:
)和氢气为原料制备乙二醇的反应原理如下:
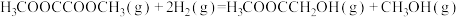


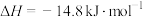
在2MPa条件下,将氢气和草酸二甲酯体积比(氢酯比)为80:1的混合气体以一定流速通过装有催化剂的反应管,草酸二甲酯的转化率、产物的选择性与温度的关系如图所示。
下列说法正确的是
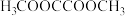 )和氢气为原料制备乙二醇的反应原理如下:
)和氢气为原料制备乙二醇的反应原理如下: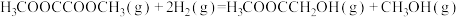


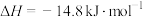
在2MPa条件下,将氢气和草酸二甲酯体积比(氢酯比)为80:1的混合气体以一定流速通过装有催化剂的反应管,草酸二甲酯的转化率、产物的选择性与温度的关系如图所示。

下列说法正确的是
| A.曲线I表示乙二醇的选择性随温度的变化 |
| B.其他条件不变,增大压强或升高温度,草酸二甲酯的平衡转化率均增大 |
| C.其他条件不变,在190~195℃温度范围,随着温度升高,出口处乙醇酸甲酯的量不断减小 |
D.其他条件不变,在190~210℃温度范围,随着温度升高,出口处甲醇和乙二醇的物质的量之比[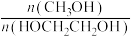 ]减小 ]减小 |
您最近半年使用:0次


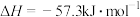 ,则含56.0gKOH的稀溶液与稀次氯酸完全反应中和,放出57.3kJ的热量
,则含56.0gKOH的稀溶液与稀次氯酸完全反应中和,放出57.3kJ的热量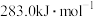 ,则
,则 反应的
反应的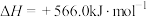
 ;
; ;则
;则