20. 丙烯是重要的有机化工原料,主要用于生产聚丙烯、丙烯腈、环氧丙烷等。
(1)以丁烯和乙烯为原料反应生成丙烯的方法被称为“烯烃歧化法”,反应为:C
4H
8(g)+C
2H
4(g)
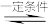
2C
3H
6(g)。已知:
①C
2H
4(g)+3O
2(g)=2CO
2(g)+2H
2O(l) ∆
H1=-1411kJ•mol
-1②C
3H
6(g)+

O
2(g)=3CO
2(g)+3H
2O(l) ∆
H2=-2049kJ•mol
-1③C
4H
8(g)+6O
2(g)=4CO
2(g)+4H
2O(l) ∆
H3=-2539kJ•mol
-1“烯烃歧化法”的反应的热化学方程式为
_______。
(2)一定温度下,在一体积恒为V升的密闭容器中充入一定量的C
4H
8和C
2H
4,发生烯烃歧化法的主要反应。t
1时刻达到平衡状态,此时容器中n(C
4H
8)=amol,n(C
2H
4)=2amol,n(C
3H
6)=bmol,且C
3H
6占平衡总体积的1/4。
①求该时间段内的反应速率v(C
4H
8)=
_______。(用只含a、V、t
1的式子表示)
②判断该反应达到平衡的标志是
_______A.2v(C
4H
8)
生成=v(C
3H
6)
消耗B.C
4H
8、C
2H
4、C
3H
6的物质的量之比为1:1:2
C.混合气体的平均相对分子质量不再改变
D.C
4H
8、C
2H
4、C
3H
6的浓度均不再变化
(3)Kp是用反应体系中气体物质的分压来表示的平衡常数,即将K表达式中平衡浓度用平衡分压代替。已知反应﹕C
4H
8(g)+C
2H
4(g)
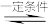
2C
3H
6(g),该反应中正反应速率v
正=k
正·p(C
4H
8)·p(C
2H
4),逆反应速率v
逆=k
逆·p
2(C
3H
6),其中k
正、k
逆为速率常数,则Kp为
_______(用k
正、k
逆表示)。
II“丁烯裂解法”是另一种重要的丙烯生产法,但生产过程中会有生成乙烯的副反应发生。反应如下主反应:3C
4H
8
4C
3H
6;副反应:C
4H
8
2C
2H
4测得上述两反应的平衡体系中,各组分的质量分数(w%)随温度(T)和压强(P)变化的趋势分别如图1和图2所示:

(4)平衡体系中的丙烯和乙烯的质量比是工业生产丙烯时选择反应条件的重要指标之一,从产物的纯度考虑,该数值越高越好,从图1和图2中表现的趋势来看,下列反应条件最适宜的是
__(填字母序号)。
A.300
oC0.1MPa B.700
oC0.1MPa C.300
oC0.5MPa D.700
oC0.5MPa
(5)有研究者结合图1数据并综合考虑各种因素,认为450℃的反应温度比300℃或700℃更合适,从反应原理角度分析其理由可能是
____。
(6)图2中,随压强增大平衡体系中丙烯的百分含量呈上升趋势,从平衡角度解释其原因是
__。