回答下列问题:
(1)19 g某二价金属氯化物(ACl2)中含有0.4 molCl−,则ACl2的摩尔质量是____ g/mol;ACl2的化学式是_____ 。
(2)配制480 mL 0.1mol/L的硫酸铜溶液,需用托盘天平称取CuSO4·5H2O____ g;在配制过程中,若其它操作均正确,则下列操作会使所配溶液物质的量浓度偏低的是_________ (填字母序号)。
A.溶解后小烧杯、玻璃棒没有洗涤
B.所用容量瓶中,已有少量蒸馏水
C.定容、加盖倒转摇匀后,发现液面低于刻度线,又滴加蒸馏水至刻度线
D.定容时俯视刻度线
(3)将适量铁粉加到三氯化铁溶液中,完全反应后,溶液中的Fe3+和Fe2+浓度相等,则已反应的Fe3+和未反应的Fe3+的物质的量之比是______ 。
(1)19 g某二价金属氯化物(ACl2)中含有0.4 molCl−,则ACl2的摩尔质量是
(2)配制480 mL 0.1mol/L的硫酸铜溶液,需用托盘天平称取CuSO4·5H2O
A.溶解后小烧杯、玻璃棒没有洗涤
B.所用容量瓶中,已有少量蒸馏水
C.定容、加盖倒转摇匀后,发现液面低于刻度线,又滴加蒸馏水至刻度线
D.定容时俯视刻度线
(3)将适量铁粉加到三氯化铁溶液中,完全反应后,溶液中的Fe3+和Fe2+浓度相等,则已反应的Fe3+和未反应的Fe3+的物质的量之比是
更新时间:2019-02-01 18:01:03
|
相似题推荐
计算题
|
适中
(0.65)
【推荐1】计算填空:
(1)实验室要配制360 g 10%的盐酸,需要36%的浓盐酸的质量是_______ 。
(2)配制溶质质量分数20%的稀硫酸溶液100 g,需要98%的浓硫酸(密度为1.84 g·mL-1)的体积是_______ 。
(3)配制溶质质量分数为20%的硫酸溶液1000g,需要98%的浓硫酸的质量是_______ ,需要10%的稀硫酸的质量是_______ 。
(1)实验室要配制360 g 10%的盐酸,需要36%的浓盐酸的质量是
(2)配制溶质质量分数20%的稀硫酸溶液100 g,需要98%的浓硫酸(密度为1.84 g·mL-1)的体积是
(3)配制溶质质量分数为20%的硫酸溶液1000g,需要98%的浓硫酸的质量是
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】现从固体KOH出发配制0.1mol/L 的KOH溶液 500mL,回答下列问题:
(1)配制过程中需要用到的玻璃仪器有烧杯、玻璃棒、量筒、胶头滴管、___________
(2)如果在定容时仰视操作,则所配得溶液的浓度_______ 0.1mol/L(填> , =" ," <)
(3)若所用的固体KOH中混有NaOH,则所配得溶液的OH-浓度___ 0.1mol/L(填> , =" ," <)
(4)若用250mL的H2SO4溶液恰好能将此500mL 0.1mol/L 的KOH溶液中和,则该硫酸的物质的量浓度为________ mol/L
(1)配制过程中需要用到的玻璃仪器有烧杯、玻璃棒、量筒、胶头滴管、
(2)如果在定容时仰视操作,则所配得溶液的浓度
(3)若所用的固体KOH中混有NaOH,则所配得溶液的OH-浓度
(4)若用250mL的H2SO4溶液恰好能将此500mL 0.1mol/L 的KOH溶液中和,则该硫酸的物质的量浓度为
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐3】根据所学知识回答下列问题:
(1)常温下铝具有较强的抗腐蚀性,主要原因是___________ 。
(2)标准状况下, 氨气与同条件下
氨气与同条件下___________ gH2S含有相同的氢原子数。
(3)标准状况下, 由
由 和
和 组成的混合气体的质量为12g,则
组成的混合气体的质量为12g,则 和
和 的物质的量之比是
的物质的量之比是___________ 。
(4)将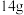 由
由 和
和 组成的混合物加入足量的水中充分反应后,生成标准状况下
组成的混合物加入足量的水中充分反应后,生成标准状况下 气体所得溶液的体积为
气体所得溶液的体积为 。则原混合物中
。则原混合物中 的物质的量为
的物质的量为___________  ;所得溶液中溶质的物质的量浓度为
;所得溶液中溶质的物质的量浓度为___________  。
。
(5)实验室籥配制 溶液,实际应称量绿矾(
溶液,实际应称量绿矾( )的质量为
)的质量为___________ g。配制时,其正确的操作顺序是___________ (填标号,每个标号只能用一次)。
①用 水洗涤烧杯2~3次,洗涤液均注入容量瓶,振荡
水洗涤烧杯2~3次,洗涤液均注入容量瓶,振荡
②将准确称量的绿矾倒入烧杯中,再加适量水溶解
③将已冷却的溶液沿玻璃棒注入容量瓶中
④将容量瓶盖紧振荡,反复上下颠倒,摇匀
⑤改用胶头滴管加水,使溶液凹面恰好与刻度线相切
⑥继续往容量瓶内小心加水,直到液面接近刻度线下 处
处
(1)常温下铝具有较强的抗腐蚀性,主要原因是
(2)标准状况下,
 氨气与同条件下
氨气与同条件下(3)标准状况下,
 由
由 和
和 组成的混合气体的质量为12g,则
组成的混合气体的质量为12g,则 和
和 的物质的量之比是
的物质的量之比是(4)将
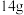 由
由 和
和 组成的混合物加入足量的水中充分反应后,生成标准状况下
组成的混合物加入足量的水中充分反应后,生成标准状况下 气体所得溶液的体积为
气体所得溶液的体积为 。则原混合物中
。则原混合物中 的物质的量为
的物质的量为 ;所得溶液中溶质的物质的量浓度为
;所得溶液中溶质的物质的量浓度为 。
。(5)实验室籥配制
 溶液,实际应称量绿矾(
溶液,实际应称量绿矾( )的质量为
)的质量为①用
 水洗涤烧杯2~3次,洗涤液均注入容量瓶,振荡
水洗涤烧杯2~3次,洗涤液均注入容量瓶,振荡②将准确称量的绿矾倒入烧杯中,再加适量水溶解
③将已冷却的溶液沿玻璃棒注入容量瓶中
④将容量瓶盖紧振荡,反复上下颠倒,摇匀
⑤改用胶头滴管加水,使溶液凹面恰好与刻度线相切
⑥继续往容量瓶内小心加水,直到液面接近刻度线下
 处
处
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐1】按要求完成。
(1)19.6克硫酸是___________ molH2SO4,含有___________ 个原子,1.7克NH3在同温同压下与___________ 克H2S气体含有的氢原子数相同。
(2)标准状况下,密度为0.75g/L的NH3与CH4组成的混合气体中,NH3的体积分数___________ ,混合气体的平均摩尔质量为___________ 该气体对氢气的相对密度为___________ 。
(3)已知Wg气体A含有a个分子,那么在标准状况下,bg气体A所占的体积是___________ (其中阿伏加德罗常数用NA表示)。
(4)将MgCl2·xH2O的晶体4.06g溶于水配成100mL溶液,取出50mL溶液正好与0.02moL的AgNO3溶液完全作用,4.06g的MgCl2·xH2O物质的量为___________ 式中x的数值___________ 。
(5)配制100mL1mol·L-1的稀H2SO4溶液,需要用量筒量取浓H2SO4(密度为1.84g·mL-1,质量分数为98%)的体积为___________ mL。
(6)现要配制1mol·L-1Na2CO3溶液250mL
①需要含结晶水的碳酸钠晶体(Na2CO3·10H2O)___________ g;
②在配制上述溶液的过程中,可能导致配制溶液浓度偏小的有___________
A.固体Na2CO3·10H2O放在右盘(1g以下用游码);
B.容量瓶用碳酸钠溶液先润洗;
C.转移溶液时未洗涤烧杯
D.定容时溶液未冷却;
E.定容时视线仰视;
F.摇匀时,发现液面低于容量瓶刻度线,但未补加水;
G.容量瓶未干燥。
(1)19.6克硫酸是
(2)标准状况下,密度为0.75g/L的NH3与CH4组成的混合气体中,NH3的体积分数
(3)已知Wg气体A含有a个分子,那么在标准状况下,bg气体A所占的体积是
(4)将MgCl2·xH2O的晶体4.06g溶于水配成100mL溶液,取出50mL溶液正好与0.02moL的AgNO3溶液完全作用,4.06g的MgCl2·xH2O物质的量为
(5)配制100mL1mol·L-1的稀H2SO4溶液,需要用量筒量取浓H2SO4(密度为1.84g·mL-1,质量分数为98%)的体积为
(6)现要配制1mol·L-1Na2CO3溶液250mL
①需要含结晶水的碳酸钠晶体(Na2CO3·10H2O)
②在配制上述溶液的过程中,可能导致配制溶液浓度偏小的有
A.固体Na2CO3·10H2O放在右盘(1g以下用游码);
B.容量瓶用碳酸钠溶液先润洗;
C.转移溶液时未洗涤烧杯
D.定容时溶液未冷却;
E.定容时视线仰视;
F.摇匀时,发现液面低于容量瓶刻度线,但未补加水;
G.容量瓶未干燥。
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐2】每年10月23日上午6∶02到晚上6∶02被誉为“摩尔日”(MoleDay),这个时间的美式写法为6:0210/23,外观与阿伏加德罗常数相似。
(1)amol H2SO4中含有b个氧原子,则阿伏加德罗常数可以表示为___________  。
。
(2)某固体A在一定条件下加热分解,产物全是气体,A的分解反应为: 。现测得分解产生的混合气体对氢气的相对密度为8,则A的摩尔质量为
。现测得分解产生的混合气体对氢气的相对密度为8,则A的摩尔质量为___________  。
。
(3)由CH4和O2组成的混合气体在同温、同压下与CO的密度相同,则混合气体中CH4的体积分数为___________ 。
(4)在某温度时,一定量的元素A的氢化物AH3,在恒温恒压的密闭容器中完全分解为两种气态单质,此时容器的体积变为原来的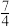 ,则A单质的分子式为
,则A单质的分子式为___________ 。
(5)实验室需配制 溶液,下列叙述中正确的是___________。
溶液,下列叙述中正确的是___________。
(6)某溶液中只含有 、
、 、
、 、
、 等四种离子,它们的物质的量之比为1:6:3:2,该溶液所含的溶质可能是___________。
等四种离子,它们的物质的量之比为1:6:3:2,该溶液所含的溶质可能是___________。
(7)4g下列金属混合物与氯气反应后质量增加7.1g,这种元素是___________。
(1)amol H2SO4中含有b个氧原子,则阿伏加德罗常数可以表示为
 。
。(2)某固体A在一定条件下加热分解,产物全是气体,A的分解反应为:
 。现测得分解产生的混合气体对氢气的相对密度为8,则A的摩尔质量为
。现测得分解产生的混合气体对氢气的相对密度为8,则A的摩尔质量为 。
。(3)由CH4和O2组成的混合气体在同温、同压下与CO的密度相同,则混合气体中CH4的体积分数为
(4)在某温度时,一定量的元素A的氢化物AH3,在恒温恒压的密闭容器中完全分解为两种气态单质,此时容器的体积变为原来的
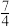 ,则A单质的分子式为
,则A单质的分子式为(5)实验室需配制
 溶液,下列叙述中正确的是___________。
溶液,下列叙述中正确的是___________。| A.容量瓶上标有温度、容积和浓度 |
| B.定容时若俯视刻度线观察液面,会使所配制的NaOH溶液的浓度偏高 |
| C.转移液体时,玻璃棒应紧靠容量瓶口 |
| D.用电子天平称量20gNaOH固体 |
 、
、 、
、 、
、 等四种离子,它们的物质的量之比为1:6:3:2,该溶液所含的溶质可能是___________。
等四种离子,它们的物质的量之比为1:6:3:2,该溶液所含的溶质可能是___________。| A.KNO3、Na2SO4 | B.K2SO4、NaNO3、KNO3 |
| C.KNO3、Na2SO4、NaNO3 | D.K2SO4、Na2SO4、KNO3 |
| A.Na和Fe | B.Mg和Fe | C.Al和Cu | D.Zn和Cu |
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐3】在花瓶中加入“鲜花保鲜剂”可延长鲜花的寿命。下表是1 L“鲜花保鲜剂”的成分,阅读后回答下列问题:
(1)阿司匹林的相对分子质量为______ 。蔗糖的物质的量为______ mol。
(2)1 L“鲜花保鲜剂”中K+的物质的量浓度为(蔗糖、阿司匹林中不含K+)______ mol·L-1。
(3)使用时应将“鲜花保鲜剂”稀释至20倍后使用,稀释后c(AgNO3)=______ mol·L-1(用科学记数法表示)。
(4)配制1 L上述“鲜花保鲜剂”过程中,下列操作使配制浓度偏低的是______ 。
A.容量瓶在使用前未干燥,里面有少量蒸馏水
B.定容时仰视
C.用蒸馏水洗涤烧杯和玻璃棒2~3次,洗涤液倒入废液缸中,防止污染环境
D.定容摇匀后发现液面低于容量瓶的刻度线,但未做任何处理
(5)高锰酸钾的作用除了做钾肥外,还有消毒杀菌的作用,说明高锰酸钾具有______ 性。已知氯气也是常用消毒剂,“鲜花保鲜剂”中高锰酸钾的消毒效率(消毒效率是指单位质量的消毒剂得电子数的多少,KMnO4被还原为Mn2+)相当于氯气的______ 倍。(保留1位小数)
| 成分 | 质量/g | 摩尔质量/(g·mol-1) |
| 蔗糖 | 85.50 | 342 |
| 硫酸钾 | 0.87 | 174 |
| 阿司匹林 | 0.35 | 180 |
| 高锰酸钾 | 1.58 | 158 |
| 硝酸银 | 0.034 | 170 |
(2)1 L“鲜花保鲜剂”中K+的物质的量浓度为(蔗糖、阿司匹林中不含K+)
(3)使用时应将“鲜花保鲜剂”稀释至20倍后使用,稀释后c(AgNO3)=
(4)配制1 L上述“鲜花保鲜剂”过程中,下列操作使配制浓度偏低的是
A.容量瓶在使用前未干燥,里面有少量蒸馏水
B.定容时仰视
C.用蒸馏水洗涤烧杯和玻璃棒2~3次,洗涤液倒入废液缸中,防止污染环境
D.定容摇匀后发现液面低于容量瓶的刻度线,但未做任何处理
(5)高锰酸钾的作用除了做钾肥外,还有消毒杀菌的作用,说明高锰酸钾具有
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐1】一种含钠的化合物W的组成可以表示为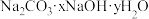 。为测定其组成,某学习小组做了如下实验:
。为测定其组成,某学习小组做了如下实验:
①称取27.6g化合物W,并配制成100mL 的物质的量浓度为
的物质的量浓度为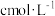 的溶液。
的溶液。
②取出10mL①中所得溶液,加入足量的 溶液,充分反应后,将得到的沉淀过滤、洗涤、干燥,称量得1.97g固体a。
溶液,充分反应后,将得到的沉淀过滤、洗涤、干燥,称量得1.97g固体a。
③另取出10mL①中所得溶液,加入1 的盐酸,充分反应至无气体放出,消耗盐酸的体积为40mL。
的盐酸,充分反应至无气体放出,消耗盐酸的体积为40mL。
(1)配制成100 mL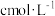 溶液时,需要用到的玻璃仪器有烧杯、量筒、玻璃棒、
溶液时,需要用到的玻璃仪器有烧杯、量筒、玻璃棒、_______ 。
(2)固体a为_______ (填化学式)。
(3)化合物W的组成中x=_______ ,y=_______ 。
(4)①中c=_______ 。
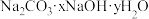 。为测定其组成,某学习小组做了如下实验:
。为测定其组成,某学习小组做了如下实验:①称取27.6g化合物W,并配制成100mL
 的物质的量浓度为
的物质的量浓度为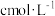 的溶液。
的溶液。②取出10mL①中所得溶液,加入足量的
 溶液,充分反应后,将得到的沉淀过滤、洗涤、干燥,称量得1.97g固体a。
溶液,充分反应后,将得到的沉淀过滤、洗涤、干燥,称量得1.97g固体a。③另取出10mL①中所得溶液,加入1
 的盐酸,充分反应至无气体放出,消耗盐酸的体积为40mL。
的盐酸,充分反应至无气体放出,消耗盐酸的体积为40mL。(1)配制成100 mL
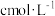 溶液时,需要用到的玻璃仪器有烧杯、量筒、玻璃棒、
溶液时,需要用到的玻璃仪器有烧杯、量筒、玻璃棒、(2)固体a为
(3)化合物W的组成中x=
(4)①中c=
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】医院处方药“复方电解质注射液”可作为水、电解质的补充源,注射液中含有NaCl、MgCl2和KCl三种无机盐,其中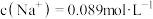 。
。
(1)若实验室药配制该电解质注射液500mL,所需的玻璃仪器有:玻璃板、烧杯和_______ ,需用托盘天平称量氯化钠固体___________ g;
(2)已知该注射液中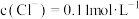 ,
,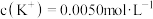 ,则
,则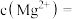
________  。
。
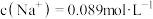 。
。(1)若实验室药配制该电解质注射液500mL,所需的玻璃仪器有:玻璃板、烧杯和
(2)已知该注射液中
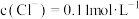 ,
,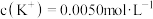 ,则
,则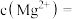
 。
。
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐3】光卤石(xKCl·yMgCl2·zH2O)的组成可通过下列实验测定:
(1)准确称取5.550g样品溶于水,配成100.00mL溶液,将溶液分成二等份。配制100.00mL溶液时,所需的玻璃仪器有:烧杯、玻璃棒、胶头滴管,还有_______ 。
(2)在一份中加入足量的NaOH溶液至沉淀完全,过滤、洗涤、干燥至恒重,得到白色固体[Mg(OH)2]0.580g,其中一份中n(Mg2+)=_________ mol
(3)在另一份溶液中加入足量的HNO3酸化的AgNO3溶液至沉淀完全,过滤、洗涤、干燥至恒重,得到白色固体4.305g,其中一份中n(Cl-)=________ mol
(4)其中一份中n(K+)=___________ mol,n(H2O)=____________ mol
(5)光卤石的化学式为______________________
(1)准确称取5.550g样品溶于水,配成100.00mL溶液,将溶液分成二等份。配制100.00mL溶液时,所需的玻璃仪器有:烧杯、玻璃棒、胶头滴管,还有
(2)在一份中加入足量的NaOH溶液至沉淀完全,过滤、洗涤、干燥至恒重,得到白色固体[Mg(OH)2]0.580g,其中一份中n(Mg2+)=
(3)在另一份溶液中加入足量的HNO3酸化的AgNO3溶液至沉淀完全,过滤、洗涤、干燥至恒重,得到白色固体4.305g,其中一份中n(Cl-)=
(4)其中一份中n(K+)=
(5)光卤石的化学式为
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐1】将 19.5 g锌粒投入250 mL 2mol/L的硫酸溶液中,试计算:(写出计算过程)
(1)产生的氢气在标准状况下的体积;
(2)忽略溶液体积变化体积,反应后溶液中氢离子浓度是多少?
(3)要配制250 mL 2mol/L的硫酸溶液,需用质量百分数为98%,密度为1.84 g/cm3浓硫酸多少毫升?(保留三位有效数字)
(1)产生的氢气在标准状况下的体积;
(2)忽略溶液体积变化体积,反应后溶液中氢离子浓度是多少?
(3)要配制250 mL 2mol/L的硫酸溶液,需用质量百分数为98%,密度为1.84 g/cm3浓硫酸多少毫升?(保留三位有效数字)
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐2】将24.4 g NaOH固体溶于水配成100 mL溶液,其密度为1.22 g·mL-1。
(1)该溶液中NaOH的物质的量浓度为_______________ ;
(2)该溶液中NaOH的质量分数为__________ ;
(3)从该溶液中取出10 mL,其中NaOH的物质的量浓度为__________ ,NaOH的质量分数为__________ ,溶液的密度为___________ ,含NaOH的质量为_________ ,含NaOH的物质的量为__________ ;
(4)将取出的10 mL溶液加水稀释到100 mL,稀释后溶液中NaOH的物质的量浓度为________ 。
(1)该溶液中NaOH的物质的量浓度为
(2)该溶液中NaOH的质量分数为
(3)从该溶液中取出10 mL,其中NaOH的物质的量浓度为
(4)将取出的10 mL溶液加水稀释到100 mL,稀释后溶液中NaOH的物质的量浓度为
您最近一年使用:0次




