现有甲、乙、丙、丁四种物质,乙、丁的焰色反应均为黄色。丙是一种强酸的酸式盐,将丙加入BaCl2溶液有不溶于盐酸的白色沉淀生成,丁晶体在干燥空气中容易逐渐失去结晶水变成白色粉末。对甲、乙、丙、丁进行下列实验,实验过程和记录如下图所示(无关物质已略去),请回答:
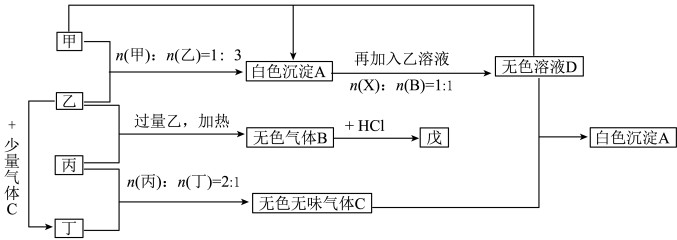
(1)将D溶液蒸干得到的固体是:____________ (写化学式)。
(2)C的结构式是______ ,B的电子式为__________________ 。
(3)写出D溶液与过量的C反应的离子方程式__________________________________ 。
(4)电解戊的水溶液一段时间后,收集到的三种气体,其一为无色气体B,另两种是单质,写出电解戊溶液的总方程式:____________________________ 。
(5)有人设想在适当大小的管道中填充一定量的丁的晶体(摩尔质量在280~300之间),管道环绕在一个房子的周围,这样的房子白天晚上室内温度可保持相对恒定,请简述其原理:_____________________________________ 。

(1)将D溶液蒸干得到的固体是:
(2)C的结构式是
(3)写出D溶液与过量的C反应的离子方程式
(4)电解戊的水溶液一段时间后,收集到的三种气体,其一为无色气体B,另两种是单质,写出电解戊溶液的总方程式:
(5)有人设想在适当大小的管道中填充一定量的丁的晶体(摩尔质量在280~300之间),管道环绕在一个房子的周围,这样的房子白天晚上室内温度可保持相对恒定,请简述其原理:
10-11高三·江苏·阶段练习 查看更多[1]
(已下线)2012届江苏省致远中学高三第一次教学质量检测化学试卷
更新时间:2016/12/09 02:06:24
|
相似题推荐
解答题-无机推断题
|
较难
(0.4)
解题方法
【推荐1】已知X、Y、Z、W四种元素分别是元素周期表中三个连续短周期的元素,且原子序数依次增大。X、W同主族,Y、Z为同周期的相邻元素。W原子的质子数等于Y、Z 原子的最外层电子数之和。Z原子最外层电子数是次外层电子数的3倍,试推断:
(1)上述元素两两形成的化合物中,溶于水显碱性的气态氢化物的电子式为___________ ,含有离子键和非极性共价键的化合物的电子式为_______________________ ;含有极性共价键和非极性共价键的化合物的电子式为____________________ 。
(2)由X、Y、Z所形成的常见离子化合物是_________________________ (写化学式),该化合物与[W的最高价氧化物对应水化物的浓溶液加热时反应的离子方程式为_________ 。
(1)上述元素两两形成的化合物中,溶于水显碱性的气态氢化物的电子式为
(2)由X、Y、Z所形成的常见离子化合物是
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
名校
解题方法
【推荐2】氮和碳一样也存在一系列氢化物,如NH3、N2H4、N3H5、N4H6等。
请回答下列问题
(1)上述氮的系列氢化物的通式为______________ ;N3H5的电子式为_____________________ 。
(2)已知:①4NH3(g)+5O2(g)==4NO(g)+6H2O(g) △H1= a kJ·mol-1 K1
②4NH3(g)+3O2(g)==2N2(g)+6H2O(g) △H2= b kJ·mol-1 K2
写出N2 与O2反应生成1mol NO气体的热化学方程式:________________________________ ;该反应式的平衡常数表达式K=__________________ (用含有K1、K2的代数式表示)。
(3)已知NH3·H2O为一元弱碱,N2H4·H2O 为二元弱碱,N2H4·H2O在水溶液中的一级电离方程式为N2H4·H2O+H2O N2H5·H2O++ OH-,则可溶性盐盐酸肼(N2H6Cl2)
N2H5·H2O++ OH-,则可溶性盐盐酸肼(N2H6Cl2)
第一步水解的离子方程式为_________________________________________________ ;溶液中离子浓度由大到小的顺序为________________________________________________ 。
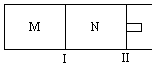
(4)如图所示,隔板I固定不动,活塞II可自由移动,M、N 两个容器中均发生反应:N2(g)+ 3H2(g) 2NH3(g)。向M、N 中均通入lmol N2 和2.3 mol H2。初始时M、N 容积相同,并保持温度不变,则达到平衡时H2 的转化率aM(H2)
2NH3(g)。向M、N 中均通入lmol N2 和2.3 mol H2。初始时M、N 容积相同,并保持温度不变,则达到平衡时H2 的转化率aM(H2)_____ aN(H2)(填“>”“=”“或”)。达到平衡时测得容器N 的容积为2.0 L,其中含有0.2 mol NH3,则此条件下该反应的平衡常数K=______________ 。
请回答下列问题
(1)上述氮的系列氢化物的通式为
(2)已知:①4NH3(g)+5O2(g)==4NO(g)+6H2O(g) △H1= a kJ·mol-1 K1
②4NH3(g)+3O2(g)==2N2(g)+6H2O(g) △H2= b kJ·mol-1 K2
写出N2 与O2反应生成1mol NO气体的热化学方程式:
(3)已知NH3·H2O为一元弱碱,N2H4·H2O 为二元弱碱,N2H4·H2O在水溶液中的一级电离方程式为N2H4·H2O+H2O
 N2H5·H2O++ OH-,则可溶性盐盐酸肼(N2H6Cl2)
N2H5·H2O++ OH-,则可溶性盐盐酸肼(N2H6Cl2)第一步水解的离子方程式为
(4)如图所示,隔板I固定不动,活塞II可自由移动,M、N 两个容器中均发生反应:N2(g)+ 3H2(g)
 2NH3(g)。向M、N 中均通入lmol N2 和2.3 mol H2。初始时M、N 容积相同,并保持温度不变,则达到平衡时H2 的转化率aM(H2)
2NH3(g)。向M、N 中均通入lmol N2 和2.3 mol H2。初始时M、N 容积相同,并保持温度不变,则达到平衡时H2 的转化率aM(H2)
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
名校
【推荐3】短周期主族元素X、Y、Z、W、M的原子半径依次增大,与元素有关的信息如表所示:
回答下列问题:
(1) 的一种核素含有8个中子,其核素符号为
的一种核素含有8个中子,其核素符号为___________ ,写出其简单氢化物的一种用途:___________ 。
(2)由 与
与 组成的化合物含有的化学键类型为
组成的化合物含有的化学键类型为___________ 。
(3)上述元素对应的简单离子中半径最大的为___________ (填离子符号)。
(4) 单质与
单质与 的最高价氧化物对应水化物混合使用,可用于疏通地下管道,其发生反应的离子方程式为
的最高价氧化物对应水化物混合使用,可用于疏通地下管道,其发生反应的离子方程式为___________ 。
(5) 与
与 形成的一种化合物中,所有原子均满足8电子稳定结构,用电子式表示该化合物的形成过程
形成的一种化合物中,所有原子均满足8电子稳定结构,用电子式表示该化合物的形成过程___________ 。
(6) 的简单氢化物的沸点比
的简单氢化物的沸点比 的简单氢化物的沸点高,从结构角度分析其原因为
的简单氢化物的沸点高,从结构角度分析其原因为___________ 。
(7)下列关于 及
及 同主族元素的说法错误的是___________。
同主族元素的说法错误的是___________。
| 元素 | 相关信息 |
 | 简单氢化物的水溶液可以刻蚀玻璃 |
 | 最外层电子数比次外层多3 |
 | 最高正价和最低负价的代数和为4 |
 | 地壳中含量最高的金属元素 |
 | 最高价氧化物对应水化物属于强碱 |
(1)
 的一种核素含有8个中子,其核素符号为
的一种核素含有8个中子,其核素符号为(2)由
 与
与 组成的化合物含有的化学键类型为
组成的化合物含有的化学键类型为(3)上述元素对应的简单离子中半径最大的为
(4)
 单质与
单质与 的最高价氧化物对应水化物混合使用,可用于疏通地下管道,其发生反应的离子方程式为
的最高价氧化物对应水化物混合使用,可用于疏通地下管道,其发生反应的离子方程式为(5)
 与
与 形成的一种化合物中,所有原子均满足8电子稳定结构,用电子式表示该化合物的形成过程
形成的一种化合物中,所有原子均满足8电子稳定结构,用电子式表示该化合物的形成过程(6)
 的简单氢化物的沸点比
的简单氢化物的沸点比 的简单氢化物的沸点高,从结构角度分析其原因为
的简单氢化物的沸点高,从结构角度分析其原因为(7)下列关于
 及
及 同主族元素的说法错误的是___________。
同主族元素的说法错误的是___________。A.将 的单质通入其同族元素与钠形成的钠盐溶液中,可置换出同族元素的单质 的单质通入其同族元素与钠形成的钠盐溶液中,可置换出同族元素的单质 |
| B.随着原子序数递增,该主族元素对应单质的沸点逐渐升高 |
C.该主族元素中最高价氧化物对应水化物酸性最强的元素为 |
D. 的简单氢化物可与强碱溶液反应 的简单氢化物可与强碱溶液反应 |
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
解题方法
【推荐1】下图是某元素及其重要化合物之间的相互转化关系图(生成物中不含该元素的物质均已略去)。其中A是单质,D在常温下呈气态,F可用作氮肥。
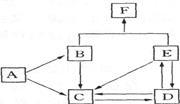
据此,请回答下列问题:
(1)写出以下物质的化学式:A____________ ,D___________________ ,F_____________ 。
(2)写出下列变化的化学方程式:E→C_________________________________ 。

据此,请回答下列问题:
(1)写出以下物质的化学式:A
(2)写出下列变化的化学方程式:E→C
您最近一年使用:0次
解答题-有机推断题
|
较难
(0.4)
解题方法
【推荐2】固体X是由两种常见元素组成的化合物,其中金属元素与另一元素的质量比为14∶1。在一定条件下X可发生如下框图的转化关系,有的反应标出全部产物,有的反应标出部分产物。已知P为两种气体的混合物,R是无色无味能使澄清石灰水变浑浊的气体,C为红褐色物质,M为常见金属单质,Q为常见非金属单质。试填空。
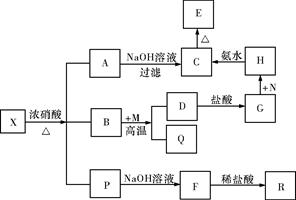
(1)X的化学式为_____ ,P中气体的化学式为_______ 。
(2)实现G→H,欲不引进新的杂质,N可以选择下列物质中的____ (填序号)。
①KMnO4 ②HNO3 ③H2O2 ④Cl2
(3)写出B和M反应的化学方程式:__________ 。
(4)已知P中有一种气体与氢氧化钠溶液反应可生成两种正盐,该反应的离子方程式为_____________________________ 。

(1)X的化学式为
(2)实现G→H,欲不引进新的杂质,N可以选择下列物质中的
①KMnO4 ②HNO3 ③H2O2 ④Cl2
(3)写出B和M反应的化学方程式:
(4)已知P中有一种气体与氢氧化钠溶液反应可生成两种正盐,该反应的离子方程式为
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
解题方法
【推荐3】化合物A由两种元素组成,将A按如下流程进行实验。
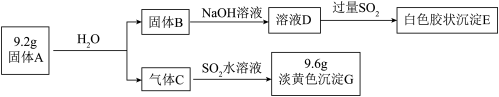
请回答:
(1)组成A的两种元素是______ ,A的化学式是____________ 。
(2)溶液D与过量  反应的离子方程式是
反应的离子方程式是__________ 。
(3)某兴趣小组利用下面实验装置制备气体C,并探究气体C能否与溶液D反应产生白色胶状沉淀:

①装置A是气体C的发生装置,写出该装置中可能发生的化学方程式__________ ,简要描述检查装置A气密性的方法:___________ 。
②该方案还缺少一个尾气吸收装置,下列吸收装置可以选用的是__________ 。
A. B.
B.  C.
C.  D.
D.

请回答:
(1)组成A的两种元素是
(2)溶液D与
 反应的离子方程式是
反应的离子方程式是(3)某兴趣小组利用下面实验装置制备气体C,并探究气体C能否与溶液D反应产生白色胶状沉淀:

①装置A是气体C的发生装置,写出该装置中可能发生的化学方程式
②该方案还缺少一个尾气吸收装置,下列吸收装置可以选用的是
A.
 B.
B.  C.
C.  D.
D.
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
解题方法
【推荐1】有关物质的转化关系如下图所示。C是海水中最多的盐,D是常见的无色液体。E和G为无色气体,其中E能使湿润的红色石蕊试纸变蓝。B、C、I、J的焰色反应为黄色,其中I可用于制发酵粉或治疗胃酸过多。
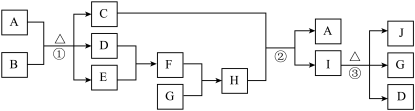
⑴F的化学式为______ 。E的电子式为______ 。
⑵写出反应①的离子方程式:______ 。
⑶写出反应②的化学方程式:______ 。
⑷写出反应③的化学方程式:______ 。

⑴F的化学式为
⑵写出反应①的离子方程式:
⑶写出反应②的化学方程式:
⑷写出反应③的化学方程式:
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
解题方法
【推荐2】已知X是一种酸式盐,常用作化肥,其有如下转化,图中的每一个方格表示有关的一种反应物或生成物,其中常温下,A、C为无色气体。___________ ;F___________ 。
(2)写出 的化学方程式:
的化学方程式:___________ 。
(3)写出实验室制备C的化学方程式:___________ 。
(4)分别取两份50mL NaOH溶液,各向其中通入一定量的A气体,随后各取反应后溶液10mL,分别将其稀释到相同体积,得到溶液甲和乙,分别向甲和乙中逐滴加入 的HCl溶液,产生的A气体体积(标准状况下)与所加入的HCl溶液体积之间的关系如图所示,试分析:
的HCl溶液,产生的A气体体积(标准状况下)与所加入的HCl溶液体积之间的关系如图所示,试分析:___________ ,其物质的量之比是___________ 。
②原NaOH溶液的物质的量浓度是___________  ,溶液甲最多还能吸收A气体的体积为
,溶液甲最多还能吸收A气体的体积为___________ mL(标准状况)。
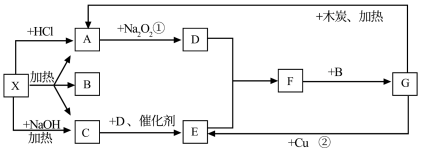
(2)写出
 的化学方程式:
的化学方程式:(3)写出实验室制备C的化学方程式:
(4)分别取两份50mL NaOH溶液,各向其中通入一定量的A气体,随后各取反应后溶液10mL,分别将其稀释到相同体积,得到溶液甲和乙,分别向甲和乙中逐滴加入
 的HCl溶液,产生的A气体体积(标准状况下)与所加入的HCl溶液体积之间的关系如图所示,试分析:
的HCl溶液,产生的A气体体积(标准状况下)与所加入的HCl溶液体积之间的关系如图所示,试分析: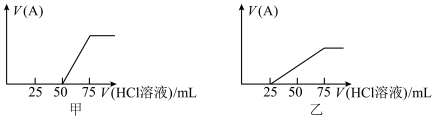
②原NaOH溶液的物质的量浓度是
 ,溶液甲最多还能吸收A气体的体积为
,溶液甲最多还能吸收A气体的体积为
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
名校
解题方法
【推荐3】(Ⅰ)向Ba(OH)2溶液中逐滴加入稀硫酸,请完成下列问题:
(1)写出反应的离子方程式_________________________ 。
(2)下列三种情况下,离子方程式与(1)相同的是________ (填字母)。
A.向NaHSO4溶液中,逐滴加入Ba(OH)2溶液至溶液显中性
B.向NaHSO4溶液中,逐滴加入Ba(OH)2溶液至SO 恰好完全沉淀
恰好完全沉淀
C.向NaHSO4溶液中,逐滴加入Ba(OH)2溶液至过量
(3)若向装有Ba(OH)2溶液的烧杯里缓缓滴入KAl(SO4)2溶液至Ba2+恰好完全反应。则反应的离子方程式是___________ 。
(Ⅱ)某无色溶液中可能含有H+、NH 、Mg2+、Fe3+、Al3+、SO
、Mg2+、Fe3+、Al3+、SO 、HCO
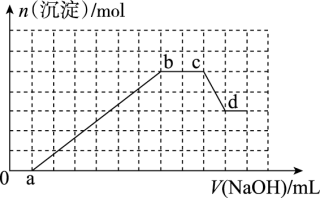
、HCO 等离子,当向溶液中加入一定浓度NaOH溶液时,生成沉淀的物质的量随加入NaOH溶液的体积关系如图所示。
等离子,当向溶液中加入一定浓度NaOH溶液时,生成沉淀的物质的量随加入NaOH溶液的体积关系如图所示。
请回答下列问题:
(1)ab段生成的沉淀的化学式为_______________ ;
(2)cd段沉淀减少的离子方程式为_________________ ;
(3)bc段表明溶液中有______ (填离子符号),检验该离子的实验操作及现象是_______________ ;
(4)原溶液中一定含有的离子的物质的量之比为______
(1)写出反应的离子方程式
(2)下列三种情况下,离子方程式与(1)相同的是
A.向NaHSO4溶液中,逐滴加入Ba(OH)2溶液至溶液显中性
B.向NaHSO4溶液中,逐滴加入Ba(OH)2溶液至SO
 恰好完全沉淀
恰好完全沉淀C.向NaHSO4溶液中,逐滴加入Ba(OH)2溶液至过量
(3)若向装有Ba(OH)2溶液的烧杯里缓缓滴入KAl(SO4)2溶液至Ba2+恰好完全反应。则反应的离子方程式是
(Ⅱ)某无色溶液中可能含有H+、NH
 、Mg2+、Fe3+、Al3+、SO
、Mg2+、Fe3+、Al3+、SO 、HCO
、HCO 等离子,当向溶液中加入一定浓度NaOH溶液时,生成沉淀的物质的量随加入NaOH溶液的体积关系如图所示。
等离子,当向溶液中加入一定浓度NaOH溶液时,生成沉淀的物质的量随加入NaOH溶液的体积关系如图所示。
请回答下列问题:
(1)ab段生成的沉淀的化学式为
(2)cd段沉淀减少的离子方程式为
(3)bc段表明溶液中有
(4)原溶液中一定含有的离子的物质的量之比为
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
解题方法
【推荐1】某化工厂以软锰矿、闪锌矿(除主要成分为MnO2、ZnS外还含有少量的FeS、CuS、Al2O3等物质)为原料制取Zn和MnO2。
(1)在一定条件下,将这两种矿粉在硫酸溶液中相互作用,配平如下的化学方程式:MnO2 + FeS + H2SO4=MnSO4 + Fe2(SO4)3 + S + H2O________
(2)将所得含有Mn2+、Fe3+、Cu2+、Al3+、Zn2+的酸性溶液按以下的工业流程进行操作处理得溶液(Ⅳ),电解溶液(Ⅳ)即得MnO2和Zn。

a.操作①中加Zn粉后发生反应的离子方程式为______________________________ 。
b.操作②中加入适量X的作用是什么__________ ;X的首选物的化学式是__________ 。
c.操作③中所加碳酸盐的化学式是______________________________ 。
(3)为了从上述流程中产生的Fe(OH)3、Al(OH)3沉淀混合物中回收Al(OH)3,工厂设计了如下的有关流程图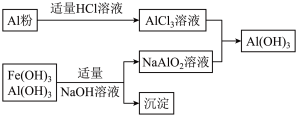
a.AlCl3溶液和NaAlO2溶液反应生成Al(OH)3的离子方程式为________________________ ,若总共得到n molAl(OH)3,则消耗的NaOH和HCl的理论量(mol)分别为_____ 、_____ 。
b.若使用下列流程回收处理,请比较两个流程消耗酸碱的用量____ ?
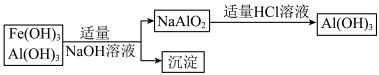
(1)在一定条件下,将这两种矿粉在硫酸溶液中相互作用,配平如下的化学方程式:MnO2 + FeS + H2SO4=MnSO4 + Fe2(SO4)3 + S + H2O
(2)将所得含有Mn2+、Fe3+、Cu2+、Al3+、Zn2+的酸性溶液按以下的工业流程进行操作处理得溶液(Ⅳ),电解溶液(Ⅳ)即得MnO2和Zn。

a.操作①中加Zn粉后发生反应的离子方程式为
b.操作②中加入适量X的作用是什么
c.操作③中所加碳酸盐的化学式是
(3)为了从上述流程中产生的Fe(OH)3、Al(OH)3沉淀混合物中回收Al(OH)3,工厂设计了如下的有关流程图

a.AlCl3溶液和NaAlO2溶液反应生成Al(OH)3的离子方程式为
b.若使用下列流程回收处理,请比较两个流程消耗酸碱的用量

您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
解题方法
【推荐2】A、B、C三种物质中均含有同一种元素,它们之间有如右图所示的转化关系(部分反应物质已略去)。

Ⅰ.(1)若A是一种两性氧化物,B的水溶液呈酸性,请写出反应④的离子方程式:______________ ,B溶液显酸性的原因(用离子方程式表示)_____________ 。
(2)若反应①为置换反应,反应④为化合反应,C物质大量存在于海水中,是人体生理活动不可缺少的物质。工业上可以用C来制取A或B,保存少量单质A的方法 是__________ ,A在氧气中燃烧产物所含的化学键有_______________ ;用C来制取B反应的化学方程式为______________________ 。
(3)若反应①②③均为化合反应,反应④为置换反应。当A为一种金属单质时,请写出反应③可能的离子方程式________________________ 。若只用一种试剂鉴别B、C,可以选的试剂是_____________ 。

Ⅰ.(1)若A是一种两性氧化物,B的水溶液呈酸性,请写出反应④的离子方程式:
(2)若反应①为置换反应,反应④为化合反应,C物质大量存在于海水中,是人体生理活动不可缺少的物质。工业上可以用C来制取A或B,保存少量单质A的方法 是
(3)若反应①②③均为化合反应,反应④为置换反应。当A为一种金属单质时,请写出反应③可能的离子方程式
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
【推荐3】IA、B、C、D均为中学化学中常见的物质,它们之间转化关系如下图(部分产物已略去):
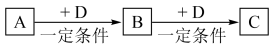
试回答:
(1)若D是具有氧化性的单质,则属于主族的金属A为___________ (填元素符号)
(2)若D是金属,C溶液在储存时应加入少最D,其理由是(用必要的文字和离子方程式表示)_____________________ ;
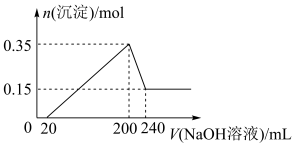
(3)若A、B、C为含同一种金属元素的无机化合物.在溶液中A和C反应生成B。请写出B转化为C的所有可能的离子力程式_________________________________________ 。化合物B经过一系列反应可以得到单质E,将一定质量的Mg和E的混合物投入500mL稀硫酸中,固体全部溶解并产生气体。待反应完全后.向所得溶液中加入NaOH溶液,生成沉淀的物质的是与加入溶液的体积关系如下图所示。则固体混合物中Mg的质量为_____________ ;NaOH溶液的物质的量浓度为___________ 。
II某一离子反应体系有反应物和产物共以下六种: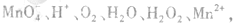
已知该反应中的H2O2只发生如下过程:
(1)该反应中的还原剂是___________ 。
(2)该反应中发生还原反应的过程是_____ →_____ 。
(3)溶液随着酸性的增强氧化性不断增强,应选择__________ (选填“稀硫酸”或“浓盐酸”)进行KMnO4溶液的酸化。
(4)如反应转移了0.6mol电子,则产生的气体在标准状况下体积为__________ 。

试回答:
(1)若D是具有氧化性的单质,则属于主族的金属A为
(2)若D是金属,C溶液在储存时应加入少最D,其理由是(用必要的文字和离子方程式表示)
(3)若A、B、C为含同一种金属元素的无机化合物.在溶液中A和C反应生成B。请写出B转化为C的所有可能的离子力程式

II某一离子反应体系有反应物和产物共以下六种:
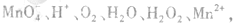
已知该反应中的H2O2只发生如下过程:

(1)该反应中的还原剂是
(2)该反应中发生还原反应的过程是
(3)溶液随着酸性的增强氧化性不断增强,应选择
(4)如反应转移了0.6mol电子,则产生的气体在标准状况下体积为
您最近一年使用:0次



