物质的类别和核心元素的化合价是研究物质性质的两个基本视角。请根据下图所示,回答下列问题:

已知:氢化物指的是由氢元素和另一种元素组成的化合物,例如NH3就是氮元素的一种氢化物。
(1)X的化学式为________ 。
(2)W的浓溶液与铜单质在加热条件下可以发生化学反应,反应的化学方程式为__________ 。
(3)已知SO3是一种酸性氧化物,则SO3与NaOH溶液反应的离子方程式为_____________ 。
(4)欲制备Na2S2O3(硫代硫酸钠),从氧化还原反应角度分析,合理的是_______ (填序号)。
A.Na2S+S B.Na2SO3+S
C.Na2SO3+Na2SO4 D.SO2+Na2SO4
(5)将X与Y混合,可生成淡黄色固体,该反应的氧化产物与还原产物的质量之比为________ 。

已知:氢化物指的是由氢元素和另一种元素组成的化合物,例如NH3就是氮元素的一种氢化物。
(1)X的化学式为
(2)W的浓溶液与铜单质在加热条件下可以发生化学反应,反应的化学方程式为
(3)已知SO3是一种酸性氧化物,则SO3与NaOH溶液反应的离子方程式为
(4)欲制备Na2S2O3(硫代硫酸钠),从氧化还原反应角度分析,合理的是
A.Na2S+S B.Na2SO3+S
C.Na2SO3+Na2SO4 D.SO2+Na2SO4
(5)将X与Y混合,可生成淡黄色固体,该反应的氧化产物与还原产物的质量之比为
18-19高一下·湖北荆州·阶段练习 查看更多[7]
河南省洛阳市洛阳格致学校2021-2022学年高一下学期三月月考化学试题(已下线)【浙江新东方】在线化学98高一下(人教版2019)必修第二册 第五章 化工生产中的重要非金属元素 第一节 硫及其化合物(已下线)专题01 硫及其化合物(核心素养卷)-【新教材精创】2019-2020学年高一化学新教材知识讲学(必修第二册)新人教版必修2同步测试:5.1.3不同价态含硫物质的转化山东省微山县第二中学2020届高三上学期第二学段质量检测化学试题【全国百强校】湖北省荆州市沙市中学2018-2019学年高一下学期2月月考化学试题
更新时间:2019-03-05 14:50:24
|
相似题推荐
【推荐1】(1)已知:氢化钠(NaH)为白色晶体,其中H-有很强的还原性,因此常用氢化钠在高温下将TiCl4还原为Ti,自身被氧化为+1价,写出其化学反应方程式,并用双线桥标出电子转移的方向与数目______________________
(2)自来水中的NO3-对人类健康产生危害。为了降低自来水中NO3-的浓度,某研究人员提出在碱性条件下用A粉还原NO3-,发生的反应可表示如下,请配平下列反应方程式:
____ 、____ 、____ 、____ 、____ 、___ 、
(3)碘是人体不可缺乏的元素,为了防止碘缺乏,现在市场上流行一种加碘盐,就是在精盐中添加一定量的KIO3进去。某研究小组为了检测某加碘盐中是否含有碘,查阅了有关的资料,发现其检测原理是:
①该反应的氧化剂是____________ 氧化产物与还原产物的物质的量比是__________
②如果反应生成0.3mol的单质碘,则转移的电子数目是_____________
③先取少量的加碘盐加蒸馏水溶解,然后加入稀硫酸和KI溶液,最后加入一定量的CCl4,振荡,静置后观察到的现象是_________________________
(2)自来水中的NO3-对人类健康产生危害。为了降低自来水中NO3-的浓度,某研究人员提出在碱性条件下用A粉还原NO3-,发生的反应可表示如下,请配平下列反应方程式:

(3)碘是人体不可缺乏的元素,为了防止碘缺乏,现在市场上流行一种加碘盐,就是在精盐中添加一定量的KIO3进去。某研究小组为了检测某加碘盐中是否含有碘,查阅了有关的资料,发现其检测原理是:

①该反应的氧化剂是
②如果反应生成0.3mol的单质碘,则转移的电子数目是
③先取少量的加碘盐加蒸馏水溶解,然后加入稀硫酸和KI溶液,最后加入一定量的CCl4,振荡,静置后观察到的现象是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】某磁性材料(Fe/Fe3O4)广泛应用于磁记录、催化等领域。一种制备该材料的流程如下:

已知反应原理为:
①Fe2++2OH-=Fe(OH)2
②3Fe(OH)2=Fe+2Fe(OH)3
③Fe(OH)2+2Fe(OH)3=Fe3O4+4H2O
(1)用FeCl2溶液和KOH溶液制备Fe/Fe3O4反应的离子方程式为_______ 。
(2)当pH<2时,Fe/Fe3O4产率极低的原因是_______ 。
(3)图1为回流时间与Fe/Fe3O4产率的关系图,图2为回流1h所得产品的X射线衍射图。回流1h所得产品Fe/Fe3O4中产生杂质可能的原因_______ 。

(4)采用Pd-Fe3O4双催化剂,可实现用H2消除酸性废水中的NO 和NO
和NO ,反应历程如图3所示。
,反应历程如图3所示。

其中Fe3O4中Fe2+和Fe3+分别用Fe(II)、Fe(III)表示。
①用该法处理废水后,溶液的pH_______ 。(填“降低”“升高”或“不变”)
②写出过程④反应的离子方程式_______ 。
③反应历程中虚线方框内NO 生成N2的过程可描述为
生成N2的过程可描述为_______ 。

已知反应原理为:
①Fe2++2OH-=Fe(OH)2
②3Fe(OH)2=Fe+2Fe(OH)3
③Fe(OH)2+2Fe(OH)3=Fe3O4+4H2O
(1)用FeCl2溶液和KOH溶液制备Fe/Fe3O4反应的离子方程式为
(2)当pH<2时,Fe/Fe3O4产率极低的原因是
(3)图1为回流时间与Fe/Fe3O4产率的关系图,图2为回流1h所得产品的X射线衍射图。回流1h所得产品Fe/Fe3O4中产生杂质可能的原因

(4)采用Pd-Fe3O4双催化剂,可实现用H2消除酸性废水中的NO
 和NO
和NO ,反应历程如图3所示。
,反应历程如图3所示。
其中Fe3O4中Fe2+和Fe3+分别用Fe(II)、Fe(III)表示。
①用该法处理废水后,溶液的pH
②写出过程④反应的离子方程式
③反应历程中虚线方框内NO
 生成N2的过程可描述为
生成N2的过程可描述为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】回答下列有关氧化还原的问题。
(1)下列微粒:①S ②S2-③Fe2+ ④H+ ⑤Cu ⑥HCl ⑦H2O。在化学反应中只能被氧化的是_______ (填序号,下同),只能表现出氧化性的是_______ 。
(2)将NaHSO3溶液滴加到酸性KMnO4溶液混合,溶液由紫色褪至无色。反应结束后,推测硫元素在反应后的化合价是_______ ,这样推测的理由是_______ 。
(3)自来水中的NO 对人类健康产生危害。为了降低自来水中NO
对人类健康产生危害。为了降低自来水中NO 的浓度,某研究人员提出两种方案:
的浓度,某研究人员提出两种方案:
①方案a:碱性条件下用Fe(OH)2 还原NO ,产物为NH3。生成1个NH3分子的同时会生成
,产物为NH3。生成1个NH3分子的同时会生成_______ 个Fe(OH)3。
②方案b:碱性条件下用Al粉还原NO ,产物是N2.发生的反应可表示如下,完成方程式配平并用单线桥标出电子转移的方向和数目
,产物是N2.发生的反应可表示如下,完成方程式配平并用单线桥标出电子转移的方向和数目_______ 。
_______Al+_______NO +_______OH-——_______AlO
+_______OH-——_______AlO +_______N2↑+_______H2O
+_______N2↑+_______H2O
(4)设计实验验证亚硫酸钠具有还原性。

试剂a:_______ 现象:_______ 。
(5)已知铜和浓硫酸可以在加热条件下发生如下反应(反应方程式已配平):2H2SO4(浓)+Cu CuSO4+A+2H2O。试通过计算和推理完成下面的问题:
CuSO4+A+2H2O。试通过计算和推理完成下面的问题:
①A物质可以导致酸雨的形成。A应该属于_______ (用字母代号填写)。
a.酸 b.碱 c.盐 d.酸性氧化物 e.碱性氧化物
②A物质可以使酸性KMnO4溶液褪色,写出反应的离子方程式_______ 。此反应中每个A分子_______ (填“得到”或“失去”)_______ 个电子,为_______ (填“氧化剂”或“还原剂”)。
(1)下列微粒:①S ②S2-③Fe2+ ④H+ ⑤Cu ⑥HCl ⑦H2O。在化学反应中只能被氧化的是
(2)将NaHSO3溶液滴加到酸性KMnO4溶液混合,溶液由紫色褪至无色。反应结束后,推测硫元素在反应后的化合价是
(3)自来水中的NO
 对人类健康产生危害。为了降低自来水中NO
对人类健康产生危害。为了降低自来水中NO 的浓度,某研究人员提出两种方案:
的浓度,某研究人员提出两种方案:①方案a:碱性条件下用Fe(OH)2 还原NO
 ,产物为NH3。生成1个NH3分子的同时会生成
,产物为NH3。生成1个NH3分子的同时会生成②方案b:碱性条件下用Al粉还原NO
 ,产物是N2.发生的反应可表示如下,完成方程式配平并用单线桥标出电子转移的方向和数目
,产物是N2.发生的反应可表示如下,完成方程式配平并用单线桥标出电子转移的方向和数目_______Al+_______NO
 +_______OH-——_______AlO
+_______OH-——_______AlO +_______N2↑+_______H2O
+_______N2↑+_______H2O(4)设计实验验证亚硫酸钠具有还原性。

试剂a:
(5)已知铜和浓硫酸可以在加热条件下发生如下反应(反应方程式已配平):2H2SO4(浓)+Cu
 CuSO4+A+2H2O。试通过计算和推理完成下面的问题:
CuSO4+A+2H2O。试通过计算和推理完成下面的问题:①A物质可以导致酸雨的形成。A应该属于
a.酸 b.碱 c.盐 d.酸性氧化物 e.碱性氧化物
②A物质可以使酸性KMnO4溶液褪色,写出反应的离子方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】硫元素是动植物生长不可缺少的元素,图1是自然界中硫元素的存在示意图。图2是硫元素的常见化合价与部分物质类别的对应关系,回答下列问题。
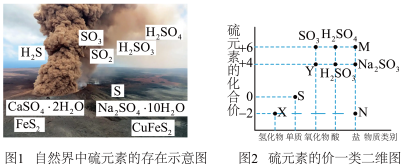
(1)图1中与图2中M、N对应的物质分别是_______ 、_______ 。
(2)X与Y反应中氧化剂与还原剂的物质的量之比为_______ 。
(3)Na2SO3溶液易变质,实验室检验Na2SO3溶液是否变质的基本操作是_______ 。
(4)SO2和氯水都有漂白性,有人为增强漂白效果,将Cl2和SO2混合使用,结果适得其反,几乎没有漂白效果,用离子方程式表示其原因:_______ 。
(5)硫酸是用途广泛的化工原料,可作脱水剂、吸水剂、氧化剂和催化剂等。甲、乙两位同学用铜和硫酸做原料,设计了两种制取硫酸铜的方案。
方案甲:铜与浓硫酸加热直接反应,即Cu→CuSO4
方案乙:由Cu→CuO→CuSO4
①方案甲,中铜和浓硫酸反应的化学方程式是_______ 。该反应体现了浓硫酸的_______ 性。
②这两种方案,你认为哪一种方案更合理?_______ 。理由是_______

(1)图1中与图2中M、N对应的物质分别是
(2)X与Y反应中氧化剂与还原剂的物质的量之比为
(3)Na2SO3溶液易变质,实验室检验Na2SO3溶液是否变质的基本操作是
(4)SO2和氯水都有漂白性,有人为增强漂白效果,将Cl2和SO2混合使用,结果适得其反,几乎没有漂白效果,用离子方程式表示其原因:
(5)硫酸是用途广泛的化工原料,可作脱水剂、吸水剂、氧化剂和催化剂等。甲、乙两位同学用铜和硫酸做原料,设计了两种制取硫酸铜的方案。
方案甲:铜与浓硫酸加热直接反应,即Cu→CuSO4
方案乙:由Cu→CuO→CuSO4
①方案甲,中铜和浓硫酸反应的化学方程式是
②这两种方案,你认为哪一种方案更合理?
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】化合价和物质类别是梳理元素及其化合物知识的两个线索,可表示为“价类”二维图。下图是硫元素的“价类”二维图。
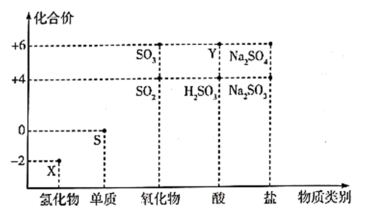
(1)X是___ (填化学式)。
(2)可选取Y的浓溶液和 反应来制备
反应来制备 ,该反应原理是
,该反应原理是___ (填化学方程式);将 排入大气中会引起
排入大气中会引起____ 。
(3) 是一种食品添加剂,其应与图中
是一种食品添加剂,其应与图中___ (填化学式)在同一位置,其具有____ (填“氧化性”或“还原性”)导致 中不可避免地存在
中不可避免地存在 。实验室中检验
。实验室中检验 的常用方法是
的常用方法是____ 。
(4)硫元素还有一种常见的价态-1价,如硫铁矿(主要成分为 )中的硫元素。
)中的硫元素。 可以与
可以与 溶液发生反应:
溶液发生反应: 。
。
①该反应中的氧化剂是____ (填化学式)。
②向反应后的溶液中通入空气就能使 溶液再生,写出再生反应的离子方程式:
溶液再生,写出再生反应的离子方程式:____ 。

(1)X是
(2)可选取Y的浓溶液和
 反应来制备
反应来制备 ,该反应原理是
,该反应原理是 排入大气中会引起
排入大气中会引起(3)
 是一种食品添加剂,其应与图中
是一种食品添加剂,其应与图中 中不可避免地存在
中不可避免地存在 。实验室中检验
。实验室中检验 的常用方法是
的常用方法是(4)硫元素还有一种常见的价态-1价,如硫铁矿(主要成分为
 )中的硫元素。
)中的硫元素。 可以与
可以与 溶液发生反应:
溶液发生反应: 。
。①该反应中的氧化剂是
②向反应后的溶液中通入空气就能使
 溶液再生,写出再生反应的离子方程式:
溶液再生,写出再生反应的离子方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】氮氧化合物和二氧化硫是引起雾霾重要物质,工业用多种方法来治理。某种综合处理含NH 废水和工业废气(主要含NO、CO、CO2、SO2、N2)的流程如图:
废水和工业废气(主要含NO、CO、CO2、SO2、N2)的流程如图:
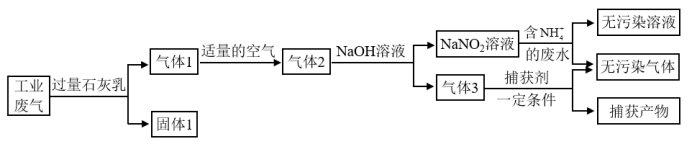
已知: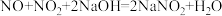 、
、
(1)NO在空气中很容易被氧化成NO2,NO2能与水发生化学反应,写出NO2与水反应的化学方程式为___ 。
(2)SO2造成的一种常见的环境污染为___ 。
(3)固体1的主要成分有Ca(OH)2、___ 、___ (填化学式)。
(4)用NaNO2溶液处理含NH 废水反应的离子方程式为
废水反应的离子方程式为__ 。
(5)验证废水中NH 已基本除净的方法是
已基本除净的方法是__ (写出操作现象与结论)。
(6)捕获剂捕获的气体主要是__ (填化学式)。
(7)流程中生成的NaNO2因外观和食盐相似,又有咸味,容易使人误食中毒。已知NaNO2能发生如下反应: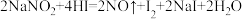 ,I2可以使淀粉溶液变蓝。根据上述反应,选择生活中常见的物质和有关试剂进行实验,以鉴别NaNO2和NaCl固体。需选用的物质是
,I2可以使淀粉溶液变蓝。根据上述反应,选择生活中常见的物质和有关试剂进行实验,以鉴别NaNO2和NaCl固体。需选用的物质是___ (填序号)。
①水②淀粉碘化钾试纸③淀粉④白酒⑤白醋
 废水和工业废气(主要含NO、CO、CO2、SO2、N2)的流程如图:
废水和工业废气(主要含NO、CO、CO2、SO2、N2)的流程如图:
已知:
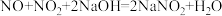 、
、
(1)NO在空气中很容易被氧化成NO2,NO2能与水发生化学反应,写出NO2与水反应的化学方程式为
(2)SO2造成的一种常见的环境污染为
(3)固体1的主要成分有Ca(OH)2、
(4)用NaNO2溶液处理含NH
 废水反应的离子方程式为
废水反应的离子方程式为(5)验证废水中NH
 已基本除净的方法是
已基本除净的方法是(6)捕获剂捕获的气体主要是
(7)流程中生成的NaNO2因外观和食盐相似,又有咸味,容易使人误食中毒。已知NaNO2能发生如下反应:
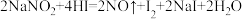 ,I2可以使淀粉溶液变蓝。根据上述反应,选择生活中常见的物质和有关试剂进行实验,以鉴别NaNO2和NaCl固体。需选用的物质是
,I2可以使淀粉溶液变蓝。根据上述反应,选择生活中常见的物质和有关试剂进行实验,以鉴别NaNO2和NaCl固体。需选用的物质是①水②淀粉碘化钾试纸③淀粉④白酒⑤白醋
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】油画的白色燃料中曾含二价铅盐,二价铅盐经过长时间空气(含有微量H2S)的侵蚀,生成PbS而变黑。可用一定量的H2O2溶液擦铁修复。完成下列填空:
(1)H2O2与PbS反应生成PbSO4的和H2O,写出该反应的化学方程式___________ 。
(2)在PbSO4的悬浊液中滴加一定量的CH3COONH4溶液,发生复分解反应,溶液变为澄清,有弱电解质生成,该弱电解质的化学式为___________ 。当PbSO4和CH3COONH4恰好完全反应时,溶液显___________ 性(选填“酸性”、“中性”或“碱性”)。
(3)H2S为二元弱酸,向Na2S溶液中加入FeSO4溶液,生成FeS沉淀,还可能生成白色沉淀,其化学式为___________ ;该物质在空气中很快变为红褐色,原因是___________ 。
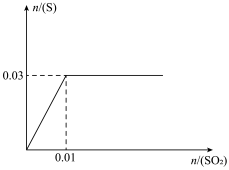
(4)向200mLH2S溶液中缓慢通入SO2,发生反应2H2S+SO2→3S +2H2O,生成S的物质的量与通入SO2的物质的量的关系如图(溶液体积变化忽略不计),由此可知原溶液中H2S的物质的量浓度为
+2H2O,生成S的物质的量与通入SO2的物质的量的关系如图(溶液体积变化忽略不计),由此可知原溶液中H2S的物质的量浓度为___________ 。从开始通SO2至饱和,再继续通一段时间,整个过程中c(H+)的变化情况为___________ 。
(1)H2O2与PbS反应生成PbSO4的和H2O,写出该反应的化学方程式
(2)在PbSO4的悬浊液中滴加一定量的CH3COONH4溶液,发生复分解反应,溶液变为澄清,有弱电解质生成,该弱电解质的化学式为
(3)H2S为二元弱酸,向Na2S溶液中加入FeSO4溶液,生成FeS沉淀,还可能生成白色沉淀,其化学式为
(4)向200mLH2S溶液中缓慢通入SO2,发生反应2H2S+SO2→3S
 +2H2O,生成S的物质的量与通入SO2的物质的量的关系如图(溶液体积变化忽略不计),由此可知原溶液中H2S的物质的量浓度为
+2H2O,生成S的物质的量与通入SO2的物质的量的关系如图(溶液体积变化忽略不计),由此可知原溶液中H2S的物质的量浓度为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】(硫、氮是重要的非金属元素,请根据它们的性质回答下列问题。
I.“价—类”二维图是学习元素及其化合物知识的重要模型。下图为硫及其化合物的“价—类”二维图。
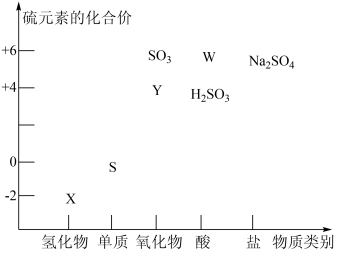
(1)图中X、Y的化学式分别为_______ 、_______ 。
(2)将Y通入如下图装置A中,A中盛有X的水溶液,观察到装置A中有淡黄色固体生成,则发生反应的化学方程式为_______ ,该反应中氧化产物与还原产物的质量比为_______ 。
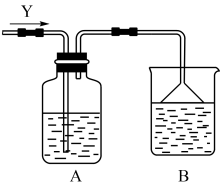
(3)在加热条件下,W的浓溶液能与铜发生反应,则反应的化学方程式为_______ 。
(4) 是重要的化工原料。从氧化还原反应的角度分析,下列制备
是重要的化工原料。从氧化还原反应的角度分析,下列制备 的方案理论上可行的是_______(填字母)。
的方案理论上可行的是_______(填字母)。
II.硝酸是重要的化工原料,用于制化肥、农药、炸药、染料等。工业上制硝酸的原理是将氨经过一系列反应得到硝酸,如下图所示(C为红棕色气体):
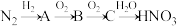
(5)写出上述过程中A到B的化学反应方程式_______ 。
(6)写出上述过程中C到 的化学反应方程式
的化学反应方程式_______ 。
(7)浓硝酸在常温下可与铜反应并生成C气体,该反应的化学方程式为_______ 。稀硝酸在常温下也可与铜反应并生成B气体。一定浓度的硝酸与铜反应,得到物质的量之比为1:1的B和C的混合气体2.24L(标况下),则溶解的Cu的质量是_______ g。
I.“价—类”二维图是学习元素及其化合物知识的重要模型。下图为硫及其化合物的“价—类”二维图。

(1)图中X、Y的化学式分别为
(2)将Y通入如下图装置A中,A中盛有X的水溶液,观察到装置A中有淡黄色固体生成,则发生反应的化学方程式为

(3)在加热条件下,W的浓溶液能与铜发生反应,则反应的化学方程式为
(4)
 是重要的化工原料。从氧化还原反应的角度分析,下列制备
是重要的化工原料。从氧化还原反应的角度分析,下列制备 的方案理论上可行的是_______(填字母)。
的方案理论上可行的是_______(填字母)。A. | B. | C.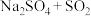 | D. |
II.硝酸是重要的化工原料,用于制化肥、农药、炸药、染料等。工业上制硝酸的原理是将氨经过一系列反应得到硝酸,如下图所示(C为红棕色气体):
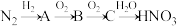
(5)写出上述过程中A到B的化学反应方程式
(6)写出上述过程中C到
 的化学反应方程式
的化学反应方程式(7)浓硝酸在常温下可与铜反应并生成C气体,该反应的化学方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】硫是人类认识最早的元素之一,含硫物质在现代生产和生活中发挥着重要作用。某小组同学验证SO2的性质。装置如图所示,培养皿中A、B、C三个塑料瓶盖内盛有不同物质。向Na2SO3固体上滴加70%硫酸,迅速用玻璃片将培养皿盖严,实验记录如下。
已知:Na2SO3+H2SO4=Na2SO4+SO2↑+H2O
(1)瓶盖___ (填字母)中的实验现象能证明SO2具有还原性,并写出反应的离子方程式___ 。
(2)瓶盖B中的现象证明SO2具有的性质是___ ;瓶盖C中发生反应的化学方程式为___ 。
(3)瓶盖C中无明显变化,若要证明C中发生了化学反应,可先在蒸馏水中滴入少量试剂X,X是___ (填字母)。
a.石蕊溶液 b.NaCl溶液
(4)将SO2气体通入H2S的水溶液中,生成淡黄色的浑浊,证明SO2具有的性质是___ ;写出反应的化学方程式___ 。
| 实验装置 | 瓶盖 | 物质 | 实验现象 |
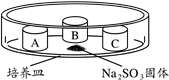 | A | KMnO4酸性溶液 | 溶液褪色 |
| B | 蘸有品红溶液的棉花 | 品红溶液褪色 | |
| C | 蒸馏水 | 无明显变化 |
已知:Na2SO3+H2SO4=Na2SO4+SO2↑+H2O
(1)瓶盖
(2)瓶盖B中的现象证明SO2具有的性质是
(3)瓶盖C中无明显变化,若要证明C中发生了化学反应,可先在蒸馏水中滴入少量试剂X,X是
a.石蕊溶液 b.NaCl溶液
(4)将SO2气体通入H2S的水溶液中,生成淡黄色的浑浊,证明SO2具有的性质是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】在化学课上,围绕浓硫酸的化学性质进行了如下实验探究:将适量的蔗糖放入烧杯中,加入几滴水,搅拌均匀。然后加入适量浓硫酸,迅速搅拌,放出大量的热,同时观察到蔗糖逐渐变黑,体积膨胀,并放出有刺激性气味的气体。请回答:
(1)生成的黑色物质是_________ (填化学式)。
(2)刺激性气味的气体主要成分是___________ (填化学式),产生该气体的化学方程式为__________ 。
(3)根据上述实验现象,表明浓硫酸具有________ (填序号)。
①酸性 ②吸水性 ③脱水性 ④强氧化性
(1)生成的黑色物质是
(2)刺激性气味的气体主要成分是
(3)根据上述实验现象,表明浓硫酸具有
①酸性 ②吸水性 ③脱水性 ④强氧化性
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】物质的类别和核心元素的化合价是研究物质性质的两个重要角度。如图所示是硫及其部分化合物的“价类二维图”,回答下列问题:

(1)X的电子式为_______ 。
(2)B物质的用途_______ 。(写一种)
(3)铜单质和D的浓溶液在加热条件下可以少量制取B,写出该反应的化学方程式:_______ 。
(4)欲制备Na2S2O3,从氧化还原角度分析,下列选项中合理的是_______(填字母)。
(5)将X的溶液与B混合,可生成淡黄色固体,写出该反应的化学方程式并用双线桥表示该过程中转移的电子数:_______ 。
(6)某地收集的雨水样品在不同时间测得pH如表所示,根据价类二维图分析该雨水样品随时间变化酸性逐渐增强的原因:_______ 。

(1)X的电子式为
(2)B物质的用途
(3)铜单质和D的浓溶液在加热条件下可以少量制取B,写出该反应的化学方程式:
(4)欲制备Na2S2O3,从氧化还原角度分析,下列选项中合理的是_______(填字母)。
| A.Na2S+S | B.Na2SO3+S | C.Na2SO3+Na2SO4 | D.SO2+Na2SO4 |
(6)某地收集的雨水样品在不同时间测得pH如表所示,根据价类二维图分析该雨水样品随时间变化酸性逐渐增强的原因:
| 时间/h | 0 | 2 | 4 | 6 | 8 | 10 |
| pH | 5.0 | 4.8 | 4.5 | 4.3 | 4.2 | 4.0 |
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】(1)利用如图装置除去下列气体中的杂质气体,若要除去NO中混有的少量NO2,洗气瓶中应装_______ ;化学方程式为_______ 。若要除去SO2中混有的少量SO3气体,洗气瓶中装试剂为:_______ ,化学方程式为_______ 。
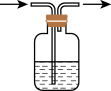
(2)加热的浓硫酸与木炭反应:_______ 。其中氧化剂是_______ (写化学式),还原产物是_______ (写化学式)。
(3)稀硝酸与铜片的反应:_______ ,若有2molHNO3被还原,则有_______ mol电子转移。
(4)请用方程式解释为什么盛装烧碱溶液试剂瓶的塞子不能用玻璃塞:_______ 写出用HF雕刻玻璃时发生的化学反应方程式_______

(2)加热的浓硫酸与木炭反应:
(3)稀硝酸与铜片的反应:
(4)请用方程式解释为什么盛装烧碱溶液试剂瓶的塞子不能用玻璃塞:
您最近一年使用:0次



