能用元素周期律解释的是
| A.酸性:HI>HF | B.碱性:NaOH>Mg(OH)2 |
| C.稳定性:CH4>H2S | D.氧化性:FeCl3> CuCl2 |
更新时间:2019/04/03 14:47:59
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】下列各组中的性质比较,正确的是
①酸性:HClO4>HBrO4>HIO4 ②碱性:Ba(OH)2>Ca(OH)2>Mg(OH)2
③还原性:F— >C1— >Br— ④稳定性:HCl>H2S>PH3
⑤熔沸点:AsH3 >PH3 >NH3
①酸性:HClO4>HBrO4>HIO4 ②碱性:Ba(OH)2>Ca(OH)2>Mg(OH)2
③还原性:F— >C1— >Br— ④稳定性:HCl>H2S>PH3
⑤熔沸点:AsH3 >PH3 >NH3
| A.①②④ | B.①②③ | C.②③④ | D.①②④⑤ |
您最近一年使用:0次
单选题-单题
|
适中
(0.65)
名校
【推荐2】 、
、 、
、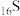 、
、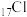 是周期表中的短周期主族元素。下列有关说法正确的是
是周期表中的短周期主族元素。下列有关说法正确的是
 、
、 、
、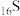 、
、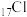 是周期表中的短周期主族元素。下列有关说法正确的是
是周期表中的短周期主族元素。下列有关说法正确的是A.键角: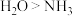 | B.第一电离能: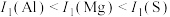 |
C.碱性: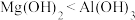 | D.半径: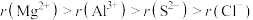 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
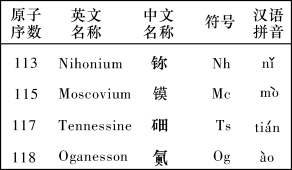
【推荐1】元素周期表的形式多种多样,如图是扇形元素周期表的一部分(字母①~⑩为前36号元素)。对比中学常见元素周期表,思考扇形元素周期表的填充规律,下列说法中正确的是


| A.②⑧⑨对应简单离子的半径依次减小 |
| B.⑥的金属性比⑦的弱 |
| C.元素⑩位于常见元素周期表第四周期VIII族 |
| D.①分别与③④⑤形成的简单化合物热稳定性依次减弱 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】短周期元素X、Y、Z、W、Q在元素周期表中的相对位置如图所示。下列说法不正确的是
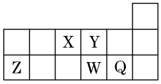
| A.W、Y对应的简单氢化物的稳定性前者高 |
| B.阴离子的还原性:W2﹣>Q﹣ |
| C.离子半径:Y2﹣>Z3+ |
| D.元素的非金属性:Y>W |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】我国新报道的高温超导材料中,铊(Tl)是其中重要的组成成分之一。已知铊与铝同主族,且位于元素周期表的第六周期,则下列关于铊的叙述错误 的是( )
| A.铊元素的原子半径大于铝元素的原子半径 |
| B.铊原子核内质子数为81 |
| C.铊的最高价氧化物对应的水化物为Tl(OH)3 |
| D.铊在空气中表面不易被氧化 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】下列元素中金属性最弱的是
| A.Cu | B.Na | C.Al | D.Mg |
您最近一年使用:0次
【推荐2】根据实验目的设计方案并进行实验,观察到相关现象,下列方案设计、结论均正确的是
| 实验目的 | 方案设计 | 现象 | 结论 | |
| A | 探究金属Na、Ca的金属性强弱 | 将金属Na、Ca分别切成体积相等的颗粒,投入蒸馏水中 | 金属Na与水反应更加剧烈 | Na的金属性强于Ca |
| B | 判断AlCl3的化学键类型 | 将AlCl3固体溶于水,进行导电性实验 | AlCl3溶液可导电 | AlCl3中含有离子键 |
| C | 探究浓硝酸与炭在加热条件下能否反应 | 将红热的木炭投入浓硝酸中 | 产生红棕色气体 | 炭与浓硝酸在加热条件下反应生成NO2 |
| D | 探究有机物中官能团之间的影响 | 分别向丙烯酸乙酯(CH2=CHCOOCH2CH3)和α-氰基丙烯酸乙酯[CH2=C(CN)COOCH2CH3]中滴入水 | 前者无明显现象,后者快速固化 | 氰基活化双键,使其更易发生加聚反应 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】某种由六种元素形成的抗癌药物的结构简式如下图所示,其中 W、X、Y、Z 是原子序数依次增大的短周期主族元素,W、Y 同主族,Y、Z 的最外层电子数之和是 X 的最外层电子数的 2 倍。下列叙述错误的是


| A.X、Y、Z 三种元素中,电负性最大的元素为 Y |
| B.W、X、Y 三种元素对应的最简单氢化物的热稳定性:Y<W<X |
| C.W 与 Z 的最简单氢化物混合后可产生白烟 |
| D.X 的一种单质和化合物 ZX2均可用于自来水消毒 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】甲乙两种非金属性质比较:①甲比乙在相同条件下更容易与氢气化合;②甲单质能与乙的阴离子发生置换反应;③最高价氧化物对应的水化物酸性比较,甲比乙的强;④与一定量的金属反应时甲原子得电子数目比乙的多;⑤甲的单质熔、沸点比乙的低,能够说明甲比乙的非金属性强的是
| A.①③④ | B.①②③ | C.①②⑤ | D.①②③④⑤ |
您最近一年使用:0次

 比1molB从酸中置换生成的
比1molB从酸中置换生成的 的单质可用于饮用水消毒。由
的单质可用于饮用水消毒。由 组成的某化合物结构如图,分子中所有原子均达到8电子稳定结构。下列说法正确的是
组成的某化合物结构如图,分子中所有原子均达到8电子稳定结构。下列说法正确的是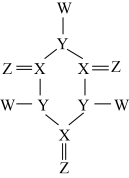
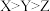
 的单质在自然界中不存在
的单质在自然界中不存在


