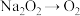用CuS、Cu2S处理酸性废水中的Cr2O72-,发生反应如下:
反应Ⅰ:CuS+Cr2O72-+H+→Cu2++SO42-+Cr3++H2O(未配平)
反应Ⅱ:Cu2S+Cr2O72-+H+→Cu2++SO42-+Cr3++H2O(未配平)
下列有关说法正确的是
反应Ⅰ:CuS+Cr2O72-+H+→Cu2++SO42-+Cr3++H2O(未配平)
反应Ⅱ:Cu2S+Cr2O72-+H+→Cu2++SO42-+Cr3++H2O(未配平)
下列有关说法正确的是
| A.反应Ⅰ和Ⅱ中Cu2+、SO42-都是氧化产物 |
| B.处理1mol Cr2O72-时反应Ⅰ、Ⅱ中消耗H+的物质的量相等 |
| C.反应Ⅱ中还原剂、氧化剂的物质的量之比为3:5 |
| D.反应Ⅰ、Ⅱ中每处理1mol Cr2O72-,转移电子数不相等 |
更新时间:2019-04-15 10:49:53
|
相似题推荐
【推荐1】唐代孙思邈的《伏硫磺法》中就记载了类似“一硫二硝三木炭”的黑火药配方。发生反应的化学方程式为:2KNO3+3C+S=N2↑+3CO2↑+K2S。下列说法错误的是
| A.氧化剂:KNO3和S |
| B.上述反应中,每生成1molN2转移电子10NA |
| C.氧化产物与还原产物的物质的量之比为3∶2 |
| D.消耗32g单质硫,产生89.6L(标况下)气体 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】聚合硫酸铁可用于水的净化,其化学式可表示为[Fea(OH)b(SO4)c]m。取一定量聚合硫酸铁样品与足量盐酸反应,将所得溶液平均分为两份。向一份溶液中加入足量的BaCl2溶液,得到白色沉淀1.7475 g。取另一份溶液,先将Fe3+还原为Fe2+(还原剂不是Fe,且加入的还原剂恰好将Fe3+还原为Fe2+),再用0.020 00 mol/LK2Cr2O7标准溶液滴定至终点,消耗K2Cr2O7标准溶液50.00 mL。该聚合硫酸铁样品中a∶b为
| A.1∶1 | B.2∶1 | C.3∶1 | D.2∶5 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】下列应用不涉及氧化还原反应的是
| A.“84”消毒液用于杀灭新型冠状病毒 | B.小苏打用作食品膨松剂 |
| C.过氧化钠用作潜艇供氧剂 | D.铁粉用作食品包装脱氧剂 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列对古诗词描述的场景分析有误的是
| A.梅花香自苦寒来——说明分子在不停地运动 |
| B.烈火焚烧若等闲——焚烧石灰石属于化合反应 |
| C.蜡炬成灰泪始干——涉及氧化还原反应 |
| D.白云深处有入家——“白云”是一种气溶胶 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】下列关于氧化还原反应的说法正确的是
| A.阴离子只有还原性,没有氧化性 |
| B.氧化还原反应的本质是元素化合价的升降 |
| C.有单质参与的化学反应一定是氧化还原反应 |
| D.氧化还原反应中,得失电子的元素可以为同一种元素 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】电石(成分为CaC2)中常含有硫化物,在反应时常产生有毒气体。工业上利用如下流程除去电石渣浆(含CaO)上层清液中的S2−,并制取石膏CaSO4•2 H2O。

下列说法正确的是

下列说法正确的是
| A.过程Ⅰ中的反应会使溶液的碱性增强 |
B.过程Ⅱ的离子方程式为4MnO +2S2−+10H+=4Mn(OH)2+S2O +2S2−+10H+=4Mn(OH)2+S2O +H2O +H2O |
C.将上层清液中0.1mol的S2−转化为SO ,理论上共需要0.2mol的O2 ,理论上共需要0.2mol的O2 |
D.由上述转化过程可知,氧化性:MnO >O2>S2O >O2>S2O |
您最近一年使用:0次