前20号元素的常见化合价与原子半径的关系图(用化学符号作答)

(1)A:_____ B:____ C:_____ D:_____ E:_____ F:_____
(2)A、B、C三种元素组成的碱为___________ ,盐为__________
(3)B、C、E三种元素的简单离子半径由大到小的顺序为______________

(1)A:
(2)A、B、C三种元素组成的碱为
(3)B、C、E三种元素的简单离子半径由大到小的顺序为
更新时间:2019/04/16 15:51:48
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
名校
【推荐1】元素在周期表中的位置、原子结构、元素的性质三者之间关系密切。根据下列短周期主族元素的原子结构特点,回答下列问题:
(1)最外层电子数是核外电子总数的 的非金属元素是
的非金属元素是_______ (填元素符号或化学式,下同)。
(2)周期序数与主族序数相等的金属元素有_______ 。
(3)最外层电子数是电子层数3倍的元素形成的双原子分子为_______ 。
(4)主族序数是电子层数的2倍且具有8个中子的核素为_______ 。
(5)K层和M层电子数相等的元素与氮元素形成的化合物为_______ 。
(1)最外层电子数是核外电子总数的
 的非金属元素是
的非金属元素是(2)周期序数与主族序数相等的金属元素有
(3)最外层电子数是电子层数3倍的元素形成的双原子分子为
(4)主族序数是电子层数的2倍且具有8个中子的核素为
(5)K层和M层电子数相等的元素与氮元素形成的化合物为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐2】A、B、C、D、E、F是原子序数依次增大的6种短周期元素,A元素原子的2p原子轨道上有2个未成对的电子,B元素在同周期元素中原子半径最大,与A可形成原子个数比为1:1和2:1的两种化合物,C单质是一种常见的半导体材料,F有9个原子轨道,且只有一个未成对电子,没有空轨道。
(1)C元素在元素周期表中的位置_______
(2)EF2中心原子杂化轨道类型为_______ 杂化,VSEPR模型为_______ ,空间结构为_______
(3)P4S3可用于制造火柴,其分子结构如图所示。

①P4S3分子中硫原子的杂化轨道类型为_______ 。
②每个P4S3分子中含孤电子对的数目为_______ 。
③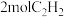 分子中含有
分子中含有_______  键
键
(1)C元素在元素周期表中的位置
(2)EF2中心原子杂化轨道类型为
(3)P4S3可用于制造火柴,其分子结构如图所示。

①P4S3分子中硫原子的杂化轨道类型为
②每个P4S3分子中含孤电子对的数目为
③
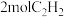 分子中含有
分子中含有 键
键
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐3】A、B、C、D四种短周期元素,原子序数依次增大,A原子的最外层上有4个电子;B的阴离子和C的阳离子具有相同的电子层结构,B与C的单质在加热条件下反应,生成一种淡黄色的固体E;D的L层电子数等于K、M两个电子层上的电子数之和
(1)写元素符号:A为______ ,C为______ ,D的最高价氧化物的水化物化学式是______ 。
(2)写出A、B形成的化合物与E反应的化学方程式:______
(3)E属于______ (“离子”或“共价”)化合物。
(4)C与D两元素可形成化合物______ 。
(1)写元素符号:A为
(2)写出A、B形成的化合物与E反应的化学方程式:
(3)E属于
(4)C与D两元素可形成化合物
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐1】X、Y、Z、R、W为五种短周期元素。X原子最外层电子数是核外电子层数的3倍;Y最高正价与最低负价代数和为4;Z的单质常用于漂白工业;R是短周期元素中金属性最强的元素,W是生活中的常见金属,其氧化物常做耐高温材料。回答下列问题:
(1)Y元素的名称______ ,在周期表中的位于第三周期__________ 族
(2)W与Z单质化合得到的物质属于__________ 化合物(选填“离子”或“共价”),向其溶液中加入足量NaOH溶液,反应的离子方程式为______ 。
(3)工业上常用W单质与氨气在1700℃发生置换反应,生成一种最轻的气体和一种坚硬耐磨的固体,试写出该反应的化学方程式_________________________ 。
(4)化合物甲由元素X、R组成,甲能与水剧烈反应,并产生大量气泡,写出其化学反应方程式______ ,甲的电子式为_____________ 。
(5)为比较元素X和Y的非金属性强弱,下列方法不可行的是___ 。
a.比较这两种元素的常见单质的沸点
b.比较这两种元素的单质与氢气化合的难易
c.比较这两种元素的气态氢化物的稳定性
(1)Y元素的名称
(2)W与Z单质化合得到的物质属于
(3)工业上常用W单质与氨气在1700℃发生置换反应,生成一种最轻的气体和一种坚硬耐磨的固体,试写出该反应的化学方程式
(4)化合物甲由元素X、R组成,甲能与水剧烈反应,并产生大量气泡,写出其化学反应方程式
(5)为比较元素X和Y的非金属性强弱,下列方法不可行的是
a.比较这两种元素的常见单质的沸点
b.比较这两种元素的单质与氢气化合的难易
c.比较这两种元素的气态氢化物的稳定性
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐2】有A、B、C、D、E五种短周期元素,其元素特征信息如下表。
回答下列问题。
(1)写出下列元素的名称:C_______ ,E_______ 。
(2)写出A、B、C形成的化合物的化学式_______ 。
(3)B、C、D的简单离子半径由大到小的顺序是_______ (用化学式表示)。
(4)①写出E单质与A、B、C形成的化合物反应的化学方程式:_______ 。
②写出D单质与A、B、C形成的化合物的水溶液反应的离子方程式:_______ 。
| 元素编号 | 元素特征信息 |
| A | 其单质是密度最小的物质 |
| B | 阴离子带两个单位负电荷,单质是空气的主要成分之一 |
| C | 其阳离子与B的阴离子有相同的电子层结构,且与B 可以形成两种氧化物 |
| D | 其氢氧化物和氧化物都有两性,与C同周期 |
| E | 与C同周期,原子半径在该周期中最小 |
(1)写出下列元素的名称:C
(2)写出A、B、C形成的化合物的化学式
(3)B、C、D的简单离子半径由大到小的顺序是
(4)①写出E单质与A、B、C形成的化合物反应的化学方程式:
②写出D单质与A、B、C形成的化合物的水溶液反应的离子方程式:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐3】A、D、E、W是中学常见的四种元素,原子序数依次增大,A的原子最外层电子数是次外层的2倍,D的氧化物属于两性氧化物,D、E位于同周期,A、D、E的原子最外层电子数之和为14,W是人体必需的微量元素,缺乏W会导致贫血症状。
(1)W在元素周期表中的位置是___ 。A与E组成的化合物是常用的溶剂,写出其电子式___ 。
(2)下列事实能用元素周期表相应规律解释的是(填字母序号)___ 。
a.D的最高价氧化物对应水化物的碱性弱于Mg(OH)2
b.E的气态氢化物的稳定性小于HF
c.A的单质能与二氧化硅高温下制得粗品硅单质
(3)WE3的溶液可用于刻蚀铜制的印刷电路板,反应的离子方程式为____ 。
(4)①工业上用电解法制备D的单质,反应的化学方程式为___ 。
②家用“管道通”的有效成分是烧碱和D的单质,使用时需加入一定量的水,此时发生反应的化学方程式为____ 。
(5)W的单质可用于处理酸性废水中的NO3-,使其转换为NH4+,同时生成有磁性的W的氧化物X,再进行后续处理,上述反应的离子方程式为__ 。上述W的氧化物X能与D的单质反应,写出该反应的化学方程式为__ 。
(1)W在元素周期表中的位置是
(2)下列事实能用元素周期表相应规律解释的是(填字母序号)
a.D的最高价氧化物对应水化物的碱性弱于Mg(OH)2
b.E的气态氢化物的稳定性小于HF
c.A的单质能与二氧化硅高温下制得粗品硅单质
(3)WE3的溶液可用于刻蚀铜制的印刷电路板,反应的离子方程式为
(4)①工业上用电解法制备D的单质,反应的化学方程式为
②家用“管道通”的有效成分是烧碱和D的单质,使用时需加入一定量的水,此时发生反应的化学方程式为
(5)W的单质可用于处理酸性废水中的NO3-,使其转换为NH4+,同时生成有磁性的W的氧化物X,再进行后续处理,上述反应的离子方程式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】原子序数小于36的X、Y、Z、R、W五种元素,其中X是周期表中原子半径最小的元素,Y是形成化合物种类最多的元素,Z原子基态时2p原子轨道上有3个未成对的电子,R单质占空气体积的1/5;W的原子序数为29。回答下列问题:
(1)Y2X4分子中Y原子轨道的杂化类型为________ ,1mol Z2X4含有σ键的数目为 ________ 。
(2)化合物ZX3与化合物X2R的VSEPR构型相同,但立体构型不同,ZX3的立体构型为________ ,两种化合物分子中化学键的键角较小的是________ (用分子式表示),其原因是________________________________________________ 。
(3)与R同主族的三种非金属元素与X可形成结构相似的三种物质,三者的沸点由高到低的顺序是________ 。
(4)元素Y的一种氧化物与元素Z的单质互为等电子体,元素Y的这种氧化物的结构式是________ 。
(5)W元素原子的价电子排布式为________ 。
(1)Y2X4分子中Y原子轨道的杂化类型为
(2)化合物ZX3与化合物X2R的VSEPR构型相同,但立体构型不同,ZX3的立体构型为
(3)与R同主族的三种非金属元素与X可形成结构相似的三种物质,三者的沸点由高到低的顺序是
(4)元素Y的一种氧化物与元素Z的单质互为等电子体,元素Y的这种氧化物的结构式是
(5)W元素原子的价电子排布式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】短周期主族元素W、X、Y、Z的原子序数依次增大,W的最简单氢化物甲是一种能使湿润的红色石蕊试纸变蓝的无色气体,常用作制冷剂,Y的金属性是所有短周期主族元素中最强的,Z与X属于同一主族,Z与Y属于同一周期。
(1)元素W在周期表中位置为_______________ 。
(2)元素W的另一常见氢化物乙是一种高能燃料,为18电子微粒,乙的结构式为___________ 。
(3)X、Y、Z的原子半径由小到大的顺序为_________________ 。
(4)若X与Z的最外层电子数之和是W核外电子数的2倍,甲可与Z单质发生置换反应,产物之一可作化肥,其反应的化学方程式为___________________ ,该产物化肥中含有的化学键有________________ 。
(5)若由X、Y和Z三种元素形成的一种盐溶于水后,加入稀盐酸,有黄色沉淀析出,同时有刺激性气味气体产生。则元素Z是______ (填元素符号),反应的离子方程式为________________ 。
(1)元素W在周期表中位置为
(2)元素W的另一常见氢化物乙是一种高能燃料,为18电子微粒,乙的结构式为
(3)X、Y、Z的原子半径由小到大的顺序为
(4)若X与Z的最外层电子数之和是W核外电子数的2倍,甲可与Z单质发生置换反应,产物之一可作化肥,其反应的化学方程式为
(5)若由X、Y和Z三种元素形成的一种盐溶于水后,加入稀盐酸,有黄色沉淀析出,同时有刺激性气味气体产生。则元素Z是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】A、B、C、D四种元素都是短周期元素,A元素的离子具有黄色的焰色反应。A、B元素的离子结构和Ne具有相同的电子层排布;5.8 g B的氢氧化物恰好能与100 mL 2 mol·L—1盐酸完全反应;B原子核中质子数和中子数相等。H2在C单质中燃烧产生苍白色火焰。 C的最高价氧化物的水化物是所有含氧酸中酸性最强的;D元素原子的电子层结构中,最外层电子数是次外层电子数的3倍。根据上述条件回答:
(1)元素C位于第__________周期第__________族,它的最高价氧化物的水化物的化学式为____________。
(2)A元素是_______,B元素是______,D元素是______。(写元素符号)
(3)A与D形成的原子个数比为2:1的化合物的化学式是___ _ ____,
用电子式表示它的形成过程
(4)C元素的单质有毒,可用A的最高价氧化物对应的水化物的溶液吸收,
其离子方程式为______________________________ __________________。
(1)元素C位于第__________周期第__________族,它的最高价氧化物的水化物的化学式为____________。
(2)A元素是_______,B元素是______,D元素是______。(写元素符号)
(3)A与D形成的原子个数比为2:1的化合物的化学式是___ _ ____,
用电子式表示它的形成过程
(4)C元素的单质有毒,可用A的最高价氧化物对应的水化物的溶液吸收,
其离子方程式为______________________________ __________________。
您最近一年使用:0次



