资料在线:查阅资料可知如表所示数据:
[实验步骤]
某学生在实验室制取乙酸乙酯的主要步骤如下:
①在30 mL的大试管A中按体积比1∶4∶4配制浓硫酸、乙醇和乙酸的混合溶液;
②按如图所示连接好装置(装置气密性良好),用小火均匀地加热装有混合溶液的大试管5~10 min;
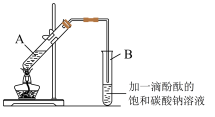
③待试管B收集到一定量的产物后停止加热,撤去试管B并用力振荡,然后静置待分层;
④分离出乙酸乙酯层、洗涤、干燥。
请根据题目要求回答下列问题:
(1)步骤①配制该混合溶液的主要操作步骤为___ ;写出制取乙酸乙酯的化学方程式:___ 。
(2)步骤②中需要小火均匀加热,其主要理由是________ 。
(3)指出步骤③所观察到的现象:________ ;
分离出乙酸乙酯后,为了干燥乙酸乙酯可选用的干燥剂为____ (填字母)。
A.P2O5 B.无水Na2SO4
C.碱石灰 D.NaOH固体
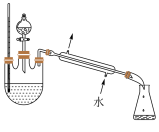
(4)某化学课外小组设计了如图所示的制取乙酸乙酯的装置(图中的铁架台、铁夹、加热装置已略去),与上图装置相比,此装置的主要优点有______ 。
| 物质 | 乙醇 | 乙酸 | 乙酸乙酯 | 浓硫酸 |
| 沸点/℃ | 78.5 | 117.9 | 77.5 | 338.0 |
某学生在实验室制取乙酸乙酯的主要步骤如下:
①在30 mL的大试管A中按体积比1∶4∶4配制浓硫酸、乙醇和乙酸的混合溶液;
②按如图所示连接好装置(装置气密性良好),用小火均匀地加热装有混合溶液的大试管5~10 min;

③待试管B收集到一定量的产物后停止加热,撤去试管B并用力振荡,然后静置待分层;
④分离出乙酸乙酯层、洗涤、干燥。
请根据题目要求回答下列问题:
(1)步骤①配制该混合溶液的主要操作步骤为
(2)步骤②中需要小火均匀加热,其主要理由是
(3)指出步骤③所观察到的现象:
分离出乙酸乙酯后,为了干燥乙酸乙酯可选用的干燥剂为
A.P2O5 B.无水Na2SO4
C.碱石灰 D.NaOH固体
(4)某化学课外小组设计了如图所示的制取乙酸乙酯的装置(图中的铁架台、铁夹、加热装置已略去),与上图装置相比,此装置的主要优点有

2018高二下·全国·专题练习 查看更多[9]
(已下线)2018年5月6日 每周一测——《每日一题》2017-2018学年高二化学人教选修5(已下线)2019年4月17日 《每日一题》选修5——酯化反应实验(已下线)2019年10月28日 《每日一题》2020年高考一轮复习-酯化反应第三节 生活中两种常见的有机物 易错疑难集训(二)——A学习区 夯实基础(人教版必修2)第三节 乙醇 与乙酸 易错疑难集训(二)——A学习区 夯实基础(人教版(2019)第二册)必修第二册RJ第7章易错疑难集训(二)湖南省常德市第一中学2020-2021学年高二上学期期中考试化学试题(已下线)7.3.2 乙酸(练好题)(基础过关)-2020-2021学年高一化学新教材新理念新设计同步课堂(人教2019必修第二册)(已下线)【教材实验热点】11 乙酸乙酯的实验室制取
更新时间:2019-04-18 15:12:21
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】某实验小组利用下图所示装置在实验室欲制备乙酸乙酯。

(1)B装置中,导管口略高于液面的目的是________________________
(2)为了改善反应过程中混合溶液变黑的现象,甲同学采用NaHSO4代替浓硫酸做催化剂(其他试剂及用量不变)来制备乙酸乙酯,NaHSO4可代替浓硫酸做催化剂的原因是__________________________________________________________
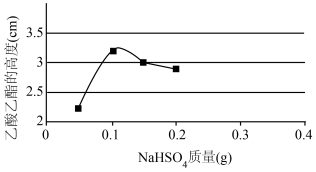
(3)下图是甲同学采用NaHSO4做催化剂,其他条件不变(其中乙酸用量为2 mL)不同质量的NaHSO4来制备乙酸乙酯的催化效果图,其中NaHSO4的质量为_______ g时催化效果最好。
(4)乙同学实验时,在饱和Na2CO3中滴加两滴酚酞,实验结束,取下试管B振荡,红色褪去。为探究褪色的原因,进行如下实验。
a试管①中产生气泡的原因是(用化学方程式解释)____________________________ 。
b对比实验①和②可得出的结论是___________________________________ 。
c针对实验②中现象,乙同学提出猜想:酚酞更易溶于乙酸乙酯。实验③中观察到__________________________________ ,证实乙的猜想正确。

(1)B装置中,导管口略高于液面的目的是
(2)为了改善反应过程中混合溶液变黑的现象,甲同学采用NaHSO4代替浓硫酸做催化剂(其他试剂及用量不变)来制备乙酸乙酯,NaHSO4可代替浓硫酸做催化剂的原因是
(3)下图是甲同学采用NaHSO4做催化剂,其他条件不变(其中乙酸用量为2 mL)不同质量的NaHSO4来制备乙酸乙酯的催化效果图,其中NaHSO4的质量为

(4)乙同学实验时,在饱和Na2CO3中滴加两滴酚酞,实验结束,取下试管B振荡,红色褪去。为探究褪色的原因,进行如下实验。
| 编号 | ① | ② | ③ |
| 实验 | 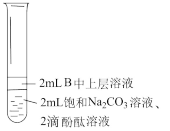 | 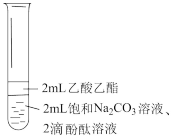 | 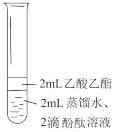 |
| 操作 | 充分振荡、静置 | 充分振荡、静置 | 充分振荡、静置、分液。取下层溶液,加入饱和Na2CO3溶液 |
| 现象 | 上层液体变薄,冒气泡,下层溶液红色褪去 | 上层液体不变薄,无气泡,下层溶液红色褪去 |
b对比实验①和②可得出的结论是
c针对实验②中现象,乙同学提出猜想:酚酞更易溶于乙酸乙酯。实验③中观察到
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐2】某化学小组以苯甲酸( )为原料,制取苯甲酸甲酯,已知有关物质的沸点如表:
)为原料,制取苯甲酸甲酯,已知有关物质的沸点如表:
Ⅰ.合成苯甲酸甲酯粗产品
在圆底烧瓶中加入12.2g苯甲酸和20mL甲醇(密度约为0.79g·cm-3),再小心加入3mL浓硫酸,混匀后,投入几块碎瓷片,小心加热使反应完全,得苯甲酸甲酯粗产品。
(1)浓硫酸的作用是______________ ;写出苯甲酸与甲醇反应的化学方程式:______________ 。
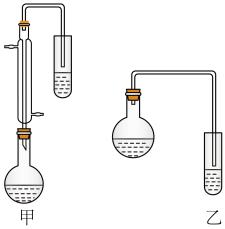
(2)甲和乙两位同学分别设计了如图所示的两套实验室合成苯甲酸甲酯的装置(夹持仪器和加热仪器均已略去)。根据有机物的沸点,最好采用__________ 装置(填“甲”或“乙”)
(3)反应物CH3OH应过量,理由是______________ 。
Ⅱ.粗产品的精制
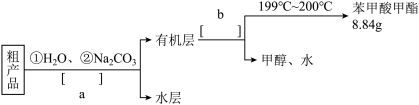
(4)苯甲酸甲酯粗产品中往往含有少量甲醇、苯甲酸和水等,现拟用下列流程图进行精制,请在流程图中方括号内填入操作方法的名称a______________ ,b______________ 。
(5)通过计算,苯甲酸甲酯的产率为______________
 )为原料,制取苯甲酸甲酯,已知有关物质的沸点如表:
)为原料,制取苯甲酸甲酯,已知有关物质的沸点如表:| 物质 | 甲醇 | 苯甲酸 | 苯甲酸甲酯 |
| 沸点/℃ | 64.7 | 249 | 199.6 |
| 密度/g·cm-3 | 0.792 | 1.2659 | 1.0888 |
| 相对分子质量 | 32 | 122 | 136 |
在圆底烧瓶中加入12.2g苯甲酸和20mL甲醇(密度约为0.79g·cm-3),再小心加入3mL浓硫酸,混匀后,投入几块碎瓷片,小心加热使反应完全,得苯甲酸甲酯粗产品。
(1)浓硫酸的作用是
(2)甲和乙两位同学分别设计了如图所示的两套实验室合成苯甲酸甲酯的装置(夹持仪器和加热仪器均已略去)。根据有机物的沸点,最好采用

(3)反应物CH3OH应过量,理由是
Ⅱ.粗产品的精制
(4)苯甲酸甲酯粗产品中往往含有少量甲醇、苯甲酸和水等,现拟用下列流程图进行精制,请在流程图中方括号内填入操作方法的名称a

(5)通过计算,苯甲酸甲酯的产率为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】乙酸正丁酯是一种优良的有机溶剂,广泛用于硝化纤维清漆中,在人造革、织物及塑料加工过程中用作溶剂,也用于香料工业。安徽师范大学附属中学化学兴趣小组在实验室用乙酸和正丁醇制备乙酸正丁酯,有关物质的相关数据及实验装置如下所示:
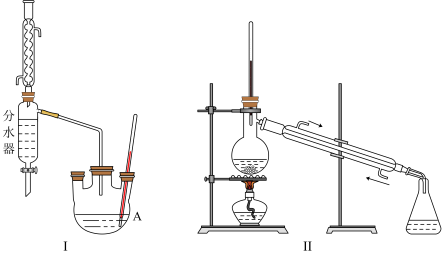
分水器的操作方法:先将分水器装满水(水位与支管口相平),再打开活塞,准确放出一定体积的水。在制备过程中,随着加热回流,蒸发后冷凝下来的有机液体和水在分水器中滞留分层,水并到下层(反应前加入的)水中:有机层从上面溢出,流回反应容器。当水层增至支管口时,停止反应。
乙酸正丁酯合成和提纯步骤为:
第一步:取18.5 ml正丁醇和14.4 ml冰醋酸混合加热发生酯化反应,反应装置如图I所示(加热仪器已省略):
第二步:依次用水、饱和Na2CO3溶液、水对三颈烧瓶中的产品洗涤并干燥;
第三步:用装置II蒸馏提纯。
请回答有关问题:
(1)第一步装置中除了加正丁醇和冰醋酸外,还需加入__________ 、___________ 。
(2)仪器A中发生反应的化学方程为___________________________________ 。根据题中给出的相关数据计算,理论上,应该从分水器中放出来的水的体积约________ 。
(3)第二步用饱和Na2CO3溶液洗涤的目的是____________________________ 。
(4)第三步蒸馏产品时,若实验中得到乙酸正丁酯13.92 g,则乙酸正丁酯的产率___ ,若从120℃开始收集馏分,则乙酸正丁酯的产率偏______________ (填“高”或“低”) ;
| 化合物 | 相对分子质量 | 密度(g/cm3) | 沸点(℃) | 溶解度(g/100g水) |
| 冰醋酸 | 60 | 1.045 | 117.9 | 互溶 |
| 正丁醇 | 74 | 0.80 | 118.0 | 9 |
| 乙酸正丁酯 | 116 | 0.882 | 126. 1 | 0.7 |

分水器的操作方法:先将分水器装满水(水位与支管口相平),再打开活塞,准确放出一定体积的水。在制备过程中,随着加热回流,蒸发后冷凝下来的有机液体和水在分水器中滞留分层,水并到下层(反应前加入的)水中:有机层从上面溢出,流回反应容器。当水层增至支管口时,停止反应。
乙酸正丁酯合成和提纯步骤为:
第一步:取18.5 ml正丁醇和14.4 ml冰醋酸混合加热发生酯化反应,反应装置如图I所示(加热仪器已省略):
第二步:依次用水、饱和Na2CO3溶液、水对三颈烧瓶中的产品洗涤并干燥;
第三步:用装置II蒸馏提纯。
请回答有关问题:
(1)第一步装置中除了加正丁醇和冰醋酸外,还需加入
(2)仪器A中发生反应的化学方程为
(3)第二步用饱和Na2CO3溶液洗涤的目的是
(4)第三步蒸馏产品时,若实验中得到乙酸正丁酯13.92 g,则乙酸正丁酯的产率
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】某实验小组利用下图所示装置在实验室欲制备乙酸乙酯。

(1)B装置中,导管口略高于液面的目的是________________________
(2)为了改善反应过程中混合溶液变黑的现象,甲同学采用NaHSO4代替浓硫酸做催化剂(其他试剂及用量不变)来制备乙酸乙酯,NaHSO4可代替浓硫酸做催化剂的原因是__________________________________________________________
(3)下图是甲同学采用NaHSO4做催化剂,其他条件不变(其中乙酸用量为2 mL)不同质量的NaHSO4来制备乙酸乙酯的催化效果图,其中NaHSO4的质量为_______ g时催化效果最好。

(4)乙同学实验时,在饱和Na2CO3中滴加两滴酚酞,实验结束,取下试管B振荡,红色褪去。为探究褪色的原因,进行如下实验。
a试管①中产生气泡的原因是(用化学方程式解释)____________________________ 。
b对比实验①和②可得出的结论是___________________________________ 。
c针对实验②中现象,乙同学提出猜想:酚酞更易溶于乙酸乙酯。实验③中观察到__________________________________ ,证实乙的猜想正确。

(1)B装置中,导管口略高于液面的目的是
(2)为了改善反应过程中混合溶液变黑的现象,甲同学采用NaHSO4代替浓硫酸做催化剂(其他试剂及用量不变)来制备乙酸乙酯,NaHSO4可代替浓硫酸做催化剂的原因是
(3)下图是甲同学采用NaHSO4做催化剂,其他条件不变(其中乙酸用量为2 mL)不同质量的NaHSO4来制备乙酸乙酯的催化效果图,其中NaHSO4的质量为

(4)乙同学实验时,在饱和Na2CO3中滴加两滴酚酞,实验结束,取下试管B振荡,红色褪去。为探究褪色的原因,进行如下实验。
| 编号 | ① | ② | ③ |
| 实验 |  |  |  |
| 操作 | 充分振荡、静置 | 充分振荡、静置 | 充分振荡、静置、分液。取下层溶液,加入饱和Na2CO3溶液 |
| 现象 | 上层液体变薄,冒气泡,下层溶液红色褪去 | 上层液体不变薄,无气泡,下层溶液红色褪去 |
b对比实验①和②可得出的结论是
c针对实验②中现象,乙同学提出猜想:酚酞更易溶于乙酸乙酯。实验③中观察到
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐2】丙炔酸甲酯(CH≡C-COOCH3 )是一种重要的有机化工原料,沸点为103℃。实验室制备少量丙炔酸甲酯的反应为:CH≡C-COOH+CH3OH CH≡C-COOCH3+H2O。实验步骤如下:
CH≡C-COOCH3+H2O。实验步骤如下:
步骤1:在反应瓶中加入14 g丙炔酸、50 mL甲醇和2 mL浓硫酸,搅拌加热回流一段时间;
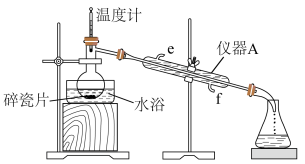
步骤2:蒸出过量的甲醇(装置见图);
步骤3:反应液冷却后,依次用饱和NaCl溶液、5%Na2CO3溶液、水洗涤,分离出有机相;
步骤4:有机相经无水Na2SO4干燥、过滤、蒸馏,得7.56g丙炔酸甲酯。
(1)步骤1中,加入过量甲醇的目的是________ 。
(2)步骤2中,图中所示的装置中仪器A的名称是________ ,自来水从________ (填“e”或“f”)进入该仪器;加入碎瓷片的目的是________ 。
(3)步骤3中,用5%Na2CO3溶液洗涤,主要除去的物质是________ ;分离出有机相的操作名称为________ 。
(4)步骤4中,蒸馏时不能用水浴加热的原因是________ 。
(5)丙炔酸甲酯的产率为________ 。
 CH≡C-COOCH3+H2O。实验步骤如下:
CH≡C-COOCH3+H2O。实验步骤如下:步骤1:在反应瓶中加入14 g丙炔酸、50 mL甲醇和2 mL浓硫酸,搅拌加热回流一段时间;
步骤2:蒸出过量的甲醇(装置见图);

步骤3:反应液冷却后,依次用饱和NaCl溶液、5%Na2CO3溶液、水洗涤,分离出有机相;
步骤4:有机相经无水Na2SO4干燥、过滤、蒸馏,得7.56g丙炔酸甲酯。
(1)步骤1中,加入过量甲醇的目的是
(2)步骤2中,图中所示的装置中仪器A的名称是
(3)步骤3中,用5%Na2CO3溶液洗涤,主要除去的物质是
(4)步骤4中,蒸馏时不能用水浴加热的原因是
(5)丙炔酸甲酯的产率为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐3】青蒿素是烃的含氧衍生物,为无色针状晶体,易溶于丙酮、氯仿和苯,可溶于甲醇、乙醇、乙醚、石油醚,几乎不溶于水中,熔点为156~157℃,热稳定性差,青蒿素是高效的抗疟药。已知乙醚的沸点为35℃。从青蒿中提取青蒿素的方法之一是以萃取原理为基础的,主要有乙醚浸取法和汽油浸取法。乙醚浸取法的主要工艺为:

请回答下列问题:
(1)对青蒿进行干燥破碎的目的是_____ 。操作II的名称是____ 。操作III的主要过程可能是____ (填序号)。
a.加水溶解,蒸发浓缩、冷却结晶
b.加95%的乙醇,浓缩、结晶、过滤
c.加入乙醚,进行萃取分液
(2)用下列实验装置测定青蒿素分子式的方法如图:将28.2g青蒿素样品放在硬质玻璃管C中,缓缓通入空气数分钟后,再点燃酒精灯充分反应,精确测定装置E和F实验前后的质量,根据所测数据计算。
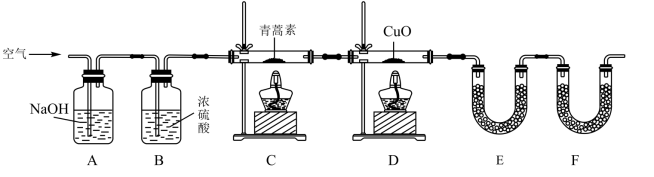
①装置E中盛放的物质是____ ,装置F中盛放的物质是____ 。
②该实验装置可能会产生误差,造成测定含氧量偏低,改进方法是____ 。
③用合理改进后的装置进行实验,称得:
则测得的青蒿素的最简式是_____ 。
(3)某学生对青蒿素的性质进行探究。将青蒿素加入含有NaOH、酚酞的水溶液中,青蒿素的溶解量较小,加热并搅拌,青蒿素的溶解量增大,且溶液红色变浅,说明青蒿素与____ (填序号)具有相似的性质。
a.乙醇 b.乙酸 c.乙酸乙酯 d.葡萄糖
(4)某科研小组经多次提取青蒿素实验,认为用石油醚做溶剂较为适宜,实验中通过控制其他实验条件不变,来研究原料的粒度、提取时间和提取温度对青蒿素提取速率的影响。

由图可知控制其他实验条件不变,最佳原料粒度、提取时间和提取温度为_____ (填序号)。
a.80目、100min、50℃ b.60目、120min、50℃ c.60目、120min、55℃
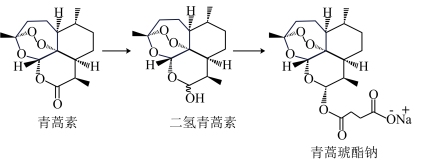
(5)在青蒿素发现、提取和合成研究之后,相继开发出其衍生物:二氢青蒿素、青蒿琥酯钠等。该类衍生物与青蒿素相比,具有____ 的优点,可显著提高疗效。

请回答下列问题:
(1)对青蒿进行干燥破碎的目的是
a.加水溶解,蒸发浓缩、冷却结晶
b.加95%的乙醇,浓缩、结晶、过滤
c.加入乙醚,进行萃取分液
(2)用下列实验装置测定青蒿素分子式的方法如图:将28.2g青蒿素样品放在硬质玻璃管C中,缓缓通入空气数分钟后,再点燃酒精灯充分反应,精确测定装置E和F实验前后的质量,根据所测数据计算。

①装置E中盛放的物质是
②该实验装置可能会产生误差,造成测定含氧量偏低,改进方法是
③用合理改进后的装置进行实验,称得:
| 装置 | 实验前/g | 实验后/g |
| E | 22.6 | 42.4 |
| F | 80.2 | 146.2 |
(3)某学生对青蒿素的性质进行探究。将青蒿素加入含有NaOH、酚酞的水溶液中,青蒿素的溶解量较小,加热并搅拌,青蒿素的溶解量增大,且溶液红色变浅,说明青蒿素与
a.乙醇 b.乙酸 c.乙酸乙酯 d.葡萄糖
(4)某科研小组经多次提取青蒿素实验,认为用石油醚做溶剂较为适宜,实验中通过控制其他实验条件不变,来研究原料的粒度、提取时间和提取温度对青蒿素提取速率的影响。

由图可知控制其他实验条件不变,最佳原料粒度、提取时间和提取温度为
a.80目、100min、50℃ b.60目、120min、50℃ c.60目、120min、55℃
(5)在青蒿素发现、提取和合成研究之后,相继开发出其衍生物:二氢青蒿素、青蒿琥酯钠等。该类衍生物与青蒿素相比,具有

您最近一年使用:0次
解答题-有机推断题
|
适中
(0.65)
解题方法
【推荐1】有机物A在标准状况下的密度为1.25g•L-1。以A为原料合成乙酸乙酯的路线如图所示。已知D的分子式为C2H4O2。

请回答下列问题:
(1)A的结构简式为___ ,D中官能团的名称是___ ,反应④的反应类型是___ 。
(2)反应②的化学方程式是__ ,反应⑤的化学方程式是__ 。
(3)某同学用如图所示的装置制取少量乙酸乙酯。实验结束后,试管甲中上层为透明的,不溶于水的油状液体。
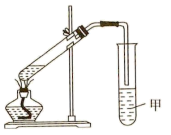
①实验开始前试管甲中的试剂为__ ,导管不能插入试管甲溶液中的原因是___ 。
②用1molB和1molD充分反应,理论上不能生成1mol乙酸乙酯,原因是__ 。

请回答下列问题:
(1)A的结构简式为
(2)反应②的化学方程式是
(3)某同学用如图所示的装置制取少量乙酸乙酯。实验结束后,试管甲中上层为透明的,不溶于水的油状液体。

①实验开始前试管甲中的试剂为
②用1molB和1molD充分反应,理论上不能生成1mol乙酸乙酯,原因是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐2】乙酸乙酯是一种重要的化工原料,广泛用于药物染料、香料等工业。已知乙醇可以和氯化钙反应生成微溶于水的CaCl2·6C2H5OH。
(一)实验室合成乙酸乙酯的粗产品的步骤如下:
制备乙酸乙酯粗产品:如图所示的仪器装置,在蒸馏烧瓶内将过量的乙醇与适量浓硫酸混合,然后经分液漏斗边滴加乙酸,边加热蒸馏。得到含有乙醇、乙酸和水的乙酸乙酯粗产品。___________ 。
(2)冷凝水流经直形冷凝管时应从___________ 进入,从___________ 流出(填“a”或“b”)。
(二)对乙酸乙酯进行精制
(3)为了除去粗产品中的乙酸,可向产品中加入___________ 溶液,然后进行___________ (填操作名称)。
(4)再向得到的有机物中加入饱和氯化钙溶液,振荡、分离,加入饱和氯化钙溶液的目的是___________ 。
(5)最后,加入无水硫酸钠除去其中的水分,再进行___________ (填操作名称),即可得到纯净的乙酸乙酯。
(6)用30 g乙酸与46 g乙醇反应合成乙酸乙酯,若实际产量是理论产量的70%,则实际得到乙酸乙酯的质量为___________ g。
(一)实验室合成乙酸乙酯的粗产品的步骤如下:
制备乙酸乙酯粗产品:如图所示的仪器装置,在蒸馏烧瓶内将过量的乙醇与适量浓硫酸混合,然后经分液漏斗边滴加乙酸,边加热蒸馏。得到含有乙醇、乙酸和水的乙酸乙酯粗产品。
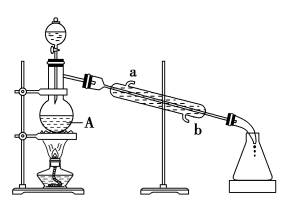
(2)冷凝水流经直形冷凝管时应从
(二)对乙酸乙酯进行精制
(3)为了除去粗产品中的乙酸,可向产品中加入
(4)再向得到的有机物中加入饱和氯化钙溶液,振荡、分离,加入饱和氯化钙溶液的目的是
(5)最后,加入无水硫酸钠除去其中的水分,再进行
(6)用30 g乙酸与46 g乙醇反应合成乙酸乙酯,若实际产量是理论产量的70%,则实际得到乙酸乙酯的质量为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】乙酸是食醋的主要成分。
(1)乙酸的分子式是___________ 。乙酸中官能团的名称是___________ 。
(2)乙酸可使紫色石蕊溶液变___________ 色。
(3)一定条件下,乙酸能与乙醇发生反应生成一种具有香味的油状液体。某研究性学习小组成员分别设计了如下甲、乙、丙三套实验装置:
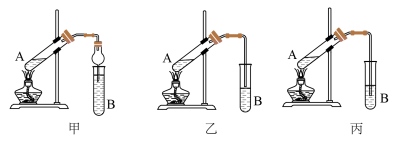
①B试管中的液体物质是___________ ,A中发生反应的化学方程式为___________ ,该有机反应的类型是___________ 反应。
②甲、乙、丙三套装置中,不宜选用的装置是___________ (填“甲”、“乙”、“丙”)
③试管B中的液体能和生成物中混有的某杂质发生反应,该反应的化学方程式是___________ 。
④生成乙酸乙酯的反应是可逆反应,下列能说明该反应已达到化学平衡状态的是___________ (填字母)。
A.单位时间里,生成1mol乙酸乙酯,同时生成1mol水
B.单位时间里,生成1mol乙酸乙酯,同时生成1mol乙酸
C.单位时间里,消耗1mol乙醇,同时消耗1mol乙酸
D.正反应的速率与逆反应的速率相等
E.混合物中各物质的物质的量相等
(1)乙酸的分子式是
(2)乙酸可使紫色石蕊溶液变
(3)一定条件下,乙酸能与乙醇发生反应生成一种具有香味的油状液体。某研究性学习小组成员分别设计了如下甲、乙、丙三套实验装置:

①B试管中的液体物质是
②甲、乙、丙三套装置中,不宜选用的装置是
③试管B中的液体能和生成物中混有的某杂质发生反应,该反应的化学方程式是
④生成乙酸乙酯的反应是可逆反应,下列能说明该反应已达到化学平衡状态的是
A.单位时间里,生成1mol乙酸乙酯,同时生成1mol水
B.单位时间里,生成1mol乙酸乙酯,同时生成1mol乙酸
C.单位时间里,消耗1mol乙醇,同时消耗1mol乙酸
D.正反应的速率与逆反应的速率相等
E.混合物中各物质的物质的量相等
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】最常见的塑化剂邻苯二甲酸二丁酯可由邻苯二甲酸酐与正丁醇在浓硫酸共热下反应制得,反应的化学方程式及装置图(部分装置省略)如下:

已知:正丁醇沸点118℃,纯邻苯二甲酸二丁酯是无色透明、具有芳香气味的油状液体,沸点340℃,酸性条件下,温度超过180℃时易发生分解,邻苯二甲酸酐、正丁醇、邻苯二甲酸二丁酯实验操作流程如下:
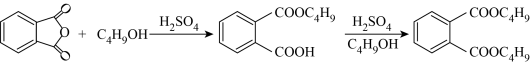
①三颈烧瓶内加入30g邻苯二甲酸酐16g正丁醇以及少量浓硫酸。
②搅拌,升温至105℃,持续搅拌反应2小时,升温至140℃。搅拌、保温至反应结束。
③冷却至室温,将反应混合物倒出,通过工艺流程中的操作X,得到粗产品。
④粗产品用无水硫酸镁处理至澄清→取清液(粗酯)→圆底烧瓶→减压蒸馏
请回答以下问题:
(1)仪器a的名称______________ ,邻苯二甲酸酐、正丁醇和浓硫酸的加入顺序有严格的要求,请问浓硫酸是在_____________ (填最前、最后或中间)加入。
(2)步骤②中不断从分水器下部分离出产物水的目的是____________ ,判断反应已结束的方法是_______________ 。
(3)反应的第一步进行得迅速而完全,第二步是可逆反应,进行较缓慢,为提高反应速率,可采取的措施是:___________________ 。
A.增大压强 B.增加正丁醇的量 C.分离出水 D.加热至200℃
(4)操作X中,应先用5%Na2CO3溶液洗涤粗产品,纯碱溶液浓度不宜过高,更不能使用氢氧化钠,若使用氢氧化钠溶液,对产物有什么影响?(用化学方程式表示):____________________________ 。
(5)粗产品提纯流程中采用减压蒸馏的目的是____________________________ 。
(6)用测定相对分子质量的方法,可以检验所得产物是否纯净,现代分析方法中测定有机物相对分子质量通常采用的仪器是________________________ 。

已知:正丁醇沸点118℃,纯邻苯二甲酸二丁酯是无色透明、具有芳香气味的油状液体,沸点340℃,酸性条件下,温度超过180℃时易发生分解,邻苯二甲酸酐、正丁醇、邻苯二甲酸二丁酯实验操作流程如下:

①三颈烧瓶内加入30g邻苯二甲酸酐16g正丁醇以及少量浓硫酸。
②搅拌,升温至105℃,持续搅拌反应2小时,升温至140℃。搅拌、保温至反应结束。
③冷却至室温,将反应混合物倒出,通过工艺流程中的操作X,得到粗产品。
④粗产品用无水硫酸镁处理至澄清→取清液(粗酯)→圆底烧瓶→减压蒸馏
请回答以下问题:
(1)仪器a的名称
(2)步骤②中不断从分水器下部分离出产物水的目的是
(3)反应的第一步进行得迅速而完全,第二步是可逆反应,进行较缓慢,为提高反应速率,可采取的措施是:
A.增大压强 B.增加正丁醇的量 C.分离出水 D.加热至200℃
(4)操作X中,应先用5%Na2CO3溶液洗涤粗产品,纯碱溶液浓度不宜过高,更不能使用氢氧化钠,若使用氢氧化钠溶液,对产物有什么影响?(用化学方程式表示):
(5)粗产品提纯流程中采用减压蒸馏的目的是
(6)用测定相对分子质量的方法,可以检验所得产物是否纯净,现代分析方法中测定有机物相对分子质量通常采用的仪器是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】1,2-二溴乙烷可作汽油抗爆剂的添加剂,常温下它是无色液体,不溶于水,易溶于醇等有机溶剂。实验室制备1,2-二溴乙烷的反应原理如下:
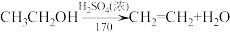

已知:①乙醇在浓硫酸存在下在 脱水生成乙醚
脱水生成乙醚

②实验中常因温度过高而使乙醇和浓硫酸反应生成少量 和
和 ,用
,用 溴和足量的乙醇制备1,2-二溴乙烷,实验装置如图所示(加热与夹持装置略):
溴和足量的乙醇制备1,2-二溴乙烷,实验装置如图所示(加热与夹持装置略):
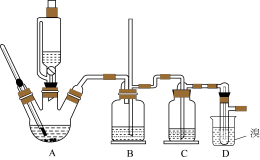
有关数据列表如下:
回答下列问题:
(1)在此制备实验中,A中按最佳体积比3∶1加入乙醇与浓硫酸后,A中还要加入几粒碎瓷片,其作用是_________ 。要尽可能迅速地把反应温度提高到 左右,其最主要目的是
左右,其最主要目的是_________ 。
(2)装置B的作用是作安全瓶,瓶中盛水,除了可以防止倒吸以外,还可判断装置是否堵塞,若堵塞,B中现象是___________ 。
(3)在装置C中应加入 溶液,其目的是
溶液,其目的是___________ 。
(4)装置D中小试管内盛有液溴,判断该制备反应已经结束的最简单方法是___________ 。
(5)将1,2-二溴乙烷粗产品置于分液漏斗中加水,振荡后静置,产物应在___________ 层(填“上”或“下”)。若产物中有少量未反应的 ,最好用
,最好用___________ 洗涤除去;若产物中有少量副产物乙醚,可用___________ (填操作方法名称)的方法除去。
(6)反应过程中应用冷水冷却装置D,其主要目的是乙烯与溴反应时放热,冷却可避免溴的大量挥发;但又不能过度冷却(如用冰水),其原因是___________ 。
(7)若实验结束后得到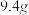 产品,1,2-二溴乙烷的产率为
产品,1,2-二溴乙烷的产率为___________ (保留三位有效数字)。
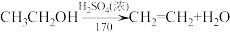

已知:①乙醇在浓硫酸存在下在
 脱水生成乙醚
脱水生成乙醚
②实验中常因温度过高而使乙醇和浓硫酸反应生成少量
 和
和 ,用
,用 溴和足量的乙醇制备1,2-二溴乙烷,实验装置如图所示(加热与夹持装置略):
溴和足量的乙醇制备1,2-二溴乙烷,实验装置如图所示(加热与夹持装置略):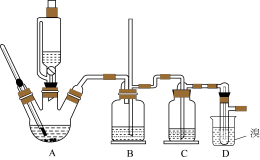
有关数据列表如下:
| 物质 | 乙醇 | 1,2-二溴乙烷 | 乙醚 |
| 状态 | 无色液体 | 无色液体 | 无色液体 |
密度/ | 0.79 | 2.2 | 0.71 |
沸点/ | 78.5 | 132 | 34.6 |
熔点/ | -130 | 9 | -116 |
(1)在此制备实验中,A中按最佳体积比3∶1加入乙醇与浓硫酸后,A中还要加入几粒碎瓷片,其作用是
 左右,其最主要目的是
左右,其最主要目的是(2)装置B的作用是作安全瓶,瓶中盛水,除了可以防止倒吸以外,还可判断装置是否堵塞,若堵塞,B中现象是
(3)在装置C中应加入
 溶液,其目的是
溶液,其目的是(4)装置D中小试管内盛有液溴,判断该制备反应已经结束的最简单方法是
(5)将1,2-二溴乙烷粗产品置于分液漏斗中加水,振荡后静置,产物应在
 ,最好用
,最好用(6)反应过程中应用冷水冷却装置D,其主要目的是乙烯与溴反应时放热,冷却可避免溴的大量挥发;但又不能过度冷却(如用冰水),其原因是
(7)若实验结束后得到
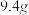 产品,1,2-二溴乙烷的产率为
产品,1,2-二溴乙烷的产率为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐3】肉桂酸是一种重要的中间体,通常用Perkin反应法制备,化学方程式为
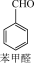 +(CH3CO)2O
+(CH3CO)2O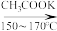 CH3COOH+
CH3COOH+
苯甲醛为无色油状液体,在水中溶解度较小,在乙醇中溶解度较大,沸点为179℃,肉桂酸为白色固体,难溶于水,在乙醇中溶解度较大,沸点为300℃。
Ⅰ.制备:如图甲将3g醋酸钾、3 新蒸馏的苯甲醛和5.5
新蒸馏的苯甲醛和5.5 乙酸酐装入反应装置中,加热使其保持微微沸腾(150~170℃)1h。
乙酸酐装入反应装置中,加热使其保持微微沸腾(150~170℃)1h。
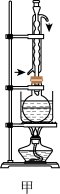
Ⅱ.分离与提纯:
①将反应混合物趁热(100℃左右)倒入盛有25 水的250
水的250 圆底烧瓶B中。用饱和碳酸钠水溶液将
圆底烧瓶B中。用饱和碳酸钠水溶液将 调为8,然后进行水蒸气蒸馏。
调为8,然后进行水蒸气蒸馏。
②加少量活性炭脱色,煮沸数分钟趁热过滤,滤液用浓盐酸调至 为4,冷却析晶,过滤,洗涤,干燥后即得白色肉桂酸。
为4,冷却析晶,过滤,洗涤,干燥后即得白色肉桂酸。
③产品用含水乙醇(水∶乙醇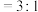 )进行重结晶,得到纯肉桂酸晶体。
)进行重结晶,得到纯肉桂酸晶体。
请回答下列问题:
(1)图甲中为控制温度在150~170℃,必须增加的玻璃仪器是_______ 。
(2)图乙装置A中装有水,装置B中导管要伸入混合物中的原因是_______ ,判断水蒸气蒸馏结束的现象为_______ 。

(3)步骤Ⅱ的②中趁热过滤的目的_______ 。
(4)步骤③重结晶析出的肉桂酸晶体通过减压过滤分离。下列说法正确的是_______ 。
A.选择减压过滤是因为过滤速度快而且能得到较干燥的晶体
B.放入比布氏漏斗内径小的滤纸后,用倾析法转移溶液和沉淀,再开大水龙头抽滤
C.当吸滤瓶液面高度达到支管口位置时,从吸滤瓶支管倒出溶液,防止溢出
D.抽滤完毕时,应先断开抽气泵和吸滤瓶之间的橡皮管,再关水龙头
(5)重结晶的正确操作为_____ (选出正确操作并按序排列)取粗产品干燥得到纯净晶体。
A.将粗产品加入圆底烧瓶中
B.安装回流装置,通冷凝水,加热、回流至晶体全部溶解
C.将适量含水乙醇加入圆底烧瓶
D.用乙醇洗涤
E.用水洗涤
F.转移至蒸发皿中蒸发至余下少量液体时,余热蒸干
G.冷却结晶,抽滤
 +(CH3CO)2O
+(CH3CO)2O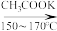 CH3COOH+
CH3COOH+
苯甲醛为无色油状液体,在水中溶解度较小,在乙醇中溶解度较大,沸点为179℃,肉桂酸为白色固体,难溶于水,在乙醇中溶解度较大,沸点为300℃。
Ⅰ.制备:如图甲将3g醋酸钾、3
 新蒸馏的苯甲醛和5.5
新蒸馏的苯甲醛和5.5 乙酸酐装入反应装置中,加热使其保持微微沸腾(150~170℃)1h。
乙酸酐装入反应装置中,加热使其保持微微沸腾(150~170℃)1h。
Ⅱ.分离与提纯:
①将反应混合物趁热(100℃左右)倒入盛有25
 水的250
水的250 圆底烧瓶B中。用饱和碳酸钠水溶液将
圆底烧瓶B中。用饱和碳酸钠水溶液将 调为8,然后进行水蒸气蒸馏。
调为8,然后进行水蒸气蒸馏。②加少量活性炭脱色,煮沸数分钟趁热过滤,滤液用浓盐酸调至
 为4,冷却析晶,过滤,洗涤,干燥后即得白色肉桂酸。
为4,冷却析晶,过滤,洗涤,干燥后即得白色肉桂酸。③产品用含水乙醇(水∶乙醇
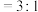 )进行重结晶,得到纯肉桂酸晶体。
)进行重结晶,得到纯肉桂酸晶体。请回答下列问题:
(1)图甲中为控制温度在150~170℃,必须增加的玻璃仪器是
(2)图乙装置A中装有水,装置B中导管要伸入混合物中的原因是

(3)步骤Ⅱ的②中趁热过滤的目的
(4)步骤③重结晶析出的肉桂酸晶体通过减压过滤分离。下列说法正确的是
A.选择减压过滤是因为过滤速度快而且能得到较干燥的晶体
B.放入比布氏漏斗内径小的滤纸后,用倾析法转移溶液和沉淀,再开大水龙头抽滤
C.当吸滤瓶液面高度达到支管口位置时,从吸滤瓶支管倒出溶液,防止溢出
D.抽滤完毕时,应先断开抽气泵和吸滤瓶之间的橡皮管,再关水龙头
(5)重结晶的正确操作为
A.将粗产品加入圆底烧瓶中
B.安装回流装置,通冷凝水,加热、回流至晶体全部溶解
C.将适量含水乙醇加入圆底烧瓶
D.用乙醇洗涤
E.用水洗涤
F.转移至蒸发皿中蒸发至余下少量液体时,余热蒸干
G.冷却结晶,抽滤
您最近一年使用:0次



