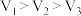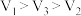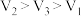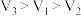下列计算结果正确的是
| A.32.5 g Zn与一定量浓硫酸完全反应,生成的气体分子数目小于0.5NA |
| B.2H2S+SO2 = 3S↓+2H2O反应中氧化产物与还原产物的物质的量之比为1 : 2 |
| C.将NO2和O2等体积混合充满试管,倒置于水槽中充分反应,试管中剩余气体占试管容积的1/8 |
| D.常温常压下(Vm=24.5L/mol),用排空气法收集HCl气体于干燥烧瓶做喷泉实验,假设烧瓶内溶液不外溢,所得盐酸的物质的量浓度为1/24.5 mol/L |
更新时间:2019-06-01 21:13:47
|
相似题推荐
单选题
|
适中
(0.65)
解题方法
【推荐1】把a L含(NH4)2SO4和NH4NO3的混合液分成两等份,一份用b mol烧碱刚好把NH3全部赶出,另一份与BaCl2溶液完全反应,消耗c mol BaCl2,则原溶液中c(NO )为
)为
 )为
)为A.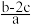 mol·L-1 mol·L-1 | B. mol·L-1 mol·L-1 |
C.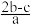 mol·L-1 mol·L-1 | D.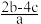 mol·L-1 mol·L-1 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】0.5L0.5mol/L的AlCl3溶液与0.25L1mol/L的MgCl2溶液中,Cl-浓度之比为
| A.3∶2 | B.1∶2 | C.3∶4 | D.2∶3 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】足量的铜与一定量的浓硝酸反应得到硝酸铜溶液和NO、N2O4、NO2 的混合气体,这些气体与1.68LO2(标准状况)混合后通入水中,所有气体完全被水吸收生成硝酸,则和铜反应的硝酸的物质的量可能是
| A.0.55mol | B.0.4mol | C.0.6mol | D.0.65mol |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】诺贝尔化学奖获得者施罗克等人发现金属钼的卡宾化合物可以作为非常有效的烯烃复分解催化剂。工业上冶炼钼的化学原理为
①2MoS2+7O2 2MoO3+4SO2;
2MoO3+4SO2;
②MoO3+2NH3·H2O=(NH4)2MoO4+H2O;
③(NH4)2MoO4+2HCl=H2MoO4↓+2NH4Cl;
④H2MoO4 MoO3+H2O;
MoO3+H2O;
⑤用还原剂将MoO3还原成金属钼。
则下列说法正确的是
①2MoS2+7O2
 2MoO3+4SO2;
2MoO3+4SO2;②MoO3+2NH3·H2O=(NH4)2MoO4+H2O;
③(NH4)2MoO4+2HCl=H2MoO4↓+2NH4Cl;
④H2MoO4
 MoO3+H2O;
MoO3+H2O;⑤用还原剂将MoO3还原成金属钼。
则下列说法正确的是
| A.煅烧MoS2生成22.4L SO2反应转移电子的物质的量为7mol |
| B.MoO3是金属氧化物,也是碱性氧化物 |
| C.H2MoO4是一种强酸 |
| D.利用H2、CO和铝分别还原等量的MoO3,所消耗还原剂的物质的量之比为3:3:2 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】将盛有NO2和N2混合气体的试管倒立于水中,经过足够长的时间后,试管内气体体积缩小为原体积的一半,原混合气体中N2与NO2的体积比为
| A.1:1 | B.1:2 | C.1:3 | D.3:1 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】同温同压下,将两个容积相等的干燥圆底烧瓶中分别充满相应的气体后进行喷泉实验(如图所示)。下列说法错误的是
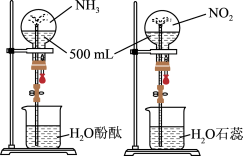

| A.打开止水夹,挤出胶头滴管中的水都可产生“喷泉” |
| B.“喷泉”都呈红色 |
| C.实验后烧瓶中溶液的体积之比是3∶2 |
| D.实验后烧瓶中溶质的物质的量浓度之比是3∶2 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】对下列事实的解释不正确的是
| A.古代农谚中有“雷雨发庄稼”、“豆茬种谷,必定有福”的说法,其中“雷雨”、“豆茬”涉及到的是自然固氮 |
B. 和氯气均能使品红溶液褪色,说明 和氯气均能使品红溶液褪色,说明 和氯气均有漂白性 和氯气均有漂白性 |
| C.氨可以设计完成喷泉实验,说明氨极易溶于水 |
| D.加入浓硫酸后的蔗糖固体由白色变为黑色海绵状,并有刺激性气味的气体放出,说明浓硫酸具有脱水性和强氧化性 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列说法正确的是
| A.工业上通过氯气与澄清石灰水反应制取漂白粉 |
| B.浓硫酸具有吸水性,可用于干燥硫化氢气体 |
| C.浓硫酸与铁在常温下不能持续反应,所以可用铁质容器贮运浓硫酸 |
| D.“洁厕灵”(主要成分为盐酸)和“84消毒液”(主要成分为次氯酸钠)常被混合使用 |
您最近半年使用:0次


 通入适量KOH溶液,产物中可能有KCl、KClO、
通入适量KOH溶液,产物中可能有KCl、KClO、 ,且产物的成分与温度高低有关。当
,且产物的成分与温度高低有关。当 时,下列有关说法错误的是
时,下列有关说法错误的是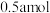
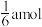
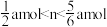
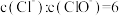 ,则溶液中
,则溶液中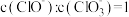
 、
、 、
、 ,则下列关系正确的是
,则下列关系正确的是