下列各物质中,按熔点由高到低的顺序排列正确的是( )
| A.CH4>SiH4>GeH4>SnH4 |
| B.KCl>NaCl>MgCl2>MgO |
| C.Rb>K>Na>Li |
| D.金刚石>Si>钠 |
16-17高二下·新疆·阶段练习 查看更多[8]
(已下线)解密05 物质结构 元素周期律(讲义)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(浙江专用)(已下线)解密05 物质结构 元素周期律(讲义)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(全国通用)(已下线)解密05 物质结构元素周期律(讲义)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练(已下线)解密05 物质结构元素周期律(讲义)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练(浙江专版)江苏省镇江市吕叔湘中学2019-2020学年高二下学期4月诊断考试化学试题黑龙江省哈尔滨市阿城区第二中学2018-2019学年高二下学期期中考试化学试题河北省黄骅中学2018-2019学年高二下学期第二次月考化学试题新疆生产建设兵团第二中学2016-2017学年高二下学期第二次月考化学试题
更新时间:2019-06-06 17:46:07
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】下列关于晶体的说法中错误的是
| A.固态不导电而熔融状态导电的晶体一定是离子晶体 |
| B.金属晶体中一定含有金属键,金属键没有方向性和饱和性 |
C.熔点是10.31 ,液态不导电,水溶液能导电的晶体一定是分子晶体 ,液态不导电,水溶液能导电的晶体一定是分子晶体 |
D.具有正四面体结构的晶体,可能是共价晶体或分子晶体,其键角都是 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列各项叙述中,正确的是
| A.电负性相差越大的元素间越易形成离子键 |
| B.AB₃型的分子空间结构一定为平面三角形 |
| C.分子晶体中,分子间作用力越大,分子越稳定 |
D.用于幽门螺旋杆菌示踪的 外围电子排布式为2s²2p³ 外围电子排布式为2s²2p³ |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】周期表中ⅣA族元素及其化合物应用广泛。 、
、 是重要的半导体材料;我国古代就掌握了青铜(铜-锡合金)的冶炼、加工技术,制造出许多精美的青铜器;
是重要的半导体材料;我国古代就掌握了青铜(铜-锡合金)的冶炼、加工技术,制造出许多精美的青铜器;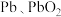 是铅蓄电池的电极材料。下列说法正确的是
是铅蓄电池的电极材料。下列说法正确的是
 、
、 是重要的半导体材料;我国古代就掌握了青铜(铜-锡合金)的冶炼、加工技术,制造出许多精美的青铜器;
是重要的半导体材料;我国古代就掌握了青铜(铜-锡合金)的冶炼、加工技术,制造出许多精美的青铜器;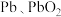 是铅蓄电池的电极材料。下列说法正确的是
是铅蓄电池的电极材料。下列说法正确的是A.金刚石与石墨烯中的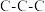 夹角都为 夹角都为 |
B.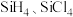 都是由极性键构成的非极性分子 都是由极性键构成的非极性分子 |
C.锗原子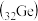 基态核外电子排布式为 基态核外电子排布式为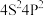 |
| D.ⅣA族元素单质的晶体类型相同 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列关于物质的组成、结构或性质的叙述中,正确的是
| A.第三周期主族元素中,第一电离能和电负性最大的都是氯 |
| B.HF的稳定性很强,是因为其分子间能形成氢键 |
| C.基态原子价电子排布式为(n-1)d6~8ns2的元素属于第ⅧB族 |
| D.金刚石、金刚砂(SiC)、单晶硅为共价晶体,共价键依次增强,熔点依次升高 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】下面的叙述不正确的是( )
| A.晶胞空间利用率:金属铜>金属镁>金属钾>金属钋 |
| B.硬度由大到小:金刚石>碳化硅>晶体硅 |
| C.晶体熔点由低到高:Na2O<MgO<Al2O3 |
| D.晶格能由大到小:NaF>NaCl>NaBr>NaI |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】下列描述正确的是
| A.焰色反应只是金属单质特有的性质 |
| B.能看见漂亮的焰火是因为电子吸收能量跃迁到能量较高的能级而发出的光 |
| C.金属具有金属光泽是因为金属中的自由电子吸收了可见光,又把各种波长的光大部分反射出来 |
| D.金属具有导热性,是通过金属阳离子之间的碰撞来传导热量 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】从结构角度分析,下列说法错误的是
A.I 的立体构型为V形,中心原子的杂化方式为sp3 的立体构型为V形,中心原子的杂化方式为sp3 |
| B.CCl2F2无同分异构体,说明其中碳原子采用sp3方式杂化 |
| C.N2O与CO2、CCl3F与CCl2F2互为等电子体 |
| D.因金属性K>Na>Mg,所以熔点:KCl >NaCl >MgCl2 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】下列物质性质的变化规律中与共价键键能大小有关的是
①F2、Cl2、Br2、I2的熔点、沸点逐渐升高;②HF、HCl、HBr、HI的热稳定性依次减弱
③金刚石的硬度、熔点、沸点都高于晶体硅;④NaF、NaCl、NaBr、NaI熔点依次降低
①F2、Cl2、Br2、I2的熔点、沸点逐渐升高;②HF、HCl、HBr、HI的热稳定性依次减弱
③金刚石的硬度、熔点、沸点都高于晶体硅;④NaF、NaCl、NaBr、NaI熔点依次降低
| A.仅③ | B.①③ | C.②④ | D.②③ |
您最近一年使用:0次

 表示阿伏加德罗常数。下列说法不正确的是
表示阿伏加德罗常数。下列说法不正确的是 和
和 所含的分子数相同
所含的分子数相同 和
和 所含的质子数相同
所含的质子数相同 金刚石中
金刚石中 键数和
键数和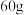 石英晶体中
石英晶体中 键数均为
键数均为
 丙烯中
丙烯中 键数为
键数为 ,
, 键数为
键数为

