我国科学家借助自主研制的新型钨钴合金催化剂攻克了单壁碳纳米管结构的可控制备难题。

(1)基态钴原子的核外未成对电子数为__________ 。单壁碳纳米管可看作石墨烯沿一定方向卷曲而成的空心圆柱体,其结构如图所示,其中碳原子的杂化方式为_______ 。
(2)纳米结构氧化钴可在室温下将甲醛(HCHO)完全催化氧化,已知甲醛各原子均满足稳定结构,甲醛分子属______ 分子(选填“极性”“非极性”),其分子的空间构型为_____ 。新制备的Cu(OH)2可将乙醛(CH3CHO)氧化为乙酸,而自身还原成Cu2O,乙酸的沸点明显高于乙醛,其主要原因是______ 。Cu2O为半导体材料,在其立方晶胞内部有4个氧原子,其余氧原子位于面心和顶点,则该晶胞中有______ 个铜原子。金属Cu为________ 堆积,配位数为_______ 。
(3)橙红色晶体羰基钴的熔点为52℃,分子式为Co2(CO)8,是一种重要的配合物,可溶于多数有机溶剂。该晶体属于______ 晶体,三种元素电负性由大到小的顺序为(填元素符号)_____ 。配体CO的任意一种等电子体的电子式:_____ 。配体CO中与Co形成配位键的原子是C而不是O的原因是________ 。

(1)基态钴原子的核外未成对电子数为
(2)纳米结构氧化钴可在室温下将甲醛(HCHO)完全催化氧化,已知甲醛各原子均满足稳定结构,甲醛分子属
(3)橙红色晶体羰基钴的熔点为52℃,分子式为Co2(CO)8,是一种重要的配合物,可溶于多数有机溶剂。该晶体属于
更新时间:2019-06-22 10:56:30
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】请回答以下问题:
(1)NH3BH3分子中,与N原子相连的H呈正电性(Hδ+),与B原子相连的H呈负电性(Hδ-),而与其原子总数相等的等电子体CH3CH3相比,NH3BH3熔点比CH3CH3高,其原因是__ 。
(2)已知高温下,冰晶石密度为2.1g/cm3,铝单质的密度为2.3g/cm3,工业上电解法制单质铝的过程中,冰晶石起到哪些作用__ 。
(1)NH3BH3分子中,与N原子相连的H呈正电性(Hδ+),与B原子相连的H呈负电性(Hδ-),而与其原子总数相等的等电子体CH3CH3相比,NH3BH3熔点比CH3CH3高,其原因是
(2)已知高温下,冰晶石密度为2.1g/cm3,铝单质的密度为2.3g/cm3,工业上电解法制单质铝的过程中,冰晶石起到哪些作用
您最近一年使用:0次
【推荐2】氮及其化合物在生产、生活和科技等方面有重要的应用。请回答下列问题:
(1)氮元素基态原子的价电子排布式为______________ 。
(2)在氮分子中,氮原子之间存在着______ 个σ键和______ 个π键。
(3)磷、氮、氧是周期表中相邻的三种元素,比较:(均填“大于”、“小于”或“等于”)
①氮原子的第一电离能________ 氧原子的第一电离能;
②N2分子中氮氮键的键长________ 白磷(P4)分子中磷磷键的键长;
(4)氮元素的氢化物(NH3)是一种易液化的气体,请阐述原因是_____________________ 。
(5)配合物[Cu(NH3)4]Cl2中含有4个配位键,若用2个N2H4代替其中的2个NH3,得到的配合物[Cu(NH3)2(N2H4)2]Cl2中含有配位键的个数为________ 。
(1)氮元素基态原子的价电子排布式为
(2)在氮分子中,氮原子之间存在着
(3)磷、氮、氧是周期表中相邻的三种元素,比较:(均填“大于”、“小于”或“等于”)
①氮原子的第一电离能
②N2分子中氮氮键的键长
(4)氮元素的氢化物(NH3)是一种易液化的气体,请阐述原因是
(5)配合物[Cu(NH3)4]Cl2中含有4个配位键,若用2个N2H4代替其中的2个NH3,得到的配合物[Cu(NH3)2(N2H4)2]Cl2中含有配位键的个数为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】判断电子的运动状态
按要求填空:
(1)基态F原子核外电子的运动状态有______ 种。
(2)基态钛原子的价电子排布式为________ ,其原子核外电子的空间运动状态有________ 种,共有________ 种运动状态不同的电子。
(3)基态Si原子价电子的运动状态有________ 种,若其电子排布式表示为[Ne]3s23p 违背了
违背了________ 。
(4)基态Cu原子核外电子的空间运动状态有________ 种。
按要求填空:
(1)基态F原子核外电子的运动状态有
(2)基态钛原子的价电子排布式为
(3)基态Si原子价电子的运动状态有
 违背了
违背了(4)基态Cu原子核外电子的空间运动状态有
您最近一年使用:0次
【推荐2】如图是s能级和p能级的原子轨道图。

试回答下列问题:
(1)s电子的原子轨道呈_______ 形,每个s能级有_______ 个原子轨道;p电子的原子轨道呈_______ 形,每个p能级有_______ 个原子轨道。
(2)元素X的原子最外层电子排布式为nsnnpn+1,原子中能量最高的是_______ 电子,其电子云在空间有3个互相_______ (填“垂直”或“平行”)的伸展方向。元素X的名称是_______ ,它的最低价氢化物的电子式是_______ 。
(3)元素Y的原子最外层电子排布式为nsn-1npn+1,Y的元素符号为_______ ,原子的核外电子排布式为_______ 。
(4)下列电子排布图中,能正确表示元素X的原子处于最低能量状态的是_______。

试回答下列问题:
(1)s电子的原子轨道呈
(2)元素X的原子最外层电子排布式为nsnnpn+1,原子中能量最高的是
(3)元素Y的原子最外层电子排布式为nsn-1npn+1,Y的元素符号为
(4)下列电子排布图中,能正确表示元素X的原子处于最低能量状态的是_______。
A.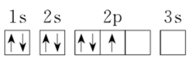 | B.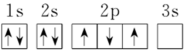 |
C. | D. |
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】回答下列问题:
(1)如图所示为元素周期表中氮元素部分信息,数据“14.01”表示的是____ ,氮元素原子核外有____ 个未成对电子,最外层有____ 种能量不同的电子。

(2)氮和磷是同主族元素,下列能说明二者非金属性相对强弱的是____ (填编号)。
a.NH3比PH3稳定性强 b.电负性数据:N3.0、P2.1
c.硝酸显强氧化性,磷酸不显强氧化性 d.氮气常温是气体,磷单质是固体
(3)2020年12月17日,我国“嫦娥五号”返回器携月壤成功着陆。研究发现,月壤中存在天然的铁、金、银、铅、锌、铜、锑、铼等矿物颗粒。
①要证明月壤中含有这些元素,可采用的方法是____ 。
②写出铜的基态原子的电子排布式____ 。
③周期表中,与铜位于同一周期的元素原子中最外层电子数与铜原子的相同的元素有____ (填元素符号)。
(1)如图所示为元素周期表中氮元素部分信息,数据“14.01”表示的是

(2)氮和磷是同主族元素,下列能说明二者非金属性相对强弱的是
a.NH3比PH3稳定性强 b.电负性数据:N3.0、P2.1
c.硝酸显强氧化性,磷酸不显强氧化性 d.氮气常温是气体,磷单质是固体
(3)2020年12月17日,我国“嫦娥五号”返回器携月壤成功着陆。研究发现,月壤中存在天然的铁、金、银、铅、锌、铜、锑、铼等矿物颗粒。
①要证明月壤中含有这些元素,可采用的方法是
②写出铜的基态原子的电子排布式
③周期表中,与铜位于同一周期的元素原子中最外层电子数与铜原子的相同的元素有
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】碳元素能形成多种单质如金刚石、石墨等,24g 金刚石中含有_______ 个碳碳单键。碳元素也能形成多种化合物,在形成化合物时,其所成化学键以共价键为主,原因是 _______ 。
(1)工业制镁时,电解 MgCl2 而不电解 MgO 的原因是_______ 。
(2)BeCl2 熔点较低,易升华,能溶于有机溶剂。由此可推测 BeCl2 晶体为_______ 晶体(填晶体类型),其分子为_______ 分子(填“极性”或“非极性”),分子构型为_______ ,BeCl2 熔点_______ (选填“低于”或“高于”)BeBr2。
(1)工业制镁时,电解 MgCl2 而不电解 MgO 的原因是
(2)BeCl2 熔点较低,易升华,能溶于有机溶剂。由此可推测 BeCl2 晶体为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】下表是元素周期表的一部分。表中所列的字母分别代表一种元素。
回答下列问题:
(1)D的简单气态氢化物分子的立体构型为___________ 。
(2)第一电离能H___________ X(填“>”、“<”或“=”)。
(3)DA3的沸点比D2E的沸点高,其原因是___________ 。
(4)YE 的立体构型为
的立体构型为___________ ,YE 的键角比YE
的键角比YE 的键角小的原因是
的键角小的原因是___________ 。
| A | R | ||||||||||||||||
| B | D | E | M | T | |||||||||||||
| G | H | X | J | Y | L | ||||||||||||
| N |
(1)D的简单气态氢化物分子的立体构型为
(2)第一电离能H
(3)DA3的沸点比D2E的沸点高,其原因是
(4)YE
 的立体构型为
的立体构型为 的键角比YE
的键角比YE 的键角小的原因是
的键角小的原因是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】根据要求回答下列问题:
(1) 是有机合成中常用的还原剂,
是有机合成中常用的还原剂, 中阴离子的空间构型是
中阴离子的空间构型是_______ ,中心原子的杂化类型为_______ , 中,存在
中,存在_______ (填标号)。
A.离子键 B. 键 C.
键 C. 键 D.配位键
键 D.配位键
(2)碳氧化物、氨氧化物、二氧化硫的处理和应用是世界各国研究的热点问题。 的VSEPR模型为
的VSEPR模型为_______ ; 的中心原子的杂化类型为
的中心原子的杂化类型为_______ ; 与
与 互为等电子体,且
互为等电子体,且 中O只与一个N相连,则
中O只与一个N相连,则 的空间构型为
的空间构型为_______ ,分子中的 键和
键和 键数目之比是
键数目之比是_______ 。
(3)某研究小组将平面形的铂配合物分子进行层状堆砌,使每个分子中的铂原子在某一方向上排列成行,构成能导电的“分子金属”,其结构如图所示。
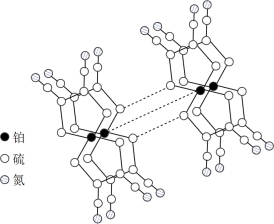
①“分子金属”可以导电,是因为_______ 能沿着其中的金属原子链流动。
②“分子金属”中,铂原子不是采取 杂化,其理由是
杂化,其理由是_______ 。
(1)
 是有机合成中常用的还原剂,
是有机合成中常用的还原剂, 中阴离子的空间构型是
中阴离子的空间构型是 中,存在
中,存在A.离子键 B.
 键 C.
键 C. 键 D.配位键
键 D.配位键(2)碳氧化物、氨氧化物、二氧化硫的处理和应用是世界各国研究的热点问题。
 的VSEPR模型为
的VSEPR模型为 的中心原子的杂化类型为
的中心原子的杂化类型为 与
与 互为等电子体,且
互为等电子体,且 中O只与一个N相连,则
中O只与一个N相连,则 的空间构型为
的空间构型为 键和
键和 键数目之比是
键数目之比是(3)某研究小组将平面形的铂配合物分子进行层状堆砌,使每个分子中的铂原子在某一方向上排列成行,构成能导电的“分子金属”,其结构如图所示。

①“分子金属”可以导电,是因为
②“分子金属”中,铂原子不是采取
 杂化,其理由是
杂化,其理由是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】根据要求完成下列问题:
(1)某元素原子共有3个价电子,其中一个价电子位于第三能层d轨道,试回答:
该元素价电子排布式_____________________ 。
(2)外围电子排布式为3d54s2的原子,其原子结构示意图为____________ ,其最高正价为________ ;其在元素周期表中的位置为___________________ 。
(3)下列分子中是否有手性原子:_________ (填“有”或“无”,若有请在图中碳原子下方用“*”标出)

(4)在下列物质①CO2、②NH3、③CCl4、④BF3、⑤H2O、⑥SO2、⑦SO3、⑧PCl3中,属于非极性分子的是(填序号)________________ 。
(5)试比较下列含氧酸的酸性强弱(填“>”“<”或“=”):
HClO3________ HClO4; H3PO4________ H3PO3。
(1)某元素原子共有3个价电子,其中一个价电子位于第三能层d轨道,试回答:
该元素价电子排布式
(2)外围电子排布式为3d54s2的原子,其原子结构示意图为
(3)下列分子中是否有手性原子:

(4)在下列物质①CO2、②NH3、③CCl4、④BF3、⑤H2O、⑥SO2、⑦SO3、⑧PCl3中,属于非极性分子的是(填序号)
(5)试比较下列含氧酸的酸性强弱(填“>”“<”或“=”):
HClO3
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】分析 、
、 、
、 、
、 、
、 、
、 分子的成键(极性键与非极性键)情况,判断其为极性分子还是非极性分子
分子的成键(极性键与非极性键)情况,判断其为极性分子还是非极性分子_________ 。
 、
、 、
、 、
、 、
、 、
、 分子的成键(极性键与非极性键)情况,判断其为极性分子还是非极性分子
分子的成键(极性键与非极性键)情况,判断其为极性分子还是非极性分子
您最近一年使用:0次



