(1)反应A+3B=2C+2D在四种不同情况下的反应速率分别为:
①v(A)=0.15 mol/(L·s); ②v(B)=0.6 mol/(L·s);
③v(C)=0.4 mol/(L·s); ④v(D)=0.45 mol/(L·s)。
该反应进行的快慢顺序为________________ 。
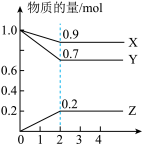
(2)某温度时,在2L容器中X、Y、Z三种物质的量随时间的变化曲线如图所示。由图中数据分析,该反应的化学方程式为_______________________ 。反应开始至2min,Z的平均反应速率为_______________________ 。
①v(A)=0.15 mol/(L·s); ②v(B)=0.6 mol/(L·s);
③v(C)=0.4 mol/(L·s); ④v(D)=0.45 mol/(L·s)。
该反应进行的快慢顺序为
(2)某温度时,在2L容器中X、Y、Z三种物质的量随时间的变化曲线如图所示。由图中数据分析,该反应的化学方程式为

更新时间:2019-06-23 18:53:06
|
相似题推荐
【推荐1】在一定温度下,向一容积为5 L的恒容密闭容器中充入0.4 mol SO2和0.2 mol O2,发生反应:2SO2(g)+O2(g) ⇌2SO3(g) ∆H =-196 kJ/mol。经2 min后达到平衡,当反应达到平衡时,容器内压强变为起始时的0.8倍。请回答下列问题:
(1)判断该反应达到平衡状态的标志是_______ (填字母);
a.SO2、O2、SO3三者的浓度之比为2:1:2
b.容器内气体的压强不变
c.容器内混合气体的密度保持不变
d.SO3的物质的量不再变化
e.SO2的生成速率和SO3的生成速率相等
(2)从反应开始到平衡的这段时间O2的转化率为_______ ,用SO2的浓度变化表示的平均反应速率v(SO2)= _______ 达到平衡时反应放出的热量为_______ ;
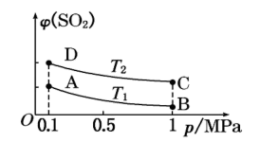
(3)若反应温度降低,SO2的转化率_______ (填“增大”“减小”或“不变”);如图表示平衡时SO2的体积分数随压强和温度变化的曲线。则温度关系:T1_______ T2(填“>”“<”或“=”)。
(1)判断该反应达到平衡状态的标志是
a.SO2、O2、SO3三者的浓度之比为2:1:2
b.容器内气体的压强不变
c.容器内混合气体的密度保持不变
d.SO3的物质的量不再变化
e.SO2的生成速率和SO3的生成速率相等
(2)从反应开始到平衡的这段时间O2的转化率为
(3)若反应温度降低,SO2的转化率

您最近半年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】无色气体N2O4是一种强氧化剂,为重要的火箭推进剂之一。N2O4与NO2转换的热化学方程式为N2O4(g)⇌2NO2(g) ΔH=+24.4 kJ·mol-1。上述反应中,正反应速率v正=k正·p(N2O4),逆反应速率v逆=k逆·p2(NO2),其中k正、k逆为速率常数,则Kp为_______ (以k正、k逆表示)。若将一定量N2O4投入真空容器中恒温恒压分解(温度298 K、压强100 kPa),已知该条件下k正=4.8×104 s-1,当N2O4分解10%时,v正=_______ kPa·s-1。
您最近半年使用:0次
计算题
|
适中
(0.65)
【推荐3】已知:反应aA(g)+bB(g)  cC(g)。某温度下,在
cC(g)。某温度下,在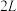 的密闭容器中投入一定的A、B,两种气体的物质的量浓度随时间变化的曲线如图所示。
的密闭容器中投入一定的A、B,两种气体的物质的量浓度随时间变化的曲线如图所示。
(1)经测定前4s内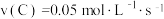 ,则该反应的化学方程式为
,则该反应的化学方程式为_________ 。
(2)请在图中将生成物C的物质的量浓度随时间的变化曲线绘制出来_________ 。
(3)若上述反应分别在甲、乙、丙三个相同的密闭器中进行,经同一段时间后,测得三个容器中的反应速率分别为
甲: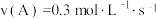
乙:
丙:
则甲、乙、丙三个容器中反应速率由快到慢的顺序为______________ 。
 cC(g)。某温度下,在
cC(g)。某温度下,在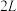 的密闭容器中投入一定的A、B,两种气体的物质的量浓度随时间变化的曲线如图所示。
的密闭容器中投入一定的A、B,两种气体的物质的量浓度随时间变化的曲线如图所示。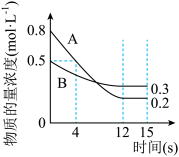
(1)经测定前4s内
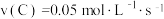 ,则该反应的化学方程式为
,则该反应的化学方程式为(2)请在图中将生成物C的物质的量浓度随时间的变化曲线绘制出来
(3)若上述反应分别在甲、乙、丙三个相同的密闭器中进行,经同一段时间后,测得三个容器中的反应速率分别为
甲:
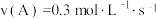
乙:

丙:

则甲、乙、丙三个容器中反应速率由快到慢的顺序为
您最近半年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐1】在一个容积为3 L的密闭容器内进行如下反应:A2(气)+3B2(气)=aX(气)。反应开始时,n(A2)=1.5 mol,n(B2)=4.0 mol,2 min后,n(B2)=0.4 mol, n(X)=2.4 mol。计算:
(1)a值______________ 。
(2)X的表示式(用A、B表示)________________ 。
(3)υ(B2)为_____________ 。
(4)2 min末的A2的浓度_______________ 。
(1)a值
(2)X的表示式(用A、B表示)
(3)υ(B2)为
(4)2 min末的A2的浓度
您最近半年使用:0次
计算题
|
适中
(0.65)
名校
【推荐2】将等物质的量的A、B混合于2L的密闭容器中,发生如下反应:3A(g)+B(g) xC(g)+2D(g),经过5分钟后,测得D的浓度为0.5mol/L,C的平均反应速率是0.1mol/(L·min),且c(A):c(B)=3:5求:
xC(g)+2D(g),经过5分钟后,测得D的浓度为0.5mol/L,C的平均反应速率是0.1mol/(L·min),且c(A):c(B)=3:5求:
(1)此时A的浓度为______ ;
(2)反应开始前放入容器中A、B的物质的量是_____________ ;
(3)B的平均反应速率是_________________ ;
(4)x值为____________ 。
 xC(g)+2D(g),经过5分钟后,测得D的浓度为0.5mol/L,C的平均反应速率是0.1mol/(L·min),且c(A):c(B)=3:5求:
xC(g)+2D(g),经过5分钟后,测得D的浓度为0.5mol/L,C的平均反应速率是0.1mol/(L·min),且c(A):c(B)=3:5求: (1)此时A的浓度为
(2)反应开始前放入容器中A、B的物质的量是
(3)B的平均反应速率是
(4)x值为
您最近半年使用:0次
计算题
|
适中
(0.65)
【推荐3】I.为比较Fe3+和Cu2+对H2O2分解的催化效果,某化学研究小组的同学分别设计了如图甲、乙所示的实验。请回答相关问题:
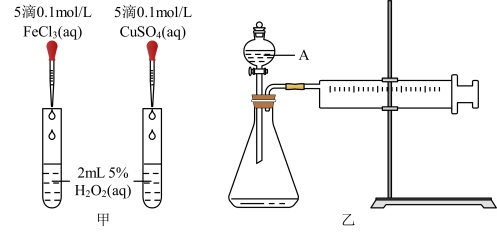
(1)定性分析:如图甲可通过观察__________ 的快慢,定性比较得出结论。有同学提出将FeCl3改为0. 05mol·L-1 Fe2 (SO4)3更为合理,其理由是____________ 。
(2)定量分析:如图乙所示,实验时均以生成40 mL气体为准,其他可能影响实验的因素均已忽略。实验中需要测量的数据是________ 。
II.某温度时,在一个2L的密闭容器中, A、B、C三种气体物质的物质的量随时间的变化曲线如图所示。根据图中数据,试填写下列空白:

(3)该反应的化学方程式为________ ;
(4)从开始至2min,A的平均反应速率为________ ;

(1)定性分析:如图甲可通过观察
(2)定量分析:如图乙所示,实验时均以生成40 mL气体为准,其他可能影响实验的因素均已忽略。实验中需要测量的数据是
II.某温度时,在一个2L的密闭容器中, A、B、C三种气体物质的物质的量随时间的变化曲线如图所示。根据图中数据,试填写下列空白:

(3)该反应的化学方程式为
(4)从开始至2min,A的平均反应速率为
您最近半年使用:0次



