按要求写出下列反应的方程式:
(1)实验室制备氯气的离子反应方程式_______________ ;
(2)乙醇催化氧化反应(铜做催化剂)_______________ ;
(3)苯与浓硝酸反应_______________ ;
(4)CH3CH=CH2生成高聚物_______________ ;
(5)往氢氧化钙溶液中加入过量碳酸氢钠的离子方程式_______________ 。
(1)实验室制备氯气的离子反应方程式
(2)乙醇催化氧化反应(铜做催化剂)
(3)苯与浓硝酸反应
(4)CH3CH=CH2生成高聚物
(5)往氢氧化钙溶液中加入过量碳酸氢钠的离子方程式
更新时间:2019-07-28 18:08:38
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】氧化还原反应在生产、生活和生命活动中起着十分重要的作用.例如,饮用水处理和污水净化问题中就广泛应用了氧化还原反应的原理.
Ⅰ.高铁酸钠 是一种新型绿色消毒剂,主要用于饮用水处理.工业上制备高铁酸钠有多种方法,其中一种方法的化学原理可用化学方程式表示为:
是一种新型绿色消毒剂,主要用于饮用水处理.工业上制备高铁酸钠有多种方法,其中一种方法的化学原理可用化学方程式表示为:
(1)在 中,
中, 的化合价为
的化合价为___________ 价;上述反应中,每生成 ,有
,有___________  电子转移.
电子转移.
(2)制备 的另外一种方法是在碱性条件下用
的另外一种方法是在碱性条件下用 和
和 反应,请配平下列离子方程式:
反应,请配平下列离子方程式:_____
__ ____
____ _____
_____ ____
____ _____
_____ _____
_____
Ⅱ.含氯消毒剂在自来水净化过程中也起到了重要作用.
(3)很多自来水厂用氯气来杀菌、消毒,实验室不能用自来水配制硝酸银溶液,用离子方程式表示其原因___________ .实验室常用浓盐酸与二氧化锰反应来制取 ,请写出反应的化学方程式
,请写出反应的化学方程式___________ .
(4)亚氯酸钠 是一种高效的漂白剂和氧化剂,其制备方法如下:
是一种高效的漂白剂和氧化剂,其制备方法如下: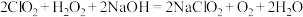
根据氧化剂的氧化性强于氧化产物这一规律,从上述反应中可知氧化性_________ >__________;
(5)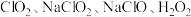 都常被用作消毒剂,上述物质消毒效率最高的是___________(填序号).(已知:消毒效率是以单位物质的量的物质得电子的数目多少表示,得电子越多效率越高)
都常被用作消毒剂,上述物质消毒效率最高的是___________(填序号).(已知:消毒效率是以单位物质的量的物质得电子的数目多少表示,得电子越多效率越高)
Ⅰ.高铁酸钠
 是一种新型绿色消毒剂,主要用于饮用水处理.工业上制备高铁酸钠有多种方法,其中一种方法的化学原理可用化学方程式表示为:
是一种新型绿色消毒剂,主要用于饮用水处理.工业上制备高铁酸钠有多种方法,其中一种方法的化学原理可用化学方程式表示为:
(1)在
 中,
中, 的化合价为
的化合价为 ,有
,有 电子转移.
电子转移.(2)制备
 的另外一种方法是在碱性条件下用
的另外一种方法是在碱性条件下用 和
和 反应,请配平下列离子方程式:
反应,请配平下列离子方程式:__
 ____
____ _____
_____ ____
____ _____
_____ _____
_____
Ⅱ.含氯消毒剂在自来水净化过程中也起到了重要作用.
(3)很多自来水厂用氯气来杀菌、消毒,实验室不能用自来水配制硝酸银溶液,用离子方程式表示其原因
 ,请写出反应的化学方程式
,请写出反应的化学方程式(4)亚氯酸钠
 是一种高效的漂白剂和氧化剂,其制备方法如下:
是一种高效的漂白剂和氧化剂,其制备方法如下: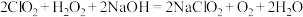
根据氧化剂的氧化性强于氧化产物这一规律,从上述反应中可知氧化性
(5)
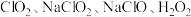 都常被用作消毒剂,上述物质消毒效率最高的是___________(填序号).(已知:消毒效率是以单位物质的量的物质得电子的数目多少表示,得电子越多效率越高)
都常被用作消毒剂,上述物质消毒效率最高的是___________(填序号).(已知:消毒效率是以单位物质的量的物质得电子的数目多少表示,得电子越多效率越高)A. | B. | C. | D. |
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】用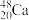 轰击
轰击 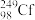 ,生成
,生成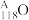 g并放出3个中子(
g并放出3个中子( )。
)。
(1)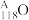 g的原子核内中子数是
g的原子核内中子数是_______ 。
(2)推测Og在元素周期表的位置_______ 。
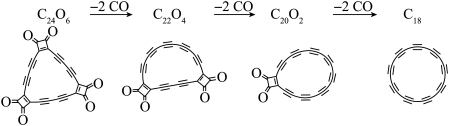
(3)2019年科学家首次合成全碳的环形分子,下列说法正确的是_______
(4)写出实验室制取氯气的化学方程式_______ ;
(5)在383K时,将二氧化锰溶解于浓硫酸中,可得硫酸锰[ Mn2 ( SO4)3]并放出氧气。试写出该反应的化学方程式_______ ;
(6)已知铋酸钠( NaBiO3 )是一种浅黄色的粉末,不溶于冷水,它可以在高酸度的溶液中将Mn2+氧化成 ,自身被还原成Bi3+。试写出该反应的离子方程式
,自身被还原成Bi3+。试写出该反应的离子方程式_______ 。
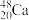 轰击
轰击 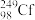 ,生成
,生成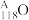 g并放出3个中子(
g并放出3个中子( )。
)。(1)
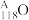 g的原子核内中子数是
g的原子核内中子数是(2)推测Og在元素周期表的位置
(3)2019年科学家首次合成全碳的环形分子,下列说法正确的是_______

| A.C18和金刚石、石墨互为同素异形体 |
| B.C18是一种性质很稳定的化合物 |
| C.C20O2、C22O4、C24O6随着碳原子数的增大,氧元素的质量百分含量依次增大 |
| D.C22O4、CO、CO2都是碳元素的氧化物 |
(5)在383K时,将二氧化锰溶解于浓硫酸中,可得硫酸锰[ Mn2 ( SO4)3]并放出氧气。试写出该反应的化学方程式
(6)已知铋酸钠( NaBiO3 )是一种浅黄色的粉末,不溶于冷水,它可以在高酸度的溶液中将Mn2+氧化成
 ,自身被还原成Bi3+。试写出该反应的离子方程式
,自身被还原成Bi3+。试写出该反应的离子方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】请写出下列反应的离子方程式:
①氯气与氯化亚铁溶液的反应_________________________________________________
②二氧化锰与浓盐酸反应_______________________________________________________
③氢氧化铝与足量氢氧化钠反应__________________________________________________
④ 偏铝酸钠与过量二氧化碳的反应________________________________________________
①氯气与氯化亚铁溶液的反应
②二氧化锰与浓盐酸反应
③氢氧化铝与足量氢氧化钠反应
④ 偏铝酸钠与过量二氧化碳的反应
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】食品安全关系国计民生,影响食品安全的因素很多.下面是以食品为主题的相关问题,请根据要求回答.
(1)聚偏二氯乙烯(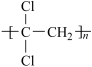 )具有超强阻隔性能,可作为保鲜食品的包装材料.它是由
)具有超强阻隔性能,可作为保鲜食品的包装材料.它是由___________ (写结构简式) 单体发生加聚反应生成的.若以乙炔为原料,通过加成反应生成1,1,2三氯乙烷,再和氢氧化钠醇溶液反应可合成这种单体,则在加成反应中宜选择的试剂是_________ .(选填编号字母)
a.HCl b.Cl2 c.HClO d.NaCl
(2)人们从食用植物油中摄取的亚油酸[ ]对人体健康是十分有益的,然而市场上经常会出现价格低廉的植物油,其中的亚油酸含量很低.下列关于亚油酸的说法中不正确的是
]对人体健康是十分有益的,然而市场上经常会出现价格低廉的植物油,其中的亚油酸含量很低.下列关于亚油酸的说法中不正确的是___________ (选填编号字母).
a.分子式为C18H34O2
b.在食用油中亚油酸通常是以甘油酯的形式存在
c.亚油酸属于一种不饱和低级脂肪酸,所以能和NaOH溶液反应
d.亚油酸含量高的植物油在空气中易氧化变质
(3)食用酱油中的“氯丙醇”是多种氯代丙醇的总称,它们是在酱油配制过程中植物蛋白水解发生一系列化学变化而产生的,氯丙醇中部分异构体对人体有不同程度的致癌效应.则氯丙醇中三氯丙醇异构体共有_________ 种(已知卤原子和羟基一般不会连在同一碳原子上).
(4)在淀粉中加入吊白块制得的粉丝有毒.淀粉最终的水解产物是葡萄糖,请设计实验证明淀粉已经全部水解,写出操作方法、现象和结论______________ .
(5)木糖醇[CH2OH(CHOH)3CH2OH]作为一种甜味剂,食用后不会引起血糖升高,比较适合于糖尿病人食用.预测木糖醇能和新制备的Cu(OH)2浊液发生化学反应的依据是___________ .
(6)酒精在人体肝脏内可转化为多种有害物质,有机物A是其中的一种,对A的结构进行如下分析:
①通过样品的质谱分析测得A的相对分子质量为60.
②对A的水溶液进行测定发现该溶液pH<7.
③核磁共振氢原子光谱能对有机物分子中同性氢原子给出相同的峰值,根据峰值可以确定分子中氢原子的种类和数目.例如乙醇有三种氢原子(图1).经测定有机物A的核磁共振氢谱示意图如图2
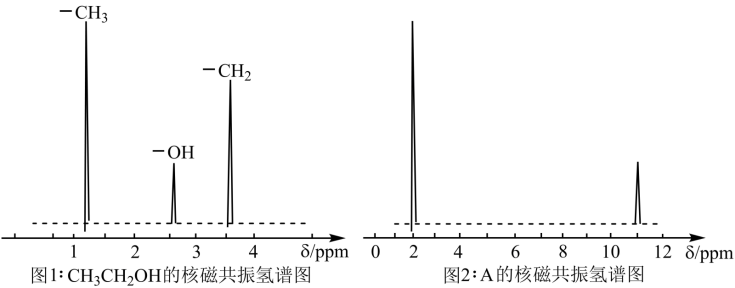
根据以上分析,写出A的结构简式__________ .
(1)聚偏二氯乙烯(
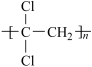 )具有超强阻隔性能,可作为保鲜食品的包装材料.它是由
)具有超强阻隔性能,可作为保鲜食品的包装材料.它是由a.HCl b.Cl2 c.HClO d.NaCl
(2)人们从食用植物油中摄取的亚油酸[
 ]对人体健康是十分有益的,然而市场上经常会出现价格低廉的植物油,其中的亚油酸含量很低.下列关于亚油酸的说法中不正确的是
]对人体健康是十分有益的,然而市场上经常会出现价格低廉的植物油,其中的亚油酸含量很低.下列关于亚油酸的说法中不正确的是a.分子式为C18H34O2
b.在食用油中亚油酸通常是以甘油酯的形式存在
c.亚油酸属于一种不饱和低级脂肪酸,所以能和NaOH溶液反应
d.亚油酸含量高的植物油在空气中易氧化变质
(3)食用酱油中的“氯丙醇”是多种氯代丙醇的总称,它们是在酱油配制过程中植物蛋白水解发生一系列化学变化而产生的,氯丙醇中部分异构体对人体有不同程度的致癌效应.则氯丙醇中三氯丙醇异构体共有
(4)在淀粉中加入吊白块制得的粉丝有毒.淀粉最终的水解产物是葡萄糖,请设计实验证明淀粉已经全部水解,写出操作方法、现象和结论
(5)木糖醇[CH2OH(CHOH)3CH2OH]作为一种甜味剂,食用后不会引起血糖升高,比较适合于糖尿病人食用.预测木糖醇能和新制备的Cu(OH)2浊液发生化学反应的依据是
(6)酒精在人体肝脏内可转化为多种有害物质,有机物A是其中的一种,对A的结构进行如下分析:
①通过样品的质谱分析测得A的相对分子质量为60.
②对A的水溶液进行测定发现该溶液pH<7.
③核磁共振氢原子光谱能对有机物分子中同性氢原子给出相同的峰值,根据峰值可以确定分子中氢原子的种类和数目.例如乙醇有三种氢原子(图1).经测定有机物A的核磁共振氢谱示意图如图2

根据以上分析,写出A的结构简式
您最近一年使用:0次
【推荐2】按要求填空:
(1)键线式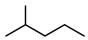 表示的分子式为
表示的分子式为_________ ,名称是____________ 。
(2)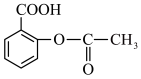 含有的官能团的名称为
含有的官能团的名称为_____________ ,写出该物质在酸性环境下水解产物的结构简式__________ 、__________ 。
(3)甲醇在铜作催化剂加热时与氧气反应的化学方程式为_________________ 。
(4)某烷烃B 的结构简式为CH3CH(CH3)CH(C2H5)2, 有一种烷烃C与烷烃B是同分异构体,它却不能由任何烯烃催化加氢得到,则C的结构简式为____________ 。
(5)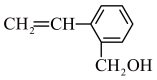 最多
最多______ 个原子共平面,写出该物质发生加聚反应的化学方程式_________ 。
(1)键线式
 表示的分子式为
表示的分子式为(2)
 含有的官能团的名称为
含有的官能团的名称为(3)甲醇在铜作催化剂加热时与氧气反应的化学方程式为
(4)某烷烃B 的结构简式为CH3CH(CH3)CH(C2H5)2, 有一种烷烃C与烷烃B是同分异构体,它却不能由任何烯烃催化加氢得到,则C的结构简式为
(5)
 最多
最多
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】填空
(1)写出漂白粉有效成分的化学式_____ 。
(2)写出1,2-二溴乙烷的结构简式_____ 。
(3)任写一个能得到SO2的化学反应方程式_____ 。
(4)已知25℃和101KPa时,液态甲醇(CH₃OH)的燃烧热/ 请写出表示甲醇燃烧热的热化学方程式
请写出表示甲醇燃烧热的热化学方程式_____ 。
(5)根据甲醇在酸性电解质中与氧气作用生成二氧化碳和水的反应,设计一种燃料电池。该燃料电池工作时,负极的电极反应式是_____ 。
(6)以丙烯为原料来生产聚丙烯,请写出该反应的化学方程式为_____ 。
(7)SOCl2是一种液态化合物。向盛有10ml水的锥形瓶中,小心滴加8~10滴SOCl2,可观察到剧烈反应,液面上有白雾形成,并有带刺激性气味的气体逸出。请写出SOCl2与水反应的化学方程式:_____ 。
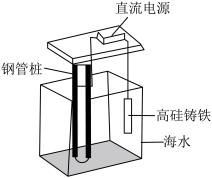
(8)海港、码头的钢管桩会受到海水的长期侵蚀,常用外加电流法对其进行保护,工作原理如图所示。钢管桩上主要发生的电极反应式为:_____ (假设海水为氯化钠溶液,下同)。也可以在钢管桩上焊接锌块进行保护,钢管桩中的铁上主要发生的电极反应式为:_____
(1)写出漂白粉有效成分的化学式
(2)写出1,2-二溴乙烷的结构简式
(3)任写一个能得到SO2的化学反应方程式
(4)已知25℃和101KPa时,液态甲醇(CH₃OH)的燃烧热/
 请写出表示甲醇燃烧热的热化学方程式
请写出表示甲醇燃烧热的热化学方程式(5)根据甲醇在酸性电解质中与氧气作用生成二氧化碳和水的反应,设计一种燃料电池。该燃料电池工作时,负极的电极反应式是
(6)以丙烯为原料来生产聚丙烯,请写出该反应的化学方程式为
(7)SOCl2是一种液态化合物。向盛有10ml水的锥形瓶中,小心滴加8~10滴SOCl2,可观察到剧烈反应,液面上有白雾形成,并有带刺激性气味的气体逸出。请写出SOCl2与水反应的化学方程式:
(8)海港、码头的钢管桩会受到海水的长期侵蚀,常用外加电流法对其进行保护,工作原理如图所示。钢管桩上主要发生的电极反应式为:

您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】(1)①写出NaHCO3的电离方程式:_________ 。
(2)写出苯与液溴在催化剂存在下制溴苯的化学方程式:____________________________ 。
(2)写出苯与液溴在催化剂存在下制溴苯的化学方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】(1)甲苯与浓硫酸、浓硝酸在100℃时能获得不溶于水的淡黄色针状晶体,请写出反应方程式:__________ 。上述反应是加成反应还是取代反应?请判断并说明原因:__________________ 。
(2)Mg3N2是离子化合物,各原子均满足8电子稳定结构,写出Mg3N2的电子式:__________ 。
(3)在常压下,乙醇在水中的溶解度比溴乙烷在水中的溶解度大,主要原因是______ 。
(2)Mg3N2是离子化合物,各原子均满足8电子稳定结构,写出Mg3N2的电子式:
(3)在常压下,乙醇在水中的溶解度比溴乙烷在水中的溶解度大,主要原因是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】现有以下几种有机物:
①CH4 ②CH3CH2OH ③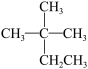 ④癸烷 ⑤CH3COOH ⑥
④癸烷 ⑤CH3COOH ⑥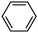 ⑦
⑦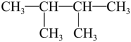 ⑧
⑧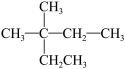 ⑨丙烷
⑨丙烷
请根据上述给出的物质按要求回答下列问题:
(1)分子中含有14个氢原子的烷烃的分子式是____ ;
(2)与③互为同分异构体的是_____ (填序号);
(3)在120℃,1.01×105Pa条件下,某种气态烃与足量的O2完全反应后,测得反应前后气体的体积没有发生改变,则该烃是____ (填序号);它与⑧互为_____ 关系;
(4)相对分子质量为44的烷烃的结构简式为______ ;
(5)用“>”表示①③④⑨熔沸点高低顺序:______ (填序号);
(6)具有特殊气味,常作萃取剂的有机物在铁作催化剂的条件下与液溴发生一取代反应的化学方程式_____ ;
(7)有机物②在加热条件下和CuO反应的化学方程式_______ ;
①CH4 ②CH3CH2OH ③
 ④癸烷 ⑤CH3COOH ⑥
④癸烷 ⑤CH3COOH ⑥ ⑦
⑦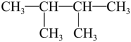 ⑧
⑧ ⑨丙烷
⑨丙烷请根据上述给出的物质按要求回答下列问题:
(1)分子中含有14个氢原子的烷烃的分子式是
(2)与③互为同分异构体的是
(3)在120℃,1.01×105Pa条件下,某种气态烃与足量的O2完全反应后,测得反应前后气体的体积没有发生改变,则该烃是
(4)相对分子质量为44的烷烃的结构简式为
(5)用“>”表示①③④⑨熔沸点高低顺序:
(6)具有特殊气味,常作萃取剂的有机物在铁作催化剂的条件下与液溴发生一取代反应的化学方程式
(7)有机物②在加热条件下和CuO反应的化学方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】(1)甲烷的电子式________ ,乙烯的结构式 ________________ ,乙炔空间构型_____________ ,
(2)在乙醇的化学性质中,各反应的断键方式可概括如下:(填序号)消去反应:______ ;催化氧化:___________ ;
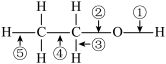
(2)在乙醇的化学性质中,各反应的断键方式可概括如下:(填序号)消去反应:

您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】已知有机物A和C都是厨房中的常用调料品.A是一种无色,有特殊香味的液体,相对分子质量是氢气的23倍.A在Cu催化下,与氧气在加热条件下能生成有机物B;有机物C是一种有强烈刺激性气味的无色液体,能使紫色石蕊溶液变红,并且A与C可以生成一种有芳香气味的液体。
根据以上条件,写出下列反应的化学方程式(注明反应条件):
A→B:______________________________________________________
A+C:________________________________________________________
根据以上条件,写出下列反应的化学方程式(注明反应条件):
A→B:
A+C:
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】下表是A、B、C、D、E五种有机物的有关信息;
根据表中信息回答下列问题:
(1)A与溴的四氯化碳溶液反应的生成物的名称为_____ ;写出在一定条件下,A生成高分子化合物的化学反应方程式______ 。
(2)写出B在浓硫酸作用下,与浓硝酸反应的化学方程式_______ 。
(3)C与E反应能生成相对分子质量为100的酯,其化学反应方程式为______ 。
(4)写出由C氧化生成D的化学反应方程式______ 。
| A | B | C | D | E |
①能使溴的四氯化碳溶液褪色;②比例模型为: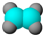 ,③能与水在一定条件下反应生成C ,③能与水在一定条件下反应生成C | ①由C、H两种元素组成;②球棍模型为: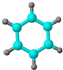 | ①由C、H、O三种元素组成;②能与Na反应,但不能与NaOH溶液反应;③能与E反应生成相对分子质量为100的酯. | ①相对分子质量比C少2;②能由C氧化而成; | ①由C、H、O三种元素组成;②球棍模型为: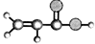 |
根据表中信息回答下列问题:
(1)A与溴的四氯化碳溶液反应的生成物的名称为
(2)写出B在浓硫酸作用下,与浓硝酸反应的化学方程式
(3)C与E反应能生成相对分子质量为100的酯,其化学反应方程式为
(4)写出由C氧化生成D的化学反应方程式
您最近一年使用:0次



