有一含NaCl、Na2CO3·10H2O和NaHCO3的混合物,某同学设计如下实验,通过测量反应前后C、D装置质量的变化,测定该混合物中各组分的质量分数。
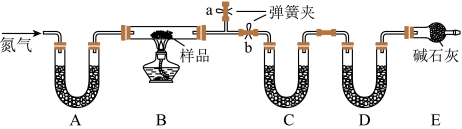
(1)加热前通入氮气的目的是_____________ ,操作方法为____________ 。
(2)装置A、C、D中盛放的试剂分别为A_______ ,C________ ,D_______ 。
(3)若将A装置换成盛放NaOH溶液的洗气瓶,则测得的NaCl的含量将_______ (填“偏高”、“偏低”或“无影响”,下同);若B中反应管右侧有水蒸气冷凝,则测定结果中NaHCO3的含量将________ ;
(4)若样品质量为wg,反应后C、D增加的质量分别为m1g、m2g,由此可知混合物中Na2CO3·10H2O的质量分数为_______ (用含w、m1、m2的代数式表示)

(1)加热前通入氮气的目的是
(2)装置A、C、D中盛放的试剂分别为A
(3)若将A装置换成盛放NaOH溶液的洗气瓶,则测得的NaCl的含量将
(4)若样品质量为wg,反应后C、D增加的质量分别为m1g、m2g,由此可知混合物中Na2CO3·10H2O的质量分数为
更新时间:2019-07-22 09:11:29
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
名校
【推荐1】如图中,A为一种常见的金属单质,B、C、D、E是含有A元素的常见化合物。它们的焰色反应均为黄色。
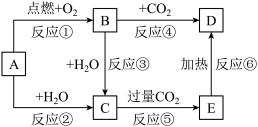
(1)写出下列物质的化学式:B_______ ;E_______ 。
(2)写出B→C反应的化学方程式:_______ ;E→D的化学方程式:_______ 。
(3)加热5.00gD和E的固体混合物,使E完全分解,固体混合物的质量减少了0.31g,则原混合物中D的质量为_______ 。

(1)写出下列物质的化学式:B
(2)写出B→C反应的化学方程式:
(3)加热5.00gD和E的固体混合物,使E完全分解,固体混合物的质量减少了0.31g,则原混合物中D的质量为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐2】碳酸钠俗称纯碱,用途非常广泛,我国化学家侯德榜发明了“侯氏制碱法”。南宁二中2023级化学兴趣小组在实验室中模拟“侯氏制碱法”制备 ,进一步处理得到产品
,进一步处理得到产品 和
和 ,实验流程如下所示。
,实验流程如下所示。
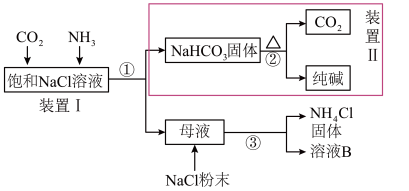
请回答下列问题:
(1)上述流程中,①②③所涉及的操作方法,包含过滤的是___________ (填序号)。过滤时,所需要的玻璃仪器:烧杯、___________ 、___________ 。
(2)向装置Ⅰ的饱和 溶液中通入足量的
溶液中通入足量的 和
和 ,应先通入足量
,应先通入足量___________ (填“ ”或“
”或“ ”)。装置Ⅰ中发生反应的化学方程式为
”)。装置Ⅰ中发生反应的化学方程式为___________ 。
(3)检验装置Ⅱ中制备的纯碱含有 的方法:取少量该纯碱样品溶于水,
的方法:取少量该纯碱样品溶于水,___________ 。
(4)向母液中加入一定量 粉末,存在
粉末,存在 。为使
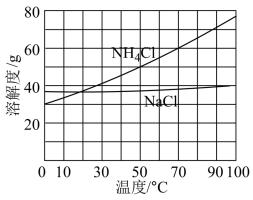
。为使 晶体充分析出并分离,根据下图中
晶体充分析出并分离,根据下图中 和
和 溶解度曲线,需采用的操作为
溶解度曲线,需采用的操作为___________ 、___________ 、过滤、洗涤、干燥。
(5)整个实验流程中,可循环利用的物质的化学式是___________ 。
(6)若装置Ⅱ中得到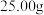 的碳酸钠和碳酸氢钠的固体混合物,加热至混合物质量不再变化,固体质量共减少了
的碳酸钠和碳酸氢钠的固体混合物,加热至混合物质量不再变化,固体质量共减少了 ,则原混合物中碳酸钠的质量分数为
,则原混合物中碳酸钠的质量分数为___________ 。
 ,进一步处理得到产品
,进一步处理得到产品 和
和 ,实验流程如下所示。
,实验流程如下所示。
请回答下列问题:
(1)上述流程中,①②③所涉及的操作方法,包含过滤的是
(2)向装置Ⅰ的饱和
 溶液中通入足量的
溶液中通入足量的 和
和 ,应先通入足量
,应先通入足量 ”或“
”或“ ”)。装置Ⅰ中发生反应的化学方程式为
”)。装置Ⅰ中发生反应的化学方程式为(3)检验装置Ⅱ中制备的纯碱含有
 的方法:取少量该纯碱样品溶于水,
的方法:取少量该纯碱样品溶于水,(4)向母液中加入一定量
 粉末,存在
粉末,存在 。为使
。为使 晶体充分析出并分离,根据下图中
晶体充分析出并分离,根据下图中 和
和 溶解度曲线,需采用的操作为
溶解度曲线,需采用的操作为
(5)整个实验流程中,可循环利用的物质的化学式是
(6)若装置Ⅱ中得到
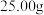 的碳酸钠和碳酸氢钠的固体混合物,加热至混合物质量不再变化,固体质量共减少了
的碳酸钠和碳酸氢钠的固体混合物,加热至混合物质量不再变化,固体质量共减少了 ,则原混合物中碳酸钠的质量分数为
,则原混合物中碳酸钠的质量分数为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
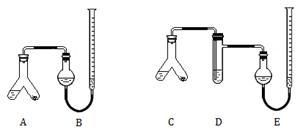
【推荐3】某实验小组分别用图1、2装置测定某种钙片中碳酸钙的含量,夹持装置已略去。
提供的试剂:研细的钙片粉末(钙片中的其他成分不与盐酸反应)、2mol/L 盐酸、5%NaOH溶液、饱和Na2CO3溶液、饱和NaHCO3溶液和蒸馏水。
实验过程:
I.检查两套装置的气密性。
II.在A、C的右边加入0.25 g钙片粉末,左边加入3 mL 2mol/L盐酸,塞紧塞子。在B、E中均加入饱和NaHCO3溶液,如图所示,记下量气管读数。
Ⅲ.将A、C倾斜,使液体与固体混合,实验结束并冷却后读出量气管读数,测得 B中收集到的气体为41.90 mL,E中收集到的气体体积为39.20 mL(以上气体体积均已折算为标准状况下的体积)。
回答下列问题:
(1)I中检查图1装置气密性的方法是______ 。
(2)A中发生反应的离子方程式为______ ;D中加入的试剂为______ 。
(3)实验前左右两管液面在同一水平面上,最后读数时右管的液面高于左管的液面,
应进行的操作是________ 。
(4)图2实验所得钙片中的碳酸钙的质量分数为_______ ;图1实验比图2实验所得钙片中的碳酸钙含量偏高,用离子方程式表示偏高的原因:_________ 。
提供的试剂:研细的钙片粉末(钙片中的其他成分不与盐酸反应)、2mol/L 盐酸、5%NaOH溶液、饱和Na2CO3溶液、饱和NaHCO3溶液和蒸馏水。

图1 图2
实验过程:
I.检查两套装置的气密性。
II.在A、C的右边加入0.25 g钙片粉末,左边加入3 mL 2mol/L盐酸,塞紧塞子。在B、E中均加入饱和NaHCO3溶液,如图所示,记下量气管读数。
Ⅲ.将A、C倾斜,使液体与固体混合,实验结束并冷却后读出量气管读数,测得 B中收集到的气体为41.90 mL,E中收集到的气体体积为39.20 mL(以上气体体积均已折算为标准状况下的体积)。
回答下列问题:
(1)I中检查图1装置气密性的方法是
(2)A中发生反应的离子方程式为
(3)实验前左右两管液面在同一水平面上,最后读数时右管的液面高于左管的液面,
应进行的操作是
(4)图2实验所得钙片中的碳酸钙的质量分数为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐1】铜转炉烟灰主要含有 [还有少量的
[还有少量的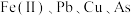 等元素]的硫酸盐和氧化物,少量为砷酸盐。制备重要化工原料活性氧化锌的工艺流程如图所示。请回答以下问题:
等元素]的硫酸盐和氧化物,少量为砷酸盐。制备重要化工原料活性氧化锌的工艺流程如图所示。请回答以下问题:

已知:活性炭净化主要是除去有机杂质。
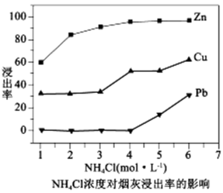
(1)反应温度为50℃,反应时间为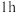 时,测定各元素的浸出率与氯化铵溶液浓度的关系如图,则氯化铵适宜的浓度为
时,测定各元素的浸出率与氯化铵溶液浓度的关系如图,则氯化铵适宜的浓度为______  。浸出液中锌元素以
。浸出液中锌元素以______ 形式存在(填离子符号)。
(2) 溶液的作用是
溶液的作用是______ ,“滤渣II”的成分为______ (填化学式)。
(3)除杂3是置换除杂过程,试剂a是______ (填化学式)。
(4)写出“沉锌”时发生反应的离子方程式______ 。
(5)取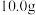 活性氧化锌样品配成待测液,加入3、4滴指示剂,再加入适量六亚甲基四胺,用
活性氧化锌样品配成待测液,加入3、4滴指示剂,再加入适量六亚甲基四胺,用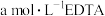 标准液进行滴定,消耗标准液
标准液进行滴定,消耗标准液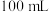 。已知:与
。已知:与 标准液
标准液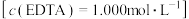 相当的以克表示的氧化锌质量为0.08139,则样品中氧化锌的质量分数为
相当的以克表示的氧化锌质量为0.08139,则样品中氧化锌的质量分数为______ (用含a的代数式表示)。
 [还有少量的
[还有少量的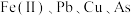 等元素]的硫酸盐和氧化物,少量为砷酸盐。制备重要化工原料活性氧化锌的工艺流程如图所示。请回答以下问题:
等元素]的硫酸盐和氧化物,少量为砷酸盐。制备重要化工原料活性氧化锌的工艺流程如图所示。请回答以下问题:
已知:活性炭净化主要是除去有机杂质。
(1)反应温度为50℃,反应时间为
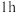 时,测定各元素的浸出率与氯化铵溶液浓度的关系如图,则氯化铵适宜的浓度为
时,测定各元素的浸出率与氯化铵溶液浓度的关系如图,则氯化铵适宜的浓度为 。浸出液中锌元素以
。浸出液中锌元素以
(2)
 溶液的作用是
溶液的作用是(3)除杂3是置换除杂过程,试剂a是
(4)写出“沉锌”时发生反应的离子方程式
(5)取
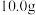 活性氧化锌样品配成待测液,加入3、4滴指示剂,再加入适量六亚甲基四胺,用
活性氧化锌样品配成待测液,加入3、4滴指示剂,再加入适量六亚甲基四胺,用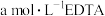 标准液进行滴定,消耗标准液
标准液进行滴定,消耗标准液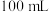 。已知:与
。已知:与 标准液
标准液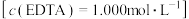 相当的以克表示的氧化锌质量为0.08139,则样品中氧化锌的质量分数为
相当的以克表示的氧化锌质量为0.08139,则样品中氧化锌的质量分数为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】某研究性学习小组为研究Cu与浓H2SO4的反应,设计如下实验探究方案(装置中的固定仪器和酒精灯均未画出)。

实验选用细铜丝、98.3% H2SO4、品红溶液、澄清石灰水、CCl4、NaOH溶液等药品,铜丝被卷成螺旋状,一端没入浓H2SO4中,另一端露置在液面上方。
以下是该学习小组部分交流记录及后续探究实验的记录:
材料一:小组交流摘录
学生1:加热前,无现象发生;加热后,液面下铜丝变黑,产生气泡,有细小黑色颗粒状物质从铜丝表面进入浓硫酸中,黑色物质是什么?值得探究!
学生2:,我也观察到黑色颗粒状物质,后来逐渐转变为灰白色固体,我想该灰白色固体极有可能是未溶于浓硫酸的CuSO4。
学生3:你们是否注意到液面以上的铜丝也发黑,而且试管上部内壁有少量淡黄色S固体凝聚,会不会液面以上的铜丝与硫发生了反应,我查资料发现:2Cu+S = Cu2S(黑色)。
材料二:探究实验剪辑
实验1 将光亮的铜丝在酒精灯火焰上灼烧变黑,然后插入稀硫酸中,铜丝重新变得光亮,溶液呈蓝绿色;将光亮的铜丝置入加热的硫蒸气中变黑,然后插入稀硫酸中无变化。
实验2 截取浓硫酸液面上方变黑的铜丝,插入稀硫酸中无变化;将浓硫酸液面下方变黑的铜丝,插入稀硫酸,黑色明显变浅,溶液呈蓝绿色。
实验3 将溶液中的黑色颗粒状物质,经过滤、稀硫酸洗、蒸馏水洗、干燥后放入氧气流中加热,然后冷却,用电子天平称重发现质量减少10%左右。
根据上述材料回答下列问题:
(1)CuSO4可由金属铜与浓硫酸反应制备,该反应的化学方程式为______________ 。
(2)A试管上方的长导管的作用是_________________ ;D、E两支试管中CCl4的作用是_____________ 。
(3)加热过程中,观察到A试管中出现大量白色烟雾,起初部分烟雾在试管上部内壁析出淡黄色固体物质,在持续加热浓硫酸(沸腾)时,淡黄色固体物质又慢慢地消失。写出淡黄色固体消失的化学反应方程式:_______________ 。
(4)对A试管中的浓H2SO4和铜丝进行加热,很快发现C试管中品红溶液褪色,但始终未见D试管中澄清石灰水出现浑浊或沉淀。你的猜想是:______________ 。设计实验验证你的猜想_____________ 。
(5)根据上述研究,结合所学知识,你认为液面下方铜丝表面的黑色物质成分是_______ 。(写化学式)

实验选用细铜丝、98.3% H2SO4、品红溶液、澄清石灰水、CCl4、NaOH溶液等药品,铜丝被卷成螺旋状,一端没入浓H2SO4中,另一端露置在液面上方。
以下是该学习小组部分交流记录及后续探究实验的记录:
材料一:小组交流摘录
学生1:加热前,无现象发生;加热后,液面下铜丝变黑,产生气泡,有细小黑色颗粒状物质从铜丝表面进入浓硫酸中,黑色物质是什么?值得探究!
学生2:,我也观察到黑色颗粒状物质,后来逐渐转变为灰白色固体,我想该灰白色固体极有可能是未溶于浓硫酸的CuSO4。
学生3:你们是否注意到液面以上的铜丝也发黑,而且试管上部内壁有少量淡黄色S固体凝聚,会不会液面以上的铜丝与硫发生了反应,我查资料发现:2Cu+S = Cu2S(黑色)。
材料二:探究实验剪辑
实验1 将光亮的铜丝在酒精灯火焰上灼烧变黑,然后插入稀硫酸中,铜丝重新变得光亮,溶液呈蓝绿色;将光亮的铜丝置入加热的硫蒸气中变黑,然后插入稀硫酸中无变化。
实验2 截取浓硫酸液面上方变黑的铜丝,插入稀硫酸中无变化;将浓硫酸液面下方变黑的铜丝,插入稀硫酸,黑色明显变浅,溶液呈蓝绿色。
实验3 将溶液中的黑色颗粒状物质,经过滤、稀硫酸洗、蒸馏水洗、干燥后放入氧气流中加热,然后冷却,用电子天平称重发现质量减少10%左右。
根据上述材料回答下列问题:
(1)CuSO4可由金属铜与浓硫酸反应制备,该反应的化学方程式为
(2)A试管上方的长导管的作用是
(3)加热过程中,观察到A试管中出现大量白色烟雾,起初部分烟雾在试管上部内壁析出淡黄色固体物质,在持续加热浓硫酸(沸腾)时,淡黄色固体物质又慢慢地消失。写出淡黄色固体消失的化学反应方程式:
(4)对A试管中的浓H2SO4和铜丝进行加热,很快发现C试管中品红溶液褪色,但始终未见D试管中澄清石灰水出现浑浊或沉淀。你的猜想是:
(5)根据上述研究,结合所学知识,你认为液面下方铜丝表面的黑色物质成分是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐3】水泥是重要的建筑材料。水泥熟料的主要成分为CaO、SiO2,并含有一定量的铁、铝和镁等金属的氧化物。实验室测定水泥样品中钙含量的过程如图所示:

(1)水泥是最常用的建筑材料,它属于___ (填字母)。
a.金属材料 b.无机非金属材料 c.有机高分子材料
(2)在分解水泥样品过程中,盐酸为溶剂,氯化铵为助溶剂,硝酸作用是___ 。
(3)沉淀A是普通玻璃的主要成分,写出沉淀A与纯碱反应的化学方程式___ 。
(4)用氨水调节pH为4~5的目的是___ 。
(5)某研究所利用SDTQ600热分析仪对草酸钙晶体(CaC2O4·xH2O)进行热分解,得相关数据,绘制成固体质量-分解温度的关系图。

①固体质量变为5.60g时的成分是___ 。(填化学式)
②x的值是___ 。

(1)水泥是最常用的建筑材料,它属于
a.金属材料 b.无机非金属材料 c.有机高分子材料
(2)在分解水泥样品过程中,盐酸为溶剂,氯化铵为助溶剂,硝酸作用是
(3)沉淀A是普通玻璃的主要成分,写出沉淀A与纯碱反应的化学方程式
(4)用氨水调节pH为4~5的目的是
(5)某研究所利用SDTQ600热分析仪对草酸钙晶体(CaC2O4·xH2O)进行热分解,得相关数据,绘制成固体质量-分解温度的关系图。

①固体质量变为5.60g时的成分是
②x的值是
您最近一年使用:0次



