有一应用前景广阔的纳米材料甲,其由A、B两种短周期非金属元素组成,难溶于水,且硬度大,熔点高。取材料甲与熔融的烧碱反应,生成一种含A元素的含氧酸盐乙和一种含B元素的气体丙,丙能使湿润的红色石蕊试纸变蓝;乙能溶于水,加盐酸产生白色沉淀,盐酸过量沉淀不溶解。
(1)甲的化学式为____________ ,其晶体属于____________ 晶体。
(2)乙的水溶液可以用来做________________________ (写出一种用途)。
(3)B元素的一种氢化物丁,相对分子质量为32,常温下为液体,其燃烧放热多且燃烧产物对环境无污染,因此可用作火箭燃料、燃料电池燃料等。则
①丁的电子式为_____ 。
②丁可由次氯酸钠与过量氨气反应制得,其化学方程式________________________ 。
甲的制备过程中氨气需要过量的理由是____________________________________ 。
③丁的水溶液呈弱碱性,室温下其电离常数K1≈1.0×10-6,则0.01 mol·L-1丁水溶液的pH等于____________ (忽略丁的二级电离和H2O的电离)。
(1)甲的化学式为
(2)乙的水溶液可以用来做
(3)B元素的一种氢化物丁,相对分子质量为32,常温下为液体,其燃烧放热多且燃烧产物对环境无污染,因此可用作火箭燃料、燃料电池燃料等。则
①丁的电子式为
②丁可由次氯酸钠与过量氨气反应制得,其化学方程式
甲的制备过程中氨气需要过量的理由是
③丁的水溶液呈弱碱性,室温下其电离常数K1≈1.0×10-6,则0.01 mol·L-1丁水溶液的pH等于
更新时间:2019-09-06 22:02:09
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
名校
【推荐1】X、Y、Z四种主族元素的单质在常温下都是气体,X、Y、Z对应的单质可以两两反应生成相应的A、B、C三个分子,其中B、C都是10电子且含有相同的元素X。A是一种难溶于水的有毒气体。他们之间还存在下列关系:
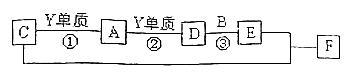
请回答下列问题:
(1)Z的原子结构示意图________ ,C的电子式为________ 。
(2)反应②的现象为______ ;写出反应③的化学方程式_________________________
(3)化合物F中含有的化合键为___________ 。

请回答下列问题:
(1)Z的原子结构示意图
(2)反应②的现象为
(3)化合物F中含有的化合键为
您最近半年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐2】A、B、C、D、E五瓶透明溶液,分别是 、
、 、
、 、
、 、
、 中的一种。已知:
中的一种。已知:
①A与B反应有气体生成;
②B与C反应有沉淀生成;
③C与D反应有沉淀生成;
④D与E反应有沉淀生成;
⑤A与E反应有气体生成;
⑥在 和
和 的反应中生成的沉淀是同一种物质。请填空:
的反应中生成的沉淀是同一种物质。请填空:
(1)在 和
和 的反应中,生成的沉淀物质的化学式是
的反应中,生成的沉淀物质的化学式是___________ 。
(2)C是___________ ,D是___________ 。(填写化学式)
(3) 与
与 反应的离子方程式是
反应的离子方程式是___________ 。
Ⅱ.某无色透明溶液中可能大量存在 、
、 、
、 、
、 、
、 中的几种。请填写下列空白:
中的几种。请填写下列空白:
(4)不做任何实验就可以肯定原溶液中不存在的离子___________ (填写化学式)。
(5)取少量原溶液,加入过量稀盐酸,有白色沉淀生成;再加入过量的稀硝酸,沉淀不消失。说明原溶液中,肯定存在的离子是___________ (填写化学式),有关离子方程式为___________ 。
(6)原溶液可能大量存在的阴离子是下列的___________。
 、
、 、
、 、
、 、
、 中的一种。已知:
中的一种。已知:①A与B反应有气体生成;
②B与C反应有沉淀生成;
③C与D反应有沉淀生成;
④D与E反应有沉淀生成;
⑤A与E反应有气体生成;
⑥在
 和
和 的反应中生成的沉淀是同一种物质。请填空:
的反应中生成的沉淀是同一种物质。请填空:(1)在
 和
和 的反应中,生成的沉淀物质的化学式是
的反应中,生成的沉淀物质的化学式是(2)C是
(3)
 与
与 反应的离子方程式是
反应的离子方程式是Ⅱ.某无色透明溶液中可能大量存在
 、
、 、
、 、
、 、
、 中的几种。请填写下列空白:
中的几种。请填写下列空白:(4)不做任何实验就可以肯定原溶液中不存在的离子
(5)取少量原溶液,加入过量稀盐酸,有白色沉淀生成;再加入过量的稀硝酸,沉淀不消失。说明原溶液中,肯定存在的离子是
(6)原溶液可能大量存在的阴离子是下列的___________。
A. | B. | C. | D. |
您最近半年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐3】A、B、C、D 均为中学所学的常见物质且均含有同一种元素,它们之间的转化关系如下图所示(反应条件及其他物质已经略去):
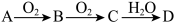
(1)若 A 是一种金属,C 是淡黄色固体,C 的阴阳离子个数比为_______ ;
(2)若 A 为淡黄色固体单质,写出 D 的浓溶液与铜反应的化学方程式_______ ;
(3)若 A 是化合物,C 是红棕色气体,则 A 的化学式为_____ ;C 转化为 D 的过程中,氧化剂与还原剂的质量比为_____ 。
(4)若 A 为黑色固体单质,C 是空气中的主要温室气体。C 还可以转化为 A,写出该反应的化学方程 式______ 。
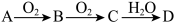
(1)若 A 是一种金属,C 是淡黄色固体,C 的阴阳离子个数比为
(2)若 A 为淡黄色固体单质,写出 D 的浓溶液与铜反应的化学方程式
(3)若 A 是化合物,C 是红棕色气体,则 A 的化学式为
(4)若 A 为黑色固体单质,C 是空气中的主要温室气体。C 还可以转化为 A,写出该反应的化学方程 式
您最近半年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】 是黄棕色具有强烈刺激性气味的气体,是一种强氧化剂,易溶于水且会与水反应生成次氯酸,与有机物、还原剂接触或浓度较大时加热会发生燃烧并爆炸。制取
是黄棕色具有强烈刺激性气味的气体,是一种强氧化剂,易溶于水且会与水反应生成次氯酸,与有机物、还原剂接触或浓度较大时加热会发生燃烧并爆炸。制取 的装置如下图所示。(已知:氨气易液化)
的装置如下图所示。(已知:氨气易液化)

已知: 的熔点为
的熔点为 ℃,沸点为3.8℃,
℃,沸点为3.8℃, 的沸点为
的沸点为 ℃;
℃; 。
。
根据题给信息,请回答下列问题:
(1)装置②盛装的试剂是__________ ,装置③的作用__________ 。
(2)过程中通入干燥空气的目的是__________ ,装置④与⑤之间不用橡皮管连接,目的是__________ 。
(3)写出工业制备 的化学方程式
的化学方程式__________ 。
(4)工业上常以 为原料制备“84”消毒液,现设计以下实验探究消毒液的性质:
为原料制备“84”消毒液,现设计以下实验探究消毒液的性质:
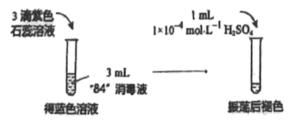
根据实验现象,可得“84”消毒液呈__________ (填“酸性”或“碱性”);
溶液褪色的原因是__________ (用离子方程式和必要文字说明)。
 是黄棕色具有强烈刺激性气味的气体,是一种强氧化剂,易溶于水且会与水反应生成次氯酸,与有机物、还原剂接触或浓度较大时加热会发生燃烧并爆炸。制取
是黄棕色具有强烈刺激性气味的气体,是一种强氧化剂,易溶于水且会与水反应生成次氯酸,与有机物、还原剂接触或浓度较大时加热会发生燃烧并爆炸。制取 的装置如下图所示。(已知:氨气易液化)
的装置如下图所示。(已知:氨气易液化)
已知:
 的熔点为
的熔点为 ℃,沸点为3.8℃,
℃,沸点为3.8℃, 的沸点为
的沸点为 ℃;
℃; 。
。根据题给信息,请回答下列问题:
(1)装置②盛装的试剂是
(2)过程中通入干燥空气的目的是
(3)写出工业制备
 的化学方程式
的化学方程式(4)工业上常以
 为原料制备“84”消毒液,现设计以下实验探究消毒液的性质:
为原料制备“84”消毒液,现设计以下实验探究消毒液的性质:
根据实验现象,可得“84”消毒液呈
溶液褪色的原因是
您最近半年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】下图中A~H均为中学化学中常见的物质,A、B、H为气体,反应①是重要的工业反应,它们之间有如下转化关系。(反应中生成的水已略去)

请回答以下问题:
(1)B是_______ ,D是_______ ,G是_______ ,H是_______ (均填化学式)。
(2)工业上常利用反应①制取漂白粉,该反应的化学方程式为_______ 。漂白粉溶于水后,受空气中的 作用,即产生有漂白、杀菌作用的次氯酸,化学方程式为
作用,即产生有漂白、杀菌作用的次氯酸,化学方程式为_______ 。

请回答以下问题:
(1)B是
(2)工业上常利用反应①制取漂白粉,该反应的化学方程式为
 作用,即产生有漂白、杀菌作用的次氯酸,化学方程式为
作用,即产生有漂白、杀菌作用的次氯酸,化学方程式为
您最近半年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】含氯消毒剂有多种, 可用于自来水消毒,84消毒液用于家庭、宾馆的消毒。实验室可用亚氯酸钠固体与
可用于自来水消毒,84消毒液用于家庭、宾馆的消毒。实验室可用亚氯酸钠固体与 制备
制备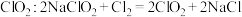 ,装置如图所示:
,装置如图所示:
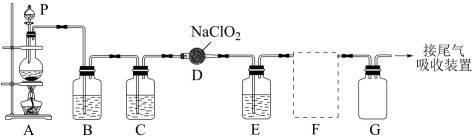
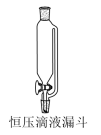
(1)仪器P的名称为___________ ,有同学认为应将P换为恒压滴液漏斗,与仪器P对比,其优点是___________ 。A装置中发生反应的离子方程式为___________
(2)B、C、E中盛装的液体依次是___________ (填编号)
a.浓硫酸 b.饱和食盐水 c. 溶液 d.
溶液 d.
(3)F处应选用的收集装置是___________ (填序号),其中与E装置导管相连的导管口是___________ (填接口字母)

(4)一种有效成分为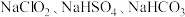 的“二氧化氯泡腾片”,能快速溶于水,溢出大量气泡,得到
的“二氧化氯泡腾片”,能快速溶于水,溢出大量气泡,得到 溶液。上述过程中,生成
溶液。上述过程中,生成 的反应属于歧化反应,每生成
的反应属于歧化反应,每生成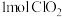 消耗
消耗 的量为
的量为___________  ;产生“气泡”的化学方程式为
;产生“气泡”的化学方程式为___________ 。
(5)用于环境杀菌消毒的 溶液须稀释并及时使用,若暴露在空气中时间过长且见光,将会导致消毒作用减弱,写出该过程的离子方程式
溶液须稀释并及时使用,若暴露在空气中时间过长且见光,将会导致消毒作用减弱,写出该过程的离子方程式___________ ,(已知: ,
, )
)
(6)某同学模仿氯碱工业,在家中用电解法自制出与“84消毒液”成分( 和水)相同的消毒液。
和水)相同的消毒液。

实验过程:向一个矿泉水瓶中装入自来水并加入3勺食盐,用卫生纸将用铅笔做成的电极包好并插入纯净水瓶中装置如图接通电源后,可以看到一侧电极无明显现象另一侧电极有细小的气泡产生。用该方法制备消毒液的总化学方程式是:___________ 。
 可用于自来水消毒,84消毒液用于家庭、宾馆的消毒。实验室可用亚氯酸钠固体与
可用于自来水消毒,84消毒液用于家庭、宾馆的消毒。实验室可用亚氯酸钠固体与 制备
制备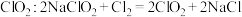 ,装置如图所示:
,装置如图所示:

(1)仪器P的名称为
(2)B、C、E中盛装的液体依次是
a.浓硫酸 b.饱和食盐水 c.
 溶液 d.
溶液 d.
(3)F处应选用的收集装置是

(4)一种有效成分为
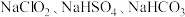 的“二氧化氯泡腾片”,能快速溶于水,溢出大量气泡,得到
的“二氧化氯泡腾片”,能快速溶于水,溢出大量气泡,得到 溶液。上述过程中,生成
溶液。上述过程中,生成 的反应属于歧化反应,每生成
的反应属于歧化反应,每生成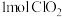 消耗
消耗 的量为
的量为 ;产生“气泡”的化学方程式为
;产生“气泡”的化学方程式为(5)用于环境杀菌消毒的
 溶液须稀释并及时使用,若暴露在空气中时间过长且见光,将会导致消毒作用减弱,写出该过程的离子方程式
溶液须稀释并及时使用,若暴露在空气中时间过长且见光,将会导致消毒作用减弱,写出该过程的离子方程式 ,
, )
)(6)某同学模仿氯碱工业,在家中用电解法自制出与“84消毒液”成分(
 和水)相同的消毒液。
和水)相同的消毒液。
实验过程:向一个矿泉水瓶中装入自来水并加入3勺食盐,用卫生纸将用铅笔做成的电极包好并插入纯净水瓶中装置如图接通电源后,可以看到一侧电极无明显现象另一侧电极有细小的气泡产生。用该方法制备消毒液的总化学方程式是:
您最近半年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐1】氢叠氮酸( )和莫尔盐
)和莫尔盐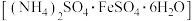 是两种常用工业原料。
是两种常用工业原料。
(1) 易溶于水,25℃时,该酸的电离常数为
易溶于水,25℃时,该酸的电离常数为
① 在水溶液中的电离方程式为
在水溶液中的电离方程式为___________ 。
②初始浓度为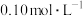 的
的 溶液,达电离平衡后,溶液的pH=
溶液,达电离平衡后,溶液的pH=___________ 。
③已知T℃时,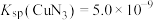 ,
, ,在此温度下,
,在此温度下, ,该反应正反应方向
,该反应正反应方向___________ (填“能”或“不能”)基本进行完全(已知但 时,反应就进行的基本完全),请通过计算说明
时,反应就进行的基本完全),请通过计算说明___________ 。
(2)在 溶液中,加入固体
溶液中,加入固体 可制备莫尔盐晶体,为了测定产品纯度,称取
可制备莫尔盐晶体,为了测定产品纯度,称取 产品溶于水,配制成500mL溶液,用浓度为
产品溶于水,配制成500mL溶液,用浓度为 的酸性高锰酸钾溶液滴定,每次所取待测液体积均为
的酸性高锰酸钾溶液滴定,每次所取待测液体积均为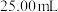 ,实验结果记录如下(已知莫尔盐的相对分子质量为392):
,实验结果记录如下(已知莫尔盐的相对分子质量为392):
滴定终点的现象是___________ ,通过实验数据计算该产品的纯度为___________ (用含字母a、c的式子表示)。上表中第一次实验的记录数据明显大于后两次,其原因可能是___________ (填字母)。
A.第一次滴定时,锥形瓶用待测液润洗
B.该酸性高锰酸钾标准液保存时间过长,部分变质
C.滴定前酸式滴定管中尖嘴处有气泡,滴定结束后气泡消失
 )和莫尔盐
)和莫尔盐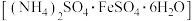 是两种常用工业原料。
是两种常用工业原料。(1)
 易溶于水,25℃时,该酸的电离常数为
易溶于水,25℃时,该酸的电离常数为
①
 在水溶液中的电离方程式为
在水溶液中的电离方程式为②初始浓度为
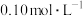 的
的 溶液,达电离平衡后,溶液的pH=
溶液,达电离平衡后,溶液的pH=③已知T℃时,
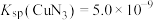 ,
, ,在此温度下,
,在此温度下, ,该反应正反应方向
,该反应正反应方向 时,反应就进行的基本完全),请通过计算说明
时,反应就进行的基本完全),请通过计算说明(2)在
 溶液中,加入固体
溶液中,加入固体 可制备莫尔盐晶体,为了测定产品纯度,称取
可制备莫尔盐晶体,为了测定产品纯度,称取 产品溶于水,配制成500mL溶液,用浓度为
产品溶于水,配制成500mL溶液,用浓度为 的酸性高锰酸钾溶液滴定,每次所取待测液体积均为
的酸性高锰酸钾溶液滴定,每次所取待测液体积均为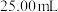 ,实验结果记录如下(已知莫尔盐的相对分子质量为392):
,实验结果记录如下(已知莫尔盐的相对分子质量为392):| 实验次数 | 第一次 | 第二次 | 第三次 |
消耗 溶液体积/mL 溶液体积/mL | 25.52 | 25.02 | 24.98 |
A.第一次滴定时,锥形瓶用待测液润洗
B.该酸性高锰酸钾标准液保存时间过长,部分变质
C.滴定前酸式滴定管中尖嘴处有气泡,滴定结束后气泡消失
您最近半年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐2】维持pH的稳定对生命体的生理活动、化学电源的高效工作等具有重要意义。
(1)常温下,在不同试剂中加入酸或碱后体系pH的变化如下表所示。
①a=___________ (忽略通入HCl气体前后体系的体积变化)。
②结合化学用语解释试剂ii显酸性的原因:___________ 。
③试剂ii中微粒浓度关系正确的有___________ (填字母序号)。
a.c(CH3COOH)>c(Na+)>c(CH3COO-)
b.2c(H+)=c(CH3COO-)-c(CH3COOH)+2c(OH-)
c.c(CH3COOH)+c(CH3COO-)=0.2mol/L
④由表中数据可知,试剂ii的pH受一定量的酸和碱的影响不大。溶液的这种能对抗外来少量强酸、强碱或适当稀释,而保持溶液的pH几乎不变的作用称为缓冲作用。下列具有缓冲作用的溶液是___________ (填字母序号)。
a.HCl—NaCl b.Na2CO3—NaHCO3
c.NH3·H2O—NH4Cl d.KOH—KCl
⑤已知:25℃时CH3COOH(aq)+OH-(aq)=CH3COO-(aq)+H2O(1) =-a kJ·mol
=-a kJ·mol
H+(aq)+OH-(aq)=H2O(1) =-b kJ·mol
=-b kJ·mol
醋酸电离的热化学方程式为___________ 。
(2)缓冲溶液应用在某种液钒电池中能稳定电池的输出电流,该电池装置示意图如下图所示,电池的总反应如下:Zn+2VOSO4+2H2SO4 ZnSO4+V2(SO4)3+2H2O
ZnSO4+V2(SO4)3+2H2O
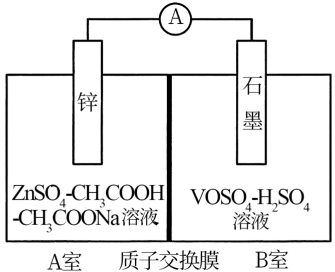
已知:VOSO4和V2(SO4)3的电离方程式分别为:
VOSO4=VO2++SO
V2(SO4)3=2V3++3SO
①放电时,B室中c(H+)___________ (填“增大”、“减小”或“不变”),结合化学用语说明理由___________ 。
②充电时,A室中的c(H+)变化缓慢的原因是___________ 。
(1)常温下,在不同试剂中加入酸或碱后体系pH的变化如下表所示。
| 试剂 | pH | ||
| 初始 | 通入0.01mol HCl气体 | 加入0.01mol NaOH固体 | |
| i.1L H2O | 7 | a | 12 |
| ii.0.10mol CH3COOH+0.10mol CH3COONa配制成1L溶液 | 4.76 | 4.67 | 4.85 |
②结合化学用语解释试剂ii显酸性的原因:
③试剂ii中微粒浓度关系正确的有
a.c(CH3COOH)>c(Na+)>c(CH3COO-)
b.2c(H+)=c(CH3COO-)-c(CH3COOH)+2c(OH-)
c.c(CH3COOH)+c(CH3COO-)=0.2mol/L
④由表中数据可知,试剂ii的pH受一定量的酸和碱的影响不大。溶液的这种能对抗外来少量强酸、强碱或适当稀释,而保持溶液的pH几乎不变的作用称为缓冲作用。下列具有缓冲作用的溶液是
a.HCl—NaCl b.Na2CO3—NaHCO3
c.NH3·H2O—NH4Cl d.KOH—KCl
⑤已知:25℃时CH3COOH(aq)+OH-(aq)=CH3COO-(aq)+H2O(1)
 =-a kJ·mol
=-a kJ·mol
H+(aq)+OH-(aq)=H2O(1)
 =-b kJ·mol
=-b kJ·mol
醋酸电离的热化学方程式为
(2)缓冲溶液应用在某种液钒电池中能稳定电池的输出电流,该电池装置示意图如下图所示,电池的总反应如下:Zn+2VOSO4+2H2SO4
 ZnSO4+V2(SO4)3+2H2O
ZnSO4+V2(SO4)3+2H2O
已知:VOSO4和V2(SO4)3的电离方程式分别为:
VOSO4=VO2++SO

V2(SO4)3=2V3++3SO

①放电时,B室中c(H+)
②充电时,A室中的c(H+)变化缓慢的原因是
您最近半年使用:0次
【推荐3】(1)水溶液中的离子平衡是中学化学中重要知识。
①常温下,0.001mol/LNaOH溶液的pH=____ ;
②(NH4)2SO4是一种重要的氮肥,长期施用会使土壤酸化,其原因是_______ (用离子方程式表示);
③已知在25℃:AgCl(s) Ag+(aq)+Cl-(aq) Ksp=1.8×10-10,Ag2S(s)
Ag+(aq)+Cl-(aq) Ksp=1.8×10-10,Ag2S(s)  2Ag+(aq)+S2-(aq) Ksp=6.3×10-50,向KCl和K2S浓度均为0.001mol/L的混合溶液中,逐滴加入AgNO3溶液,最先产生的沉淀是
2Ag+(aq)+S2-(aq) Ksp=6.3×10-50,向KCl和K2S浓度均为0.001mol/L的混合溶液中,逐滴加入AgNO3溶液,最先产生的沉淀是_____ (填“AgCl”或“Ag2S”)。
(2)甲醇是可再生能源,其燃烧热为726.5kJ·mol-1。下列能正确表示甲醇燃烧的热化学方程式的是____ (填字母代号)。
A.CH3OH(l)+ O2(g)=CO2(g)+2H2O(l) △H=+726.5kJ·mol-1
O2(g)=CO2(g)+2H2O(l) △H=+726.5kJ·mol-1
B.CH3OH(l)+ O2(g)=CO2(g)+2H2O(l) △H=−726.5kJ·mol-1
O2(g)=CO2(g)+2H2O(l) △H=−726.5kJ·mol-1
C.CH3OH+ O2=CO2+2H2O △H=−726.5kJ·mol-1
O2=CO2+2H2O △H=−726.5kJ·mol-1
(3)800℃,向某恒容密闭容器中充入反应物A,发生反应2A(g) 2B(g)+C(g) △H<0。已知A的浓度随时间的变化如下:
2B(g)+C(g) △H<0。已知A的浓度随时间的变化如下:
请回答下列问题:
①在10-20min内,A的平均反应速率为________ mol/(L.min);
②不能说明该反应达到化学平衡状态的是__________ (填字母代号);
A.容器内气体密度不再变化 B.容器内气体平均摩尔质量不再变化 C.容器内气体的压强不再变化
③800℃时,平衡常数K=_________ ;
④若温度将为600℃,其平衡常数K将________ (填“增大”、“减小”、或“不变”)。
(4)如图所示,闭合S后不久,可观察到滤纸a端附近呈蓝色,则:
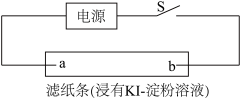
①滤纸b端与电源__________ (填“正极”或“负 极”)相连;
②滤纸a端发生的电极反应式为________ 。
①常温下,0.001mol/LNaOH溶液的pH=
②(NH4)2SO4是一种重要的氮肥,长期施用会使土壤酸化,其原因是
③已知在25℃:AgCl(s)
 Ag+(aq)+Cl-(aq) Ksp=1.8×10-10,Ag2S(s)
Ag+(aq)+Cl-(aq) Ksp=1.8×10-10,Ag2S(s)  2Ag+(aq)+S2-(aq) Ksp=6.3×10-50,向KCl和K2S浓度均为0.001mol/L的混合溶液中,逐滴加入AgNO3溶液,最先产生的沉淀是
2Ag+(aq)+S2-(aq) Ksp=6.3×10-50,向KCl和K2S浓度均为0.001mol/L的混合溶液中,逐滴加入AgNO3溶液,最先产生的沉淀是(2)甲醇是可再生能源,其燃烧热为726.5kJ·mol-1。下列能正确表示甲醇燃烧的热化学方程式的是
A.CH3OH(l)+
 O2(g)=CO2(g)+2H2O(l) △H=+726.5kJ·mol-1
O2(g)=CO2(g)+2H2O(l) △H=+726.5kJ·mol-1B.CH3OH(l)+
 O2(g)=CO2(g)+2H2O(l) △H=−726.5kJ·mol-1
O2(g)=CO2(g)+2H2O(l) △H=−726.5kJ·mol-1C.CH3OH+
 O2=CO2+2H2O △H=−726.5kJ·mol-1
O2=CO2+2H2O △H=−726.5kJ·mol-1(3)800℃,向某恒容密闭容器中充入反应物A,发生反应2A(g)
 2B(g)+C(g) △H<0。已知A的浓度随时间的变化如下:
2B(g)+C(g) △H<0。已知A的浓度随时间的变化如下:| 反应时间((min) | 0 | 10 | 20 | 30 | 40 | 50 | 60 |
| c(A)(mol/L) | 1.0 | 0.80 | 0.67 | 0.58 | 0.43 | 0.50 | 0.50 |
①在10-20min内,A的平均反应速率为
②不能说明该反应达到化学平衡状态的是
A.容器内气体密度不再变化 B.容器内气体平均摩尔质量不再变化 C.容器内气体的压强不再变化
③800℃时,平衡常数K=
④若温度将为600℃,其平衡常数K将
(4)如图所示,闭合S后不久,可观察到滤纸a端附近呈蓝色,则:

①滤纸b端与电源
②滤纸a端发生的电极反应式为
您最近半年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐1】两种非金属元素X和Y,能分别形成常见气态氢化物Q和P,Q和P都是无色刺激性气味的气体,且都极易溶于水。常温常压下,Q的密度与空气的密度之比为0.59:1。标准状况下,P的密度为1.63 g/L。Q与P能1:1化合生成盐M。
(1)元素X在周期表中的位置为__________________ ,M的电子式为________________ 。
(2)氢化物Q极易溶于水的主要原因是________________ 。
(3)X元素与氢元素组成分子式为HX3的化合物,该化合物能与Q以1:1化合生成盐W,盐W中阴离子的结构与CO2相似,写出该阴离子的结构式:________________ 。
(4)某化合物由氢元素与X、Y元素组成,分子式为XH2Y,在水中是一种缓释强效消毒剂,请用化学方程式表示其原因:_________ 。
(5)某化合物由硼元素与X元素组成,化学式为BX,有多种结晶形态,其中立方结晶被认为是目前已知最硬的物质,BX立方结晶高硬度的原因是________________ 。
(1)元素X在周期表中的位置为
(2)氢化物Q极易溶于水的主要原因是
(3)X元素与氢元素组成分子式为HX3的化合物,该化合物能与Q以1:1化合生成盐W,盐W中阴离子的结构与CO2相似,写出该阴离子的结构式:
(4)某化合物由氢元素与X、Y元素组成,分子式为XH2Y,在水中是一种缓释强效消毒剂,请用化学方程式表示其原因:
(5)某化合物由硼元素与X元素组成,化学式为BX,有多种结晶形态,其中立方结晶被认为是目前已知最硬的物质,BX立方结晶高硬度的原因是
您最近半年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐2】我国秦俑彩绘和汉代器物上用的颜料被称为“中国蓝”、“中国紫”,直到近年来人们才研究出来其成分为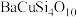 ,
,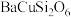 。
。
(1)“中国蓝”、“中国紫”中均具有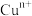 离子,
离子,
________ ,基态时该阳离子的价电子排布式为________ 。
(2)合成“中国蓝”、“中国紫”的原料有 ,孔雀石
,孔雀石 和砂子(
和砂子( )。现代文物分析发现,“中国蓝”中含有微量硫元素。假若硫元素来源于一种阴离子的立体结构型是正四面体的天然钡矿中,则该钡矿主要成分化学式是
)。现代文物分析发现,“中国蓝”中含有微量硫元素。假若硫元素来源于一种阴离子的立体结构型是正四面体的天然钡矿中,则该钡矿主要成分化学式是________ 。
(3)在5500年前,古代埃及人就已经知道如何合成蓝色颜料—“埃及蓝”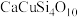 ,其合成原料中用
,其合成原料中用 代替了
代替了 ,其他和“中国蓝”一致。
,其他和“中国蓝”一致。 中键角为
中键角为________ 。根据所学,从原料分解的角度判断“埃及蓝”的合成温度比“中国蓝”更________ (填“高”或“低”)。
(4)硝酸铜溶于氨水形成 的深蓝色溶液。
的深蓝色溶液。
① 中阴离子的立体构型是
中阴离子的立体构型是________ 。 中心原子的轨道杂化类型为
中心原子的轨道杂化类型为________ 。
②氨气在一定的压强下,测得的密度比该压强下理论密度略大,请解释原因________ 。
(5)自然界中的 硬度较大,主要原因是
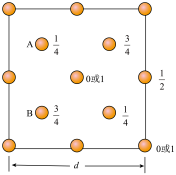
硬度较大,主要原因是________ 。下图为 晶胞中
晶胞中 原子沿
原子沿 轴方向在
轴方向在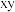 平面的投影图(即俯视图),其中
平面的投影图(即俯视图),其中 原子略去,
原子略去, 原子旁标注的数字表示每个
原子旁标注的数字表示每个 原子位于
原子位于 轴的高度,则
轴的高度,则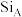 与
与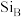 的距离是
的距离是________ 。
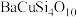 ,
,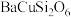 。
。(1)“中国蓝”、“中国紫”中均具有
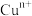 离子,
离子,
(2)合成“中国蓝”、“中国紫”的原料有
 ,孔雀石
,孔雀石 和砂子(
和砂子( )。现代文物分析发现,“中国蓝”中含有微量硫元素。假若硫元素来源于一种阴离子的立体结构型是正四面体的天然钡矿中,则该钡矿主要成分化学式是
)。现代文物分析发现,“中国蓝”中含有微量硫元素。假若硫元素来源于一种阴离子的立体结构型是正四面体的天然钡矿中,则该钡矿主要成分化学式是(3)在5500年前,古代埃及人就已经知道如何合成蓝色颜料—“埃及蓝”
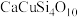 ,其合成原料中用
,其合成原料中用 代替了
代替了 ,其他和“中国蓝”一致。
,其他和“中国蓝”一致。 中键角为
中键角为(4)硝酸铜溶于氨水形成
 的深蓝色溶液。
的深蓝色溶液。①
 中阴离子的立体构型是
中阴离子的立体构型是 中心原子的轨道杂化类型为
中心原子的轨道杂化类型为②氨气在一定的压强下,测得的密度比该压强下理论密度略大,请解释原因
(5)自然界中的
 硬度较大,主要原因是
硬度较大,主要原因是 晶胞中
晶胞中 原子沿
原子沿 轴方向在
轴方向在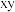 平面的投影图(即俯视图),其中
平面的投影图(即俯视图),其中 原子略去,
原子略去, 原子旁标注的数字表示每个
原子旁标注的数字表示每个 原子位于
原子位于 轴的高度,则
轴的高度,则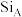 与
与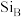 的距离是
的距离是
您最近半年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐3】硼及其化合物在新材料、工农业生产等方面用途广泛。请回答下列问题:
(1)二溴硼基二茂铁(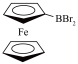 )是硼的有机化合物,写出基态Fe原子的电子排布式
)是硼的有机化合物,写出基态Fe原子的电子排布式 ___________ ;基态溴原子的最外层电子排布图 ___________ 。
(2)立方氮化硼(BN)可利用人工方法在高温高压条件下合成,属于超硬材料,同属原子晶体的氮化硼比晶体硅具有更高的硬度和耐热性的原因是:_____ 。
(3)BF3常被用于制取其他硼的化合物,BF3分子中中心原子的杂化轨道类型是___________ ,SiF4微粒的空间构型是___________ 。
(4)NaBH4被认为是有机化学中的“万能还原剂”,其中三种元素的电负性由大到小的顺序是___________ ;NaBH4的电子式为___________ 。
(5)自然界中含硼元素的钠盐是一种天然矿藏,其化学式写作 ,实际上它的结构单元是由两个
,实际上它的结构单元是由两个 和两个
和两个 缩合而成的双六元环,应该写成
缩合而成的双六元环,应该写成 ,其结构如图所示,它的阴离子可形成链状结构,则该晶体中不存在的作用力是
,其结构如图所示,它的阴离子可形成链状结构,则该晶体中不存在的作用力是___________ (填字母)。
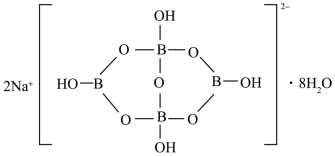
A.离子键 B.共价键 C.氢键 D.金属键
(1)二溴硼基二茂铁(
 )是硼的有机化合物,写出基态Fe原子的电子排布式
)是硼的有机化合物,写出基态Fe原子的电子排布式 (2)立方氮化硼(BN)可利用人工方法在高温高压条件下合成,属于超硬材料,同属原子晶体的氮化硼比晶体硅具有更高的硬度和耐热性的原因是:
(3)BF3常被用于制取其他硼的化合物,BF3分子中中心原子的杂化轨道类型是
(4)NaBH4被认为是有机化学中的“万能还原剂”,其中三种元素的电负性由大到小的顺序是
(5)自然界中含硼元素的钠盐是一种天然矿藏,其化学式写作
 ,实际上它的结构单元是由两个
,实际上它的结构单元是由两个 和两个
和两个 缩合而成的双六元环,应该写成
缩合而成的双六元环,应该写成 ,其结构如图所示,它的阴离子可形成链状结构,则该晶体中不存在的作用力是
,其结构如图所示,它的阴离子可形成链状结构,则该晶体中不存在的作用力是
A.离子键 B.共价键 C.氢键 D.金属键
您最近半年使用:0次



