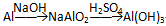某混合物甲中含有明矾[KA1(SO4)2·12H2O]、Al2O3和Fe2O3在一定条件下由甲可实现下图所示的物质之间的转化:
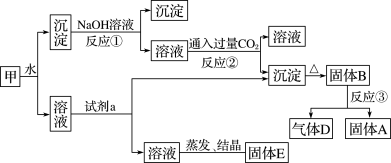
请回答下列问题:
(1)写出A、B、D的化学式:A________ 、B________ 、D___________ 。
(2)试剂a最好选用______ (填字母)
A. NaOH溶液 B.稀盐酸 C.二氧化碳 D.氨水
(3)写出反应①的离子方程式:_____________________________
(4)写出反应②中生成沉淀的化学方程式:___________________________ 。
(5)固体E可以作为复合性的化学肥料,E所含物质的化学式为_________________ 。

请回答下列问题:
(1)写出A、B、D的化学式:A
(2)试剂a最好选用
A. NaOH溶液 B.稀盐酸 C.二氧化碳 D.氨水
(3)写出反应①的离子方程式:
(4)写出反应②中生成沉淀的化学方程式:
(5)固体E可以作为复合性的化学肥料,E所含物质的化学式为
更新时间:2019-09-10 13:41:14
|
相似题推荐
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐1】氯化铝融盐电解法是以氯化铝为原料,以碱金属或碱土金属氯化物(含少量MgCl2、KCl、CaCl2)为电解质进行电解制取铝的方法。
(1)氯化铝融盐电解法需要先制纯氧化铝。以铝土矿(主要成分为Al2O3,含有少量Fe2O3、SiO2等杂质)为原料通过以下途径提纯氧化铝:
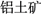
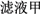


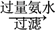
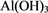
 Al2O3
Al2O3
①依次写出X、Y的成分________ ,________ 。
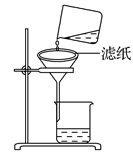
②如右图所示在实验室中进行过滤,操作中的两处错误分别是__________________________ ;____________________________ 。
(2)制备无水氯化铝的反应为:2Al2O3+6Cl2 4AlCl3+3O2
4AlCl3+3O2
③为促进该反应的进行,实际生产中需加入焦炭,其原理是____________________ 。
④加入焦炭后的化学反应可表示为Al2O3+C+Cl2 AlCl3+X↑,为确定气体X是否为混合气体,某同学将X依次通过灼热的氧化铜和澄清的石灰水,再根据现象判断。该操作是否正确?(填正确、不正确或无法判断)
AlCl3+X↑,为确定气体X是否为混合气体,某同学将X依次通过灼热的氧化铜和澄清的石灰水,再根据现象判断。该操作是否正确?(填正确、不正确或无法判断)________ ,请说明理由_________________________________________________ 。
(3)现在工业上通常用电解熔融氧化铝方式制取铝,理论上生产1吨铝消耗的氧化铝的质量________ (填“大于”、“小于”或“等于”)氯化铝质量。
(1)氯化铝融盐电解法需要先制纯氧化铝。以铝土矿(主要成分为Al2O3,含有少量Fe2O3、SiO2等杂质)为原料通过以下途径提纯氧化铝:
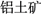
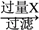
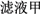


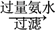
 Al2O3
Al2O3
①依次写出X、Y的成分
②如右图所示在实验室中进行过滤,操作中的两处错误分别是
(2)制备无水氯化铝的反应为:2Al2O3+6Cl2
 4AlCl3+3O2
4AlCl3+3O2③为促进该反应的进行,实际生产中需加入焦炭,其原理是
④加入焦炭后的化学反应可表示为Al2O3+C+Cl2
 AlCl3+X↑,为确定气体X是否为混合气体,某同学将X依次通过灼热的氧化铜和澄清的石灰水,再根据现象判断。该操作是否正确?(填正确、不正确或无法判断)
AlCl3+X↑,为确定气体X是否为混合气体,某同学将X依次通过灼热的氧化铜和澄清的石灰水,再根据现象判断。该操作是否正确?(填正确、不正确或无法判断)(3)现在工业上通常用电解熔融氧化铝方式制取铝,理论上生产1吨铝消耗的氧化铝的质量
您最近一年使用:0次
【推荐2】由熔盐电解法获得的粗铝含有一定量的金属钠和氢气,这些杂质可采用吹气精炼法除去,产生的尾气经处理后可用钢材镀铝。工艺流程如下:
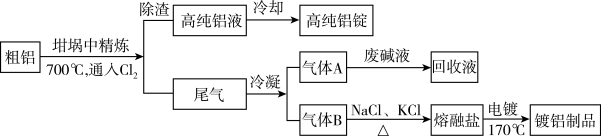
(注:NaCl熔点为801℃;AlCl3在181℃升华)
(1)工业上电解法获得金属铝的过程中,须在氧化铝中加入______ ,其目的是____ 。
(2)精炼前,需清除坩埚内的氧化铁和石英砂,防止精炼时它们分别与铝发生置换反应产生新的杂质,铝与氧化铁反应的化学方程式为:__________ 。
(3)将Cl2连续通入粗铝熔体中,杂质随气泡上浮除去。气泡的成分有____ ;固态杂质粘附于气泡上,在熔体表面形成浮渣,浮渣中的物质有________ 。
(4)在用废碱液处理A时,写出主要反应的离子方程式______ 。
(5)镀铝电解池中,以钢材镀件和铝为电极,熔融盐做电解液。则金属铝为________ 极。电镀选择在170℃下进行的原因是_________ 。采用的加热方式最好是_________ 。(填字母选项)
A 水浴 b 油浴 c 直接强热快速升温至170℃
(6)钢材表面镀铝之后,能有效防止钢材腐蚀,其原因是_______ 。

(注:NaCl熔点为801℃;AlCl3在181℃升华)
(1)工业上电解法获得金属铝的过程中,须在氧化铝中加入
(2)精炼前,需清除坩埚内的氧化铁和石英砂,防止精炼时它们分别与铝发生置换反应产生新的杂质,铝与氧化铁反应的化学方程式为:
(3)将Cl2连续通入粗铝熔体中,杂质随气泡上浮除去。气泡的成分有
(4)在用废碱液处理A时,写出主要反应的离子方程式
(5)镀铝电解池中,以钢材镀件和铝为电极,熔融盐做电解液。则金属铝为
A 水浴 b 油浴 c 直接强热快速升温至170℃
(6)钢材表面镀铝之后,能有效防止钢材腐蚀,其原因是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐3】以铝土矿(主要成分为Al2O3,含SiO2和Fe2O3等杂质)为原料生产铝和氮化铝的一种工艺流程如下[已知:SiO2在“碱溶”时转化为铝硅酸钠(NaAlSiO4·nH2O)沉淀]。
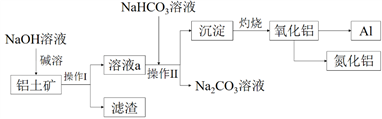
(1)操作I、Ⅱ的名称为____________ 。
(2)用氧化物的形式表示铝硅酸钠的化学式_____________ 。
(3)杂质Fe2O3最后存在于___________ 中。
(4)工业制备Al的化学方程式为__________________________ 。

(1)操作I、Ⅱ的名称为
(2)用氧化物的形式表示铝硅酸钠的化学式
(3)杂质Fe2O3最后存在于
(4)工业制备Al的化学方程式为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐1】磁性氧化铁具有广阔的应用前景,中国已成为世界磁性材料生产大国。以高硫铝土矿(主要含 、
、 、
、 ,和少量的
,和少量的 等)提取氧化铝和磁性氧化铁,其流程如下:
等)提取氧化铝和磁性氧化铁,其流程如下:

已知:
①反应III中有污染环境的 气体产生;
气体产生;
②气体II可以使湿润的红色石蕊试纸变蓝。
(1)请写出磁性氧化铁的一种用途:_______ ;滤渣Ⅰ的主要成分属于_______ 氧化物。
(2)操作I在实验中要用到的玻璃仪器有玻璃棒、_______ 、_______ 。
(3)焙烧I的过程中采用如图所示的“多层逆流焙烧”,“多层逆流焙烧”的优点是_______ (任答一点)。

(4)焙烧II中氧化铝参与反应的化学方程式为_______ 。
(5)反应III, 与
与 混合后在缺氧条件下焙烧生成
混合后在缺氧条件下焙烧生成 和
和 ,理论上完全反应消耗的
,理论上完全反应消耗的
_______ 。
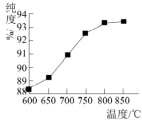
(6)反应III的煅烧温度对磁性氧化铁的纯度有很大影响。已知温度对磁性氧化铁纯度的影响如图所示,则煅烧时,温度最好控制在_______ ℃。
(7)滤液经过一系列操作可获得 ,请简述这一系列操作的具体过程:
,请简述这一系列操作的具体过程:_______ 。
 、
、 、
、 ,和少量的
,和少量的 等)提取氧化铝和磁性氧化铁,其流程如下:
等)提取氧化铝和磁性氧化铁,其流程如下:
已知:
①反应III中有污染环境的
 气体产生;
气体产生;②气体II可以使湿润的红色石蕊试纸变蓝。
(1)请写出磁性氧化铁的一种用途:
(2)操作I在实验中要用到的玻璃仪器有玻璃棒、
(3)焙烧I的过程中采用如图所示的“多层逆流焙烧”,“多层逆流焙烧”的优点是

(4)焙烧II中氧化铝参与反应的化学方程式为
(5)反应III,
 与
与 混合后在缺氧条件下焙烧生成
混合后在缺氧条件下焙烧生成 和
和 ,理论上完全反应消耗的
,理论上完全反应消耗的
(6)反应III的煅烧温度对磁性氧化铁的纯度有很大影响。已知温度对磁性氧化铁纯度的影响如图所示,则煅烧时,温度最好控制在

(7)滤液经过一系列操作可获得
 ,请简述这一系列操作的具体过程:
,请简述这一系列操作的具体过程:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐2】已知A为淡黄色固体,T、R为两种常见的用途很广的金属单质,D是具有磁性的黑色晶体,C是无色无味的气体,H是白色沉淀,且在潮湿空气中迅速变为灰绿色,最终变为红褐色固体M。

(1)写出下列物质的化学式:A:_______ ,D_______ 。
(2)按要求写出下列反应方程式:
①H在潮湿空气中变成M的过程中的化学方程式:_______ 。
②Q+B→N的离子方程式:_______ 。
(3)足量的R分别与等物质的量的HCl和B反应:
①生成H2的物质的量之比为_______ 。
②消耗R的物质的量之比为_______ 。

(1)写出下列物质的化学式:A:
(2)按要求写出下列反应方程式:
①H在潮湿空气中变成M的过程中的化学方程式:
②Q+B→N的离子方程式:
(3)足量的R分别与等物质的量的HCl和B反应:
①生成H2的物质的量之比为
②消耗R的物质的量之比为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐3】绿矾(FeSO4·7H2O)是治疗缺铁性贫血药品的重要成分。加热时,绿矾会逐渐失去结晶水,300℃时完全失去结晶水得到无水FeSO4.现利用如下工艺流程,从主要含Fe、Cu、Al及其氧化物(Fe2O3、CuO、Al2O3)的废旧金属材料中回收部分金属,同时制得绿矾。

回答下列问题:
(1)操作I、Ⅱ的名称是_______ ;滤渣Ⅱ的成分是_______ (填化学式)。
(2)碱浸时,Al2O3溶解的化学方程式为________ 。
(3)酸浸1和酸浸2用到的酸是_______ (填化学式),“酸浸2”时,发生反应的离子方程式为_______ 。
(4)由滤液Ⅱ制得绿矾需要经过一系列操作,下列说法正确的是_________ (填字母)。
a.一系列操作中包含蒸发,蒸发时要将蒸发皿中的水分蒸干然后停止加热
b.干燥绿矾晶体时,为加快干燥速率,干燥温度越高越好
c.FeSO4溶液保存时要放入一些铁粉防氧化
(5)FeSO4有还原性,定量分析中可用来标定KMnO4溶液的浓度。写出FeSO4与酸性KMnO4溶液反应的离子方程式:_________ 。

回答下列问题:
(1)操作I、Ⅱ的名称是
(2)碱浸时,Al2O3溶解的化学方程式为
(3)酸浸1和酸浸2用到的酸是
(4)由滤液Ⅱ制得绿矾需要经过一系列操作,下列说法正确的是
a.一系列操作中包含蒸发,蒸发时要将蒸发皿中的水分蒸干然后停止加热
b.干燥绿矾晶体时,为加快干燥速率,干燥温度越高越好
c.FeSO4溶液保存时要放入一些铁粉防氧化
(5)FeSO4有还原性,定量分析中可用来标定KMnO4溶液的浓度。写出FeSO4与酸性KMnO4溶液反应的离子方程式:
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】由短周期元素组成的化合物X是某抗酸药的有效成分。某同学欲探究X的组成。
查阅资料:①由短周期元素组成的抗酸药的有效成分有碳酸氢钠、碳酸镁、氢氧化铝、硅酸镁铝、磷酸铝、碱式碳酸镁铝。
②Al3+在pH=5.0时沉淀完全;Mg2+在pH=8.8时开始沉淀,在pH=11.4时沉淀完全。
实验过程:
Ⅰ.向化合物X粉末中加入过量盐酸,产生气体A,得到无色溶液。
Ⅱ.用铂丝蘸取少量Ⅰ中所得的溶液,在火焰上灼烧,无黄色火焰。
Ⅲ.向Ⅰ中所得的溶液中滴加氨水,调节pH至5~6,产生白色沉淀B,过滤。
Ⅳ.向沉淀B中加过量NaOH溶液,沉淀全部溶解。
Ⅴ.向Ⅲ中得到的滤液中滴加NaOH溶液,调节pH至12,得到白色沉淀C。
(1)Ⅰ中气体A可使澄清石灰水变浑浊,A的化学式是________ 。
(2)由Ⅰ、Ⅱ判断X一定不含有的元素是磷、________ 。
(3)Ⅲ中生成B的离子方程式是__________________________________________________ 。
(4)Ⅳ中B溶解的离子方程式是__________________________________________________ 。
(5)沉淀C的化学式是________ 。
(6)若上述n(A)∶n(B)∶n(C)=1∶1∶3,则X的化学式是__________________________ 。
查阅资料:①由短周期元素组成的抗酸药的有效成分有碳酸氢钠、碳酸镁、氢氧化铝、硅酸镁铝、磷酸铝、碱式碳酸镁铝。
②Al3+在pH=5.0时沉淀完全;Mg2+在pH=8.8时开始沉淀,在pH=11.4时沉淀完全。
实验过程:
Ⅰ.向化合物X粉末中加入过量盐酸,产生气体A,得到无色溶液。
Ⅱ.用铂丝蘸取少量Ⅰ中所得的溶液,在火焰上灼烧,无黄色火焰。
Ⅲ.向Ⅰ中所得的溶液中滴加氨水,调节pH至5~6,产生白色沉淀B,过滤。
Ⅳ.向沉淀B中加过量NaOH溶液,沉淀全部溶解。
Ⅴ.向Ⅲ中得到的滤液中滴加NaOH溶液,调节pH至12,得到白色沉淀C。
(1)Ⅰ中气体A可使澄清石灰水变浑浊,A的化学式是
(2)由Ⅰ、Ⅱ判断X一定不含有的元素是磷、
(3)Ⅲ中生成B的离子方程式是
(4)Ⅳ中B溶解的离子方程式是
(5)沉淀C的化学式是
(6)若上述n(A)∶n(B)∶n(C)=1∶1∶3,则X的化学式是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐2】随着钴酸锂电池的普及使用,从废旧的钴酸锂电池中提取锂、钴等金属材料意义重大。下图是废旧钴酸锂电池材料(主要成分为 ,含少量铁、铝、铜等元素的化合物)回收工艺流程:
,含少量铁、铝、铜等元素的化合物)回收工艺流程:________ 。
(2)滤液1中加入 的主要目的是
的主要目的是________ 。
(3)加入 氧化
氧化 的离子方程式为
的离子方程式为________ 。
(4)滤液1经过一系列反应后,加入氨水生成氢氧化铝的离子方程式为________ 。
(5)“沉钴”过程中, 的加入量(图甲)、沉淀反应的温度(图乙)与钴的沉淀率关系如图所示:
的加入量(图甲)、沉淀反应的温度(图乙)与钴的沉淀率关系如图所示: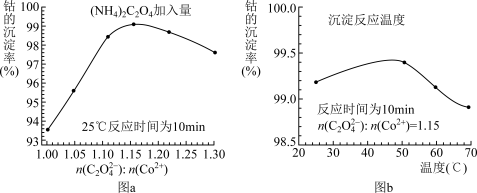
根据图分析:沉钴时应控制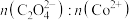 为
为________ ,温度控制在________ ℃左右。
(6)已知100kg废旧的锂电池中钴酸锂( )的含量为9.8%,若按照上述生产流程,可以生成
)的含量为9.8%,若按照上述生产流程,可以生成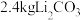 ,则其产率为
,则其产率为________ (保留一位小数)。
 ,含少量铁、铝、铜等元素的化合物)回收工艺流程:
,含少量铁、铝、铜等元素的化合物)回收工艺流程: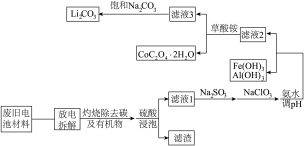
(2)滤液1中加入
 的主要目的是
的主要目的是(3)加入
 氧化
氧化 的离子方程式为
的离子方程式为(4)滤液1经过一系列反应后,加入氨水生成氢氧化铝的离子方程式为
(5)“沉钴”过程中,
 的加入量(图甲)、沉淀反应的温度(图乙)与钴的沉淀率关系如图所示:
的加入量(图甲)、沉淀反应的温度(图乙)与钴的沉淀率关系如图所示:
根据图分析:沉钴时应控制
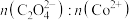 为
为(6)已知100kg废旧的锂电池中钴酸锂(
 )的含量为9.8%,若按照上述生产流程,可以生成
)的含量为9.8%,若按照上述生产流程,可以生成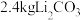 ,则其产率为
,则其产率为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐1】铝土矿的主要成分是 和少量
和少量 、
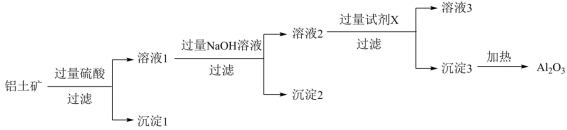
、 ,是工业制备铝单质的原料。模拟铝土矿制备
,是工业制备铝单质的原料。模拟铝土矿制备 的工艺流程如图所示。
的工艺流程如图所示。
查阅资料可知: 难溶于酸和水。
难溶于酸和水。
(1)溶液1中的金属阳离子包括______ 和______ 。
(2)写出向溶液1中加入过量 溶液的离子方程式
溶液的离子方程式______ 。
(3)试剂X可以是______ (填选项字母)。
a.稀 b.氨水 c.
b.氨水 c.
 和少量
和少量 、
、 ,是工业制备铝单质的原料。模拟铝土矿制备
,是工业制备铝单质的原料。模拟铝土矿制备 的工艺流程如图所示。
的工艺流程如图所示。
查阅资料可知:
 难溶于酸和水。
难溶于酸和水。(1)溶液1中的金属阳离子包括
(2)写出向溶液1中加入过量
 溶液的离子方程式
溶液的离子方程式(3)试剂X可以是
a.稀
 b.氨水 c.
b.氨水 c.
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
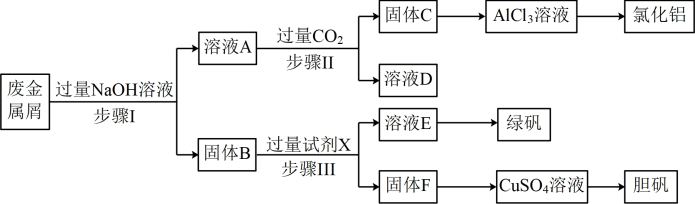
【推荐2】某工厂的废金属屑中主要成分为Cu、Fe和Al,此外还含有少量Al2O3和Fe2O3,为探索工业废料的再利用,某化学兴趣小组设计了如下实验流程,用该工厂的合金废料制取氯化铝、绿矾晶体(FeSO4·7H2O)和胆矾(CuSO4·5H2O)晶体。
请回答:
(1)步骤Ⅰ中的离子方程式有_______ 、_______ 。
(2)试剂X是_______ 。步骤Ⅱ反应的离子方程式:_______ 。
(3)在步骤Ⅱ时,用如图装置制取CO2并通入从上述流程取出的A溶液中。一段时间后,观察到烧杯中产生的白色沉淀会逐渐减少。为避免固体C减少,在本装置中应采取的改进措施是_______ 。
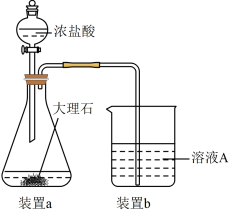
(4)由固体F制取硫酸铜溶液,通常有两种方案:
方案一:将固体F在加热条件下与浓硫酸反应〔Cu+2H2SO4(浓) CuSO4+SO2↑+2H2O〕;
CuSO4+SO2↑+2H2O〕;
方案二:将固体F投入热的稀硫酸中,然后再通入氧气;
方案一相对于方案二的缺点是:_______ (回答两条)。由CuSO4溶液通常经过蒸发浓缩、_______ 、过滤洗涤并干燥等操作得到较纯胆矾晶体。

请回答:
(1)步骤Ⅰ中的离子方程式有
(2)试剂X是
(3)在步骤Ⅱ时,用如图装置制取CO2并通入从上述流程取出的A溶液中。一段时间后,观察到烧杯中产生的白色沉淀会逐渐减少。为避免固体C减少,在本装置中应采取的改进措施是

(4)由固体F制取硫酸铜溶液,通常有两种方案:
方案一:将固体F在加热条件下与浓硫酸反应〔Cu+2H2SO4(浓)
 CuSO4+SO2↑+2H2O〕;
CuSO4+SO2↑+2H2O〕;方案二:将固体F投入热的稀硫酸中,然后再通入氧气;
方案一相对于方案二的缺点是:
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐3】某Al2O3样品中含有一定量的Cu、Fe、Fe2O3杂质。现通过下列生产过程,从该样品中提纯Al2O3,并回收铁红。流程如图:

(1)操作①是_______ ,在实验室进行该操作需要的玻璃仪器有_______ 。
(2)试剂①是_______ ,样品加入试剂①发生反应的离子方程式是_______ 。
(3)固体①加入适量稀盐酸,可能发生的反应有:_______ (用离子方程式表达)。
(4)溶液③中铁元素的存在形式是_______ ,如何用实验证明:_______ 。
(5)溶液③中通入某气体,该气体可以是_______ (任写一种的化学式)

(1)操作①是
(2)试剂①是
(3)固体①加入适量稀盐酸,可能发生的反应有:
(4)溶液③中铁元素的存在形式是
(5)溶液③中通入某气体,该气体可以是
您最近一年使用:0次