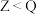短周期元素X、Y的原子序数相差2。下列有关叙述正确的是
| A.X与Y最外层电子数不可能相同 | B.X与Y一定位于同一周期 |
| C.X与Y可能形成共价化合物XY | D.X与Y不可能形成离子化合物XY |
11-12高三上·浙江杭州·阶段练习 查看更多[1]
(已下线)2012届浙江省杭州市高复高三上学期11月份月考化学试卷
更新时间:2016-12-09 02:29:57
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】下图是元素周期表中的方格,关于元素基本信息描述正确的是
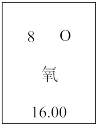

| A.“8”表示质量数 | B.“O”表示氧分子 |
| C.“氧”表示元素名称 | D.“16.00”表示质子数 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】已知短周期元素X、Y、Z、M、Q和R在周期表中的相对位置如下所示,其中Y的最高化合价为+3。下列说法不正确 的是


A.还原性: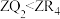 |
B.X能从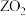 中置换出Z 中置换出Z |
C.Y能与 反应得到Fe 反应得到Fe |
| D.M最高价氧化物的水化物能与其最低价氢化物反应 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】下列有关碱金属元素、卤素原子结构和性质描述正确的是( )
①随着核电荷数的增加,碱金属单质、卤素单质的熔、沸点依次升高,密度依次增大
②F、Cl、Br、I的原子核外最外层电子数都是7,次外层电子数都是8
③碱金属单质的还原性很强,均易与氧气发生反应,加热时生成氧化物R2O
④砹是原子序数最大的卤族元素,根据卤素性质的递变规律,At与H2化合最容易
⑤根据HF、HCl、HBr、HI的稳定性逐渐减弱的事实,推出F、Cl、Br、I的非金属性逐渐增强的规律
⑥碱金属都应保存在煤油中
⑦卤素按F、Cl、Br、I的顺序,非金属性逐渐减弱的原因是随着核电荷数增加,电子层数增多,原子半径增大,得电子能力减弱
⑧碳酸铯不易发生分解反应生成氧化铯和二氧化碳
①随着核电荷数的增加,碱金属单质、卤素单质的熔、沸点依次升高,密度依次增大
②F、Cl、Br、I的原子核外最外层电子数都是7,次外层电子数都是8
③碱金属单质的还原性很强,均易与氧气发生反应,加热时生成氧化物R2O
④砹是原子序数最大的卤族元素,根据卤素性质的递变规律,At与H2化合最容易
⑤根据HF、HCl、HBr、HI的稳定性逐渐减弱的事实,推出F、Cl、Br、I的非金属性逐渐增强的规律
⑥碱金属都应保存在煤油中
⑦卤素按F、Cl、Br、I的顺序,非金属性逐渐减弱的原因是随着核电荷数增加,电子层数增多,原子半径增大,得电子能力减弱
⑧碳酸铯不易发生分解反应生成氧化铯和二氧化碳
| A.全部正确 | B.⑦⑧ |
| C.①③⑤⑥⑦ | D.①③⑦⑧ |
您最近一年使用:0次
【推荐2】下图中曲线a、b、c表示的是C、Si、P的逐级电离能,下列物理量由大到小的顺序正确的是
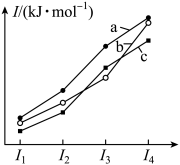

| A.原子序数:c>b>a |
| B.简单气态氢化物的稳定性:c>a>b |
| C.最高价氧化物对应水化物的酸性:b>a>c |
| D.电负性:b>c>a |
您最近一年使用:0次

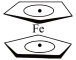
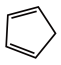 )中含有σ键的数目为5NA,π键的数目是2NA
)中含有σ键的数目为5NA,π键的数目是2NA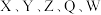 的原子序数依次增大且分占三个短周期,Z原子最外层电子数是内层电子数的3倍,
的原子序数依次增大且分占三个短周期,Z原子最外层电子数是内层电子数的3倍, 与
与 可形成离子个数比为
可形成离子个数比为 的离子化合物,
的离子化合物, 原子在同周期主族元素中原子半径最小,
原子在同周期主族元素中原子半径最小, 的原子序数之和为15,下列判断
的原子序数之和为15,下列判断 与
与