已知某溶液X可能由K+、Cu2+、Ba2+、Fe2+、AlO2-、CO32-、SO42-、I-、MnO4-中的若干种离子组成。某化学兴趣小组通过下列实验确定了其组成。
根据下列实验步骤和现象,推断实验结论:
根据下列实验步骤和现象,推断实验结论:
| 实验步骤与实验现象 | 实验结论 |
| Ⅰ.观察溶液:无色透明 | ①原溶液中一定不含的离子是 |
| Ⅱ.取适量该溶液,加入过量的硝酸,有气体生成,并得到无色溶液 | ②原溶液中一定不含的离子是 |
| Ⅲ.在Ⅱ所得溶液中再加入过量的碳酸氢铵溶液,有气体生成,同时析出白色沉淀A | ③原溶液中还一定含有的离子是 |
| Ⅳ.在Ⅲ所得溶液中再逐滴加入氢氧化钡溶液至过量,加热也有气体生成,同时析出白色沉淀B | ④白色沉淀B中一定含有 |
更新时间:2019-09-19 11:40:08
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】A、B、C、D、E均为可溶于水的固体,组成它们的离子有:
分别取它们的水溶液进行实验.
已知:Al3+ + 3OH- = Al(OH)3↓,Al(OH)3+OH-=AlO2-+2H2O结果如下:
①A溶液与B溶液反应生成白色沉淀,沉淀可溶于E溶液;
②A溶液与C溶液反应生白色沉淀,沉淀可溶于E溶液;
③A溶液与D溶液反应生成白色沉淀,沉淀可溶于盐酸;
④B溶液与适量D溶液反应生成白色沉淀,加入过量D溶液,沉淀量减少,但不消失.据此推断它们是:A_________ ;B___________ ;C___________ ;D____________ .
| 阳离子 | Na+、Mg2+、Al3+、Ba2+ |
| 阴离子 | OH﹣、Cl﹣、CO32﹣、SO42﹣、HSO4﹣ |
已知:Al3+ + 3OH- = Al(OH)3↓,Al(OH)3+OH-=AlO2-+2H2O结果如下:
①A溶液与B溶液反应生成白色沉淀,沉淀可溶于E溶液;
②A溶液与C溶液反应生白色沉淀,沉淀可溶于E溶液;
③A溶液与D溶液反应生成白色沉淀,沉淀可溶于盐酸;
④B溶液与适量D溶液反应生成白色沉淀,加入过量D溶液,沉淀量减少,但不消失.据此推断它们是:A
您最近一年使用:0次
【推荐2】某生产企业的工业废水中含有大量的FeSO4和较多的CuSO4。为了变废为宝,技术人员计划从该废水中回收FeSO4和金属Cu,工艺流程如图所示。回答下列问题:
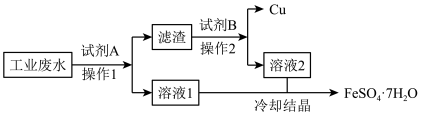
(1)“操作1”与“操作2”的名称为_______ ,在实验室中进行该操作时,所需要的玻璃仪器除烧杯外,还有_______ 。
(2)加入试剂A的目的是将 全部转化为Cu,以便回收铜单质,发生反应的离子方程式为
全部转化为Cu,以便回收铜单质,发生反应的离子方程式为______ 。
(3)“滤渣”的成分为________ ,加入的试剂B为________ (填化学式)。
(4)要鉴别“溶液2”中的金属阳离子,所需实验操作及实验现象是___________ 。

(1)“操作1”与“操作2”的名称为
(2)加入试剂A的目的是将
 全部转化为Cu,以便回收铜单质,发生反应的离子方程式为
全部转化为Cu,以便回收铜单质,发生反应的离子方程式为(3)“滤渣”的成分为
(4)要鉴别“溶液2”中的金属阳离子,所需实验操作及实验现象是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐3】今有一混合物的水溶液,只可能含有以下离子中的若干种:K+、NH4+、Cl-、Mg2+、Ba2+、CO32-、SO42-,现取三份各100mL该溶液进行如下实验:
①第一份加入AgNO3溶液有沉淀产生;
②第二份加足量NaOH溶液加热后,收集到气体0.08mol;
③第三份加足量BaCl2溶液后,得干燥沉淀12.54g,经足量盐酸洗涤、干燥后,沉淀质量为4.66g。根据上述实验,回答下列问题:
(1)由第二份进行的实验得知混合物中应含有___________ 离子,其物质的量浓度为________ 。
(2)由第三份进行的实验可知12.54克沉淀的成分是______________ (写沉淀化学式),其物质的量分别为______________________ 。
(3)原溶液中是否存在K+_______ 填“是”或“否)若存在则K+的浓度的取值范围是____________________ (若不存在此空可不填)
①第一份加入AgNO3溶液有沉淀产生;
②第二份加足量NaOH溶液加热后,收集到气体0.08mol;
③第三份加足量BaCl2溶液后,得干燥沉淀12.54g,经足量盐酸洗涤、干燥后,沉淀质量为4.66g。根据上述实验,回答下列问题:
(1)由第二份进行的实验得知混合物中应含有
(2)由第三份进行的实验可知12.54克沉淀的成分是
(3)原溶液中是否存在K+
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐1】黄铁矿烧渣(主要成分为 、
、 、
、 、
、 等)是生产硫酸的工业废渣,其综合利用对环境保护具有现实意义。利用黄铁矿烧渣为原料制备铁红
等)是生产硫酸的工业废渣,其综合利用对环境保护具有现实意义。利用黄铁矿烧渣为原料制备铁红 的流程如图所示:
的流程如图所示:

回答下列问题:
(1)铁红是炼铁的重要原料,请再说出铁红的一种用途___________ 。
(2)为了提高酸浸的速率可采取的措施是___________ (写出一种即可),“操作1”后的溶液中溶质的主要成分是___________ (填化学式)。
(3)“沉淀反应”时不宜混入过多空气,其原因为________ ,操作2的名称是_________ 。
(4) 固体会吸附硫酸根离子等杂质,为检验
固体会吸附硫酸根离子等杂质,为检验 是否洗涤干净,取最后一次洗涤液于试管,
是否洗涤干净,取最后一次洗涤液于试管,___________ ,根据现象判断是否洗涤干净。
(5)现有黄铁矿烧渣 ,铁元素的质量分数为11.2%,经过一系列转化后,得到
,铁元素的质量分数为11.2%,经过一系列转化后,得到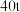 铁红,该产品的产率为
铁红,该产品的产率为___________ 。(提示:产率 )
)
 、
、 、
、 、
、 等)是生产硫酸的工业废渣,其综合利用对环境保护具有现实意义。利用黄铁矿烧渣为原料制备铁红
等)是生产硫酸的工业废渣,其综合利用对环境保护具有现实意义。利用黄铁矿烧渣为原料制备铁红 的流程如图所示:
的流程如图所示:
回答下列问题:
(1)铁红是炼铁的重要原料,请再说出铁红的一种用途
(2)为了提高酸浸的速率可采取的措施是
(3)“沉淀反应”时不宜混入过多空气,其原因为
(4)
 固体会吸附硫酸根离子等杂质,为检验
固体会吸附硫酸根离子等杂质,为检验 是否洗涤干净,取最后一次洗涤液于试管,
是否洗涤干净,取最后一次洗涤液于试管,(5)现有黄铁矿烧渣
 ,铁元素的质量分数为11.2%,经过一系列转化后,得到
,铁元素的质量分数为11.2%,经过一系列转化后,得到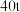 铁红,该产品的产率为
铁红,该产品的产率为 )
)
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】化合物X由5种元素组成。某兴趣小组按如下流程进行实验:
实验I
实验II
请回答:
(1)溶液F的溶质是_______ ,组成X的金属元素有_______ (填元素符号),X的化学式为_______ 。
(2)2 0.1
0.1 溶液A中加入2
溶液A中加入2 0.1
0.1
 ,再加几滴
,再加几滴 、淀粉溶液,振荡后加入5滴氯水,溶液先变红再变蓝。从上述现象中可以得到的结论有
、淀粉溶液,振荡后加入5滴氯水,溶液先变红再变蓝。从上述现象中可以得到的结论有_______ 。
(3)C→D的总化学方程式是_______ 。
(4)溶液E中的紫色离子的平均组成可表示为 ,请设计定量实验测定紫色离子中的n值:
,请设计定量实验测定紫色离子中的n值:_______ 。
实验I

实验II

请回答:
(1)溶液F的溶质是
(2)2
 0.1
0.1 溶液A中加入2
溶液A中加入2 0.1
0.1
 ,再加几滴
,再加几滴 、淀粉溶液,振荡后加入5滴氯水,溶液先变红再变蓝。从上述现象中可以得到的结论有
、淀粉溶液,振荡后加入5滴氯水,溶液先变红再变蓝。从上述现象中可以得到的结论有(3)C→D的总化学方程式是
(4)溶液E中的紫色离子的平均组成可表示为
 ,请设计定量实验测定紫色离子中的n值:
,请设计定量实验测定紫色离子中的n值:
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐3】有一固体混合物,可能由Na2CO3、Na2SO4、CuSO4、CaCl2、NaCl等物质组成,为了鉴别它们,做了如下实验:
①将固体混合物溶于水,搅拌后得到无色透明溶液;
②在①所得的溶液中滴加Ba(NO3)2溶液,有白色沉淀生成;
③过滤,然后在所得白色沉淀中加入过量稀硝酸,沉淀部分溶解。
由此判断:
(1)原混合物中肯定有___ ,肯定没有___ ,可能含有___ 。
(2)写出上述实验过程中可能发生反应的离子方程式:___ 。
(3)对可能含有的物质采用的检验方法是___ 。
①将固体混合物溶于水,搅拌后得到无色透明溶液;
②在①所得的溶液中滴加Ba(NO3)2溶液,有白色沉淀生成;
③过滤,然后在所得白色沉淀中加入过量稀硝酸,沉淀部分溶解。
由此判断:
(1)原混合物中肯定有
(2)写出上述实验过程中可能发生反应的离子方程式:
(3)对可能含有的物质采用的检验方法是
您最近一年使用:0次



