室温下,某容积固定的密闭容器由可移动的活塞隔成A、B两室,向A中充入一定量H2、O2的混合气体,向B中充入1mol空气,此时活塞的位置如图所示。
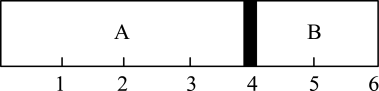
(1)A室混合气体的物质的量为_______ 。
(2)实验测得A室混合气体的质量为34g,A室中含氧气_______ mol;该混合气体的密度是同温同压时H2密度的 _______ 倍。
(3)若将A室H2、O2的混合气体点燃引爆,恢复原温度后,最终活塞停留在_____ 刻度处,容器内气体压强与反应前气体压强之比_____ 。

(1)A室混合气体的物质的量为
(2)实验测得A室混合气体的质量为34g,A室中含氧气
(3)若将A室H2、O2的混合气体点燃引爆,恢复原温度后,最终活塞停留在
更新时间:2019-10-12 12:59:47
|
相似题推荐
计算题
|
适中
(0.65)
【推荐1】室温下,某容积固定的密闭容器由可移动的挡板(厚度可忽略)隔成A、B两室,分别向A、B两室充入H2、O2的混合气体和1mol空气,此时活塞的位置如图所示。
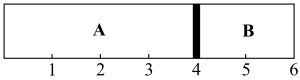
(1)A室混合气体的物质的量为_______ ,标准状况下体积为_______ 。
(2)实验测得A室混合气体的质量为34 g,则该混合气体的密度是同温同压条件下氦气密度的_______ 倍。若将A室H2、O2的混合气体点燃,恢复原温度后,最终挡板停留的位置在_______ 刻度。

(1)A室混合气体的物质的量为
(2)实验测得A室混合气体的质量为34 g,则该混合气体的密度是同温同压条件下氦气密度的
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】有以下几种物质:
①标准状况下6.72L ②
② 个HCl分子 ③7.2g
个HCl分子 ③7.2g ④0.2mol
④0.2mol
(1)①②③④中氢原子的数目之比是____________________
(2)相同温度下将①、②分别充入两个体积相同的容器中,则两容器的压强之比为________________
(3)在标准状况下,①②③④的体积由大到小的顺序是______________ (用序号回答)
(4) ,120℃时,①②③④的密度由大到小的顺序是
,120℃时,①②③④的密度由大到小的顺序是____________ (用序号回答)
①标准状况下6.72L
 ②
② 个HCl分子 ③7.2g
个HCl分子 ③7.2g ④0.2mol
④0.2mol
(1)①②③④中氢原子的数目之比是
(2)相同温度下将①、②分别充入两个体积相同的容器中,则两容器的压强之比为
(3)在标准状况下,①②③④的体积由大到小的顺序是
(4)
 ,120℃时,①②③④的密度由大到小的顺序是
,120℃时,①②③④的密度由大到小的顺序是
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐3】室温下,某容积固定的密闭容器由可移动的活塞隔成A、B两室,分别向A、B两室充入H2、O2的混合气体和1 mol空气,此时活塞的位置如图所示。
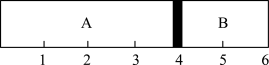
(1)A室混合气体的物质的量为________ ,标况下体积为________ 。
(2)实验测得A室混合气体的质量为34 g,则该混合气体的密度是同温同压条件下氦气密度的________ 倍。若将A室H2、O2的混合气体点燃引爆,恢复原温度后,最终活塞停留的位置在________ 刻度,容器内气体压强与反应前气体压强之比为________ 。

(1)A室混合气体的物质的量为
(2)实验测得A室混合气体的质量为34 g,则该混合气体的密度是同温同压条件下氦气密度的
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐1】(1)2molO3和3molO2的质量之比为____ ,分子数之比为____ ;同温同压下的密度之比为____ ,含氧原子数之比为_____ ,体积之比为____ 。
(2)气体化合物A的化学式可表示为OxFy,已知同温同压下10mLA受热分解生成15mLO2和10mLF2,则A的化学式为____ ,推断的依据是____ 。
(3)标准状况下,在乙室中充入1.2molHCl,甲室中充入NH3、H2的混合气体,静止时活塞如图。已知甲室中气体的质量比乙室中气体的质量少33.8g。
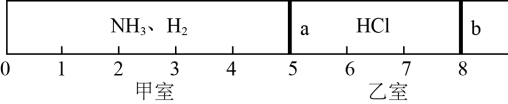
请回答下列问题:
①甲室中气体的物质的量为____ mol。
②甲室中气体的质量为____ g。
③甲室中NH3、H2的物质的量之比为___ ,质量之比为____ 。
④如果将活塞a去掉,当HCl与NH3完全反应后,活塞b将静止于刻度“____ ”(填数字)处。
(2)气体化合物A的化学式可表示为OxFy,已知同温同压下10mLA受热分解生成15mLO2和10mLF2,则A的化学式为
(3)标准状况下,在乙室中充入1.2molHCl,甲室中充入NH3、H2的混合气体,静止时活塞如图。已知甲室中气体的质量比乙室中气体的质量少33.8g。

请回答下列问题:
①甲室中气体的物质的量为
②甲室中气体的质量为
③甲室中NH3、H2的物质的量之比为
④如果将活塞a去掉,当HCl与NH3完全反应后,活塞b将静止于刻度“
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐2】填写下列空白:
(1)将等物质的量的NH3和CH4混合,混合气体中NH3与CH4的质量比为____________ 。
(2)要使NH3与CH4含相同数目的H原子,则NH3和CH4的物质的量之比为__________ 。
(3)标准状况下,密度为0.75 g·L-1的NH3与CH4组成的混合气体中,NH3的体积分数为__________ ,该混合气体对氢气的相对密度为________ 。
(4)已知a g A和b g B恰好完全反应生成0.2 mol C和d g D,则C的摩尔质量为__________________ 。
(5)同温同压下,已知O2的密度为ρg/L,则CO2的密度为__________ 。
(6)现有下列三种气体:①32 g CH4;②约含有6.02×1023个HCl分子的氯化氢气体;③标准状况下33.6 LO2。请按物理量由小到大的顺序排列:a.质量________ (填序号,下同);b.分子数目________ c.相同状况下气体的体积________ 。
(1)将等物质的量的NH3和CH4混合,混合气体中NH3与CH4的质量比为
(2)要使NH3与CH4含相同数目的H原子,则NH3和CH4的物质的量之比为
(3)标准状况下,密度为0.75 g·L-1的NH3与CH4组成的混合气体中,NH3的体积分数为
(4)已知a g A和b g B恰好完全反应生成0.2 mol C和d g D,则C的摩尔质量为
(5)同温同压下,已知O2的密度为ρg/L,则CO2的密度为
(6)现有下列三种气体:①32 g CH4;②约含有6.02×1023个HCl分子的氯化氢气体;③标准状况下33.6 LO2。请按物理量由小到大的顺序排列:a.质量
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐3】(1)现将200mL0.30mol/L的盐酸与50mL0.80mol/LCaCl2溶液混合(混合后体积变化忽略不计),所得溶液中Cl-的物质的量浓度是___ 。
(2)将20.0g氢氧化钠固体溶于水配成100mL溶液,其密度为1.25g·mL-1。该溶液中氢氧化钠的物质的量浓度为___ ,质量分数为___ ,从该溶液中取出10 mL,将其加水稀释到100 mL,稀释后溶液中氢氧化钠的物质的量浓度为___ ,将一定体积的原溶液和稀释后的溶液按1:4的体积比混合(忽略混合时溶液体积变化),所得混合溶液中氢氧化钠的物质的量浓度为___ 。
(3)气体化合物A分子式可表示为OxFy,已知同温同压下10mLA受热分解生成15mLO2和10mLF2,则A的化学式为___ ,推断的依据为___ ;
(2)将20.0g氢氧化钠固体溶于水配成100mL溶液,其密度为1.25g·mL-1。该溶液中氢氧化钠的物质的量浓度为
(3)气体化合物A分子式可表示为OxFy,已知同温同压下10mLA受热分解生成15mLO2和10mLF2,则A的化学式为
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐1】物质的量是高中常用的物理量,请回答以下有关问题
(1)0.2克H2含有__________ 个氢原子,标准状态下,由CO 和CO2 组成的混合气体共6.72 L,质量共12克,此混合物中,CO 和CO2的物质的量之比是_________ ,CO 的体积分数是_______ ,CO 的质量分数是_________ ,C 和 O 的原子个数比是_________ ,混合气体的平均相对分子质量是________ ,对氢气的相对密度是_________ 。
(2)在9.5克某二价金属的氯化物中含有0.2molCl-,此氯化物的摩尔质量为__________ ,该金属元素的相对原子质量是__________ ,标准状态下,6.72 L CO与一定量的氧化铁恰好完全反应,剩余固体的质量是_______ g
(3)0.3mol H2O 分子中所含氢原子数与______ 个NH3分子中所含氢原子数相等;8克甲烷中所含共价键的物质的量是________ ;0.5molH2O 的质量是________ 。
(1)0.2克H2含有
(2)在9.5克某二价金属的氯化物中含有0.2molCl-,此氯化物的摩尔质量为
(3)0.3mol H2O 分子中所含氢原子数与
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】Ⅰ.氧化还原反应在生产生活中普遍存在。
(1)工业上制取 的原理为:
的原理为: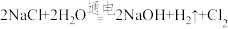 ↑ 。当收集到标准状况下224
↑ 。当收集到标准状况下224
 时,生成的
时,生成的 为
为_______ g。
(2)激光雷达的核心部件需要一种氮化铝( )导热陶瓷片。现取氮化铝样品5.0g(假设杂质只含有炭黑)与50
)导热陶瓷片。现取氮化铝样品5.0g(假设杂质只含有炭黑)与50 2.0
2.0 的
的 溶液恰好完全反应,求氮化铝样品中
溶液恰好完全反应,求氮化铝样品中 的质量分数
的质量分数_______ 已知: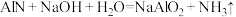 。
。
Ⅱ. 的减排已经引起国际社会的广泛关注,近日我国科学家实现了
的减排已经引起国际社会的广泛关注,近日我国科学家实现了 高选择性、高稳定性加氢合成甲醇(
高选择性、高稳定性加氢合成甲醇( )。回答下列问题:
)。回答下列问题:
(3) 的摩尔质量是
的摩尔质量是______  。
。
(4)2
 中所含原子的物质的量为
中所含原子的物质的量为_______  。
。
(5)_______ g的氢气中所含H原子的数目与1
 相同。
相同。
(6)含0.1 个O的
个O的 中有
中有_______ 个电子,标况下该 的体积为
的体积为_______ L。
(1)工业上制取
 的原理为:
的原理为: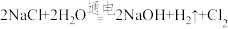 ↑ 。当收集到标准状况下224
↑ 。当收集到标准状况下224
 时,生成的
时,生成的 为
为(2)激光雷达的核心部件需要一种氮化铝(
 )导热陶瓷片。现取氮化铝样品5.0g(假设杂质只含有炭黑)与50
)导热陶瓷片。现取氮化铝样品5.0g(假设杂质只含有炭黑)与50 2.0
2.0 的
的 溶液恰好完全反应,求氮化铝样品中
溶液恰好完全反应,求氮化铝样品中 的质量分数
的质量分数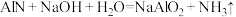 。
。Ⅱ.
 的减排已经引起国际社会的广泛关注,近日我国科学家实现了
的减排已经引起国际社会的广泛关注,近日我国科学家实现了 高选择性、高稳定性加氢合成甲醇(
高选择性、高稳定性加氢合成甲醇( )。回答下列问题:
)。回答下列问题:(3)
 的摩尔质量是
的摩尔质量是 。
。(4)2

 中所含原子的物质的量为
中所含原子的物质的量为 。
。(5)

 相同。
相同。(6)含0.1
 个O的
个O的 中有
中有 的体积为
的体积为
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐1】将1.46 g钠铝合金置于水中,合金全部溶解,产生V L(标准状况下)的H2,所得的溶液中仍含有0.02 mol NaOH。请计算:
(1)V=_______ 。
(2)合金中n(Na):n(Al)=_______ 。
(1)V=
(2)合金中n(Na):n(Al)=
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】为测定某补血剂样品[主要成分是硫酸亚铁晶体(FeSO4·7HO,M=278gmol-1)]中铁元素的含量,某化学兴趣小组设计了如下实验方案。取10片补血剂,加入一定量稀硫酸溶解后,配成250mL溶液,取25.00mL溶液于锥形瓶中,用0.00500mol·L-1酸性KMnO4溶液滴定,重复实验平均消耗酸性KMnO4溶液10.00mL。已知滴定过程反应的离子方程式为:MnO +5Fe2++8H+=Mn2++5Fe3++4H2O
+5Fe2++8H+=Mn2++5Fe3++4H2O
(1)若实验无损耗,则每片补血剂含FeSO4·7H2O含量为____ mg(列式计算)。
(2)正常人每天应补充14mg左右的铁,如果全部通过服用含FeSO4·7H2O的片剂来补充铁,则正常人每天最少需服用含FeSO4·7H2O的片剂____ 片。
 +5Fe2++8H+=Mn2++5Fe3++4H2O
+5Fe2++8H+=Mn2++5Fe3++4H2O(1)若实验无损耗,则每片补血剂含FeSO4·7H2O含量为
(2)正常人每天应补充14mg左右的铁,如果全部通过服用含FeSO4·7H2O的片剂来补充铁,则正常人每天最少需服用含FeSO4·7H2O的片剂
您最近一年使用:0次



